Содержание
- 2. Номенклатура ферментов название субстрата, реакция, катализируемая ферментом, аза – окончание.
- 3. В основе классификации лежит тип катализируемой реакции. Оксидоредуктазы катализируют окислительно-восстановительные реакции. Трансферазы - реакции с переносом
- 5. Оксидоредуктазы Окисление идёт путём дегидрирования, отщепления электрона, присоединения атома или молекулы кислорода.
- 6. Шифр фермента ЛДГ- 1.1.1.27 Подкласс определяется строением группы донора протонов и электронов. 1.1. -СН-ОН Подподкласс определяется
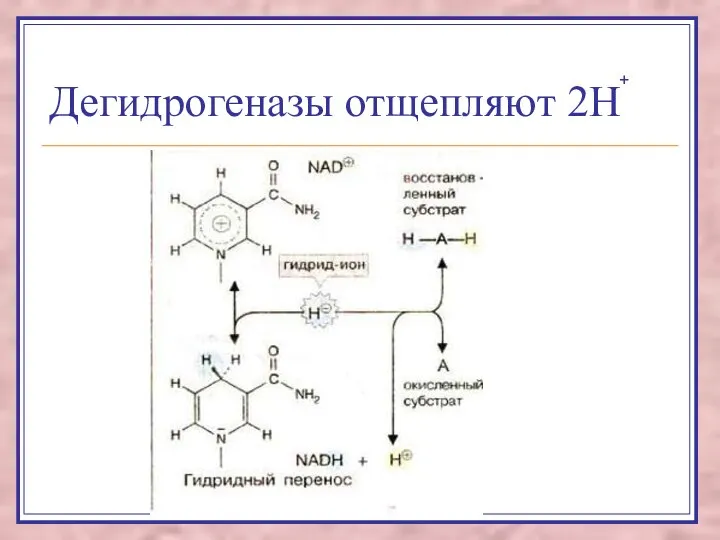
- 7. Дегидрогеназы отщепляют 2Н +
- 8. Оксидазы отщепляют водород от субстрата и передают на кислород воздуха, содержат ионы меди, в результате продуктом
- 9. Аэробные дегидрогеназы -флавопротеины удаляют водород от субстрата, акцептором водорода может быть кислород и искусственные акцепторы, оксидазы
- 10. Анаэробные дегидрогеназы удаляют водород из субстрата и передают акцептору (но не кислороду). НАД-зависимые ДГ катализируют окислительно-восстановительные
- 11. Оксигеназы катализируют введение кислорода в молекулу субстрата. Монооксигеназы (гидроксилазы). Кофермент – донор водорода (НАДФН2, аскорбиновая кислота,
- 12. Трансферазы Коферменты трансфераз: ФП, ТГФК, АТФ, ФАФС, АДФ
- 13. Подкласс определяется типом переносимой группы 2.1. – одноуглеродные остатки, 2.6. – азотистые группы. Подподкласс уточняет тип
- 14. Трансферазы фосфотрансферазы, аминотрансферазы, гликозилтрансферазы, ацилтрансферазы, переносчики одноуглеродных частиц, переносчики кетонных и альдегидных групп.
- 15. Гидролазы – простые белки.
- 16. Подкласс определяется типом расщепляемой связи 3.1. – сложноэфирные, 3.2. – гликозильные, 3.4. – пептидные. Подподкласс уточняет
- 17. В класс гидролаз входят пептидогидролазы, эстеразы, гликозидазы.
- 18. Пептидогидролазы аминопептидазы, карбоксипептидазы, дипептидазы, протеиназы (пепсин, трипсин, папаин).
- 19. Эстеразы расщепляют эфиры. карбоксиэстеразы (липаза), фосфоэстеразы (КФ, ЩФ), сульфоэстеразы. Гликозидазы катализируют гидролиз гликозидов.
- 20. Лиазы могут быть простыми и сложными белками. Коферменты: ТПФ, ФП.
- 21. Подкласс определяется типом расщепляемой связи 4.1. расщепляют связь C-C, 4.2. расщепляют связь C-O, 4.3. расщепляют связь
- 22. Примеры лиаз фумараза, альдолаза, дегидратаза, цитратсинтаза.
- 23. Изомеразы катализируют взаимопревращения изомеров цис-транс-изомеразы, мутазы, триозофосфатизомераза катализирует взаимопревращение альдоз и кетоз. Подкласс определяется характером изомерных
- 24. Лигазы Лигазы катализируют соединение двух молекул, сопряжённое с разрывом пирофосфатной связи АТФ. В ходе реакции образуются
- 25. Классификация ферментов
- 26. Классификация ферментов
- 27. Широкое использование определения активности ферментов во всём мире представляет собой одно из наиболее важных достижений современной
- 28. Энзимодиагностика применение ферментов как аналитических реактивов: - методы определения глюкозы, мочевины, активность ферментов определяют в биологических
- 29. Определение глюкозы
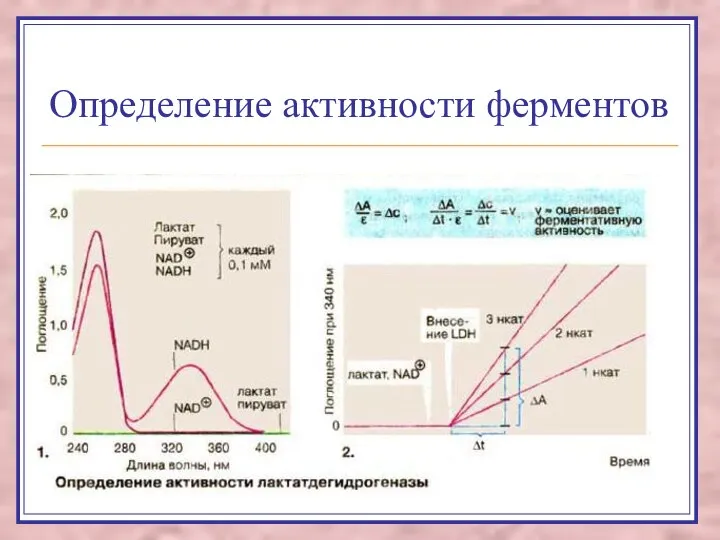
- 30. Определение активности ферментов
- 31. Гиперферментемия повышение синтеза ЩФ при рахите, повышение проницаемости мембран для АЛТ и АСТ при гепатите, некроз
- 32. Гипоферментемия уменьшение числа клеток, секретирующих фермент (ХЭ при циррозе печени, пепсиноген при гастроэктомии), избирательная недостаточность синтеза
- 33. Факторы, влияющие на активность ферментов в сыворотке крови Активность ферментов в сыворотке крови «Старение» клеток и
- 34. Диагностическое значение исследования ферментов можно повысить двумя путями определение изоферментов, определение активности нескольких ферментов.
- 35. При инфаркте миокарда исследуют ЛДГ1, МВ-КФК, АСТ, миоглобин, тропонины
- 36. При заболеваниях печени исследуют АЛТ, АСТ, ЩФ, γ-ГТП, органоспецифические ферменты печени - аргиназу, гистидазу.
- 37. Ферменты плазмы крови секреторные, индикаторные, экскреторные.
- 38. Секреторные ферменты синтезируются в печени, выделяются в плазму крови, где играют определённую физиологическую роль, снижение их
- 39. Секреторные ферменты Ренин участвует в регуляции кровяного давления. Лизоцим обеспечивает бактерицидные свойства крови. Холестеролэстераза разрушает ацетилхолин.
- 40. Индикаторные ферменты клеточные, попадают в кровь из тканей, где они выполняют определённые внутриклеточные функции.
- 41. Локализация внутриклеточных ферментов в цитоплазме клетки (ЛДГ, альдолаза), в митохондриях (ГЛДГ), в лизосомах (КФ, β-глюкуронидаза).
- 42. Цитозоль содержит ферменты гликолиза, пентозного цикла, активации аминокислот, глюконеогенеза, мультиферментный комплекс синтетазы жирных кислот, АСТ, МДГ
- 43. Ферменты митохондрий пируватдегидрогеназный комплекс, цитратсинтаза, изоцитратДГ (НАД-зависимая), МДГ и другие ферменты ЦТК, ацил-КоА-ДГ и другие ферменты
- 44. Ферменты лизосом кислая фосфатаза, β-глюкуронидаза, α-глюкозидаза, β-глюкозидаза, катепсины, кислая рибонуклеаза, кислая дезоксирибонуклеаза, α-галактозидаза, лизоцим, гиалуронидаза, арилсульфатаза,
- 45. Ферменты микросомальной фракции глюкозо-6-фосфатаза, рибосомальные ферменты белкового синтеза, ферменты, участвующие в реакциях гидроксилирования, ферменты синтеза фосфолипидов,
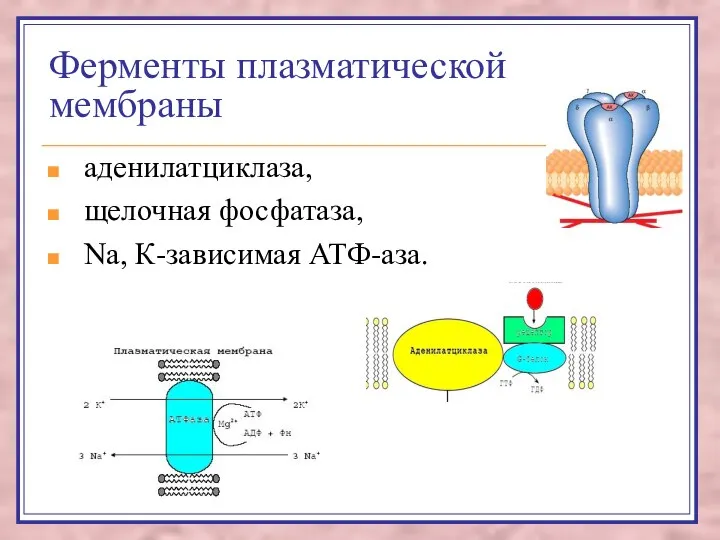
- 46. Ферменты плазматической мембраны аденилатциклаза, щелочная фосфатаза, Na, К-зависимая АТФ-аза.
- 47. Ферменты ядра ферменты репликации, транскрипции, РНК-полимераза, НАД-синтетаза.
- 48. В норме активность индикаторных ферментов в крови низкая. При поражении органа или ткани ферменты из клеток
- 49. Индикаторные ферменты неспецифические (общие для всех тканей), органоспецифические (маркёрные). Для печени: аргиназа, гистидаза, уроканиназа, сорбитолДГ, орнитинкарбомоилтрансфераза.
- 50. Распределение диагностически важных ферментов в организме
- 52. ЛДГ последний фермент гликолиза, цитоплазматический. ЛДГ +
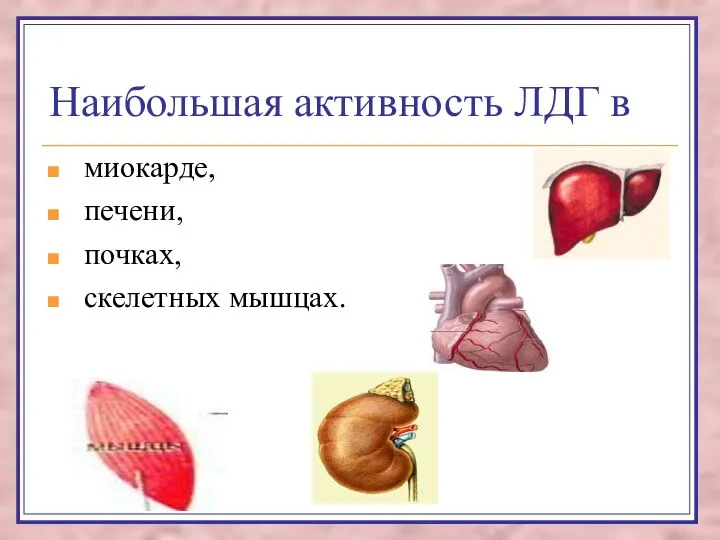
- 55. Наибольшая активность ЛДГ в миокарде, печени, почках, скелетных мышцах.
- 56. Изоферменты ЛДГ – органоспецифические ферменты. В тканях, в которых преобладает аэробный распад глюкозы присутствуют ЛДГ1,ЛДГ2 (низкое
- 57. Показатели ЛДГ при патологии При инфаркте миокарда ЛДГ1= ЛДГ2 в сыворотке, либо даже превышает её. При
- 58. В норме активность ЛДГ 0,8 – 4,0 ммоль/ч*л.
- 59. Повышается ЛДГ при повреждении миокарда, лейкозах, заболеваниях почек, гемолитической анемии, гепатитах, мышечной дистрофии, тромбах лёгочной артерии,
- 60. Возможность повышения ЛДГ1 при тестикулярных опухолях следует учитывать при диагностике инфаркта миокарда. ЛДГ1 и ЛДГ2 начинают
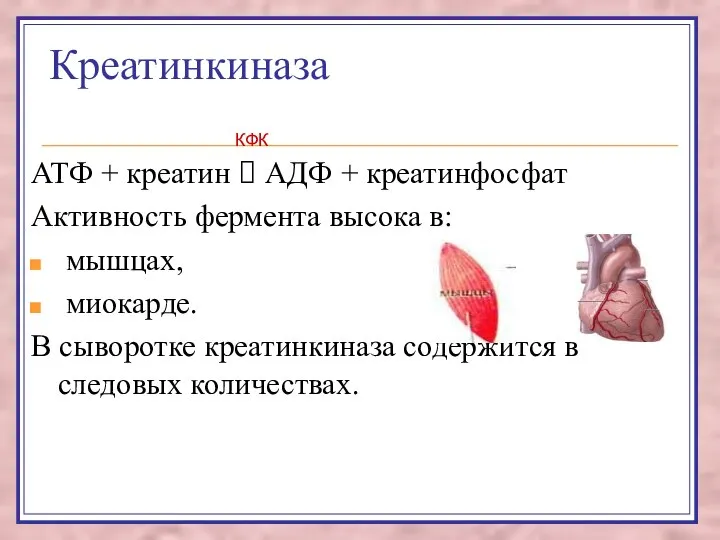
- 61. Креатинкиназа АТФ + креатин ⮀ АДФ + креатинфосфат Активность фермента высока в: мышцах, миокарде. В сыворотке
- 62. Изоферменты КФК ММ – в скелетных мышцах, МВ – в миокарде (+ММ), ВВ - в ткани
- 63. При инфаркте миокарда через 2-4 часа возрастает активность КФК, через 3 дня – нормализация. Обнаружение изофермента
- 64. При операциях аортокоронарного шунтирования повышаются КФК, миоглобин, тропонин.
- 65. ММ-КФК повышается при мышечной дистрофии, дерматомиозите.
- 66. ВВ-КФК повышается при гипоксии мозга, метастазах рака простаты.
- 67. КФК повышается при травмах, операциях, инфаркте миокарда, полимиозите, дерматомиозите, миокардите, мышечных дистрофиях, гипотермии, гипотиреозе, инфекциях, столбняке,
- 68. Причины повышения КФК в сыворотке крови Артефактные: - гемолиз эритроцитов in vitro, Физиологические: у новорожденных активность
- 69. Значительное повышение КФК при шоке и циркуляторной недостаточности, инфаркте миокарда, мышечной дистрофии.
- 70. Умеренное повышение КФК при механических повреждениях мышц, воспалении мышечной ткани, после хирургических вмешательств, физической перегрузке, после
- 71. КФК снижается при тиреотоксикозе, атрофии мышц.
- 72. АСТ наиболее активна в миокарде, печени, головном мозге, почках. Активность АСТ в миокарде в 10 000
- 73. АЛТ наиболее активна в печени, поджелудочной железе, сердце, скелетных мышцах.
- 74. При инфаркте миокарда в крови увеличивается АСТ. АСТ начинает нарастать через 6-8 часов после инфаркта миокарда.
- 75. При болезнях печени в крови увеличивается АЛТ. Особенно резко АЛТ повышается при инфекционном гепатите (за два
- 76. Коэффициент де Ритиса (1,33±0,4) АСТ/АЛТ снижается при инфекционном гепатите, повышается при инфаркте миокарда.
- 77. Причины повышения АСТ в сыворотке крови Артефактные: - гемолиз эритроцитов in vitro, - существенная задержка отделения
- 78. Значительное повышение АСТ при недостаточности кровообращения при шоке и гипоксии, инфаркте миокарда, остром вирусном и токсическом
- 79. Умеренное повышение АСТ при циррозе печени, механической желтухе, метастазах опухоли в печень, поражении скелетной мускулатуры, после
- 80. Активность АЛТ и АСТ повышается при использовании гепатотоксических препаратов анаболические стероиды, аспирин, индометацин.
- 81. Значение определения активности АСТ и АЛТ Повышение активности АСТ в сыворотке крови предложено использовать как прогностический
- 82. γ-Глутамилтранспептидаза (γ-ГТП) катализирует перенос γ-глутамильного остатка с γ-глутамилпептидов на аминокислоты с образованием новых γ-глутамилпептидов. Активность в
- 83. Активность γ-ГТП в органах в почках - 100%, в поджелудочной железе – 68%, в печени –
- 84. Фермент обнаруживается в сыворотке крови, моче, желчи. γ-ГТП сыворотки крови печёночного происхождения.
- 85. Резко повышается γ-ГТП в 10 раз при алкогольном поражении печени, холестазе, раке поджелудочной железы с обструкцией
- 86. Умеренно повышается γ-ГТП в 5-10 раз при гепатитах, циррозе (без холестаза), панкреатите, алкогольной интоксикации, опухоли поджелудочной
- 87. Превышение нормы γ-ГТП менее чем в 5 раз при алкоголизме, ятрогенных отравлениях (антиконвульсанты, фенобарбитал), застойной сердечной
- 88. Диагностическое значение При отсутствии желтухи определение γ-ГТП – чувствительный тест для выявления патологии печени. При онкозаболеваниях
- 89. γ-ГТП – фермент «репарации» Активность фермента возрастает в конце третьей недели с начала инфаркта миокарда, что
- 90. Альдолаза Концентрация в норме в сыворотке крови: 0,09-0,57ммоль/час*л. Повышается при: остром и хроническом гепатитах, травме мышц,
- 91. α-Амилаза расщепляет крахмал и гликоген до мальтозы, в плазму поступает из поджелудочной железы и слюнных желёз,
- 92. α-Амилаза содержится в панкреатическом соке, слюне, печени, мышцах, фаллопиевых трубах.
- 93. Значительное повышение α-амилазы в 10 раз при остром панкреатите, тяжёлой дисфункции почечных клубочков, тяжёлом диабетическом кетоацидозе.
- 94. При остром панкреатите α-Амилаза повышается через 3-12 часов после появления болей, достигает максимума через 20-30 часов,
- 95. Умеренное повышение α-амилазы в 5 раз при острых абдоминальных заболеваниях, заболеваниях слюнных желёз, дисфункции почечных клубочков,
- 96. Снижение α-амилазы в сыворотке и моче при некрозе поджелудочной железы, тиреотоксикозе, ожоговой болезни, позднем токсикозе, отравлениях
- 97. Диагностика панкреатита Наиболее чувствительным и специфичным тестом для диагностики панкреатита служит уровень активности Р-изофермента α-амилазы.
- 98. Причины гиперамилаземии и гиперамилазурии Патология поджелудочной железы (повышается Р-изоамилаза). Панкреатит: острый, хронический. Осложнения: ложная киста, асцит,
- 99. Патология, несвязанная с поджелудочной железой почечная недостаточность (повышается Р- и S-изоамилаза), гиперамилаземия при раке слюнных желёз
- 100. Заболевания брюшной полости комплексные патология билиарного тракта, перфорация пептической язвы (повышается Р-изоамилаза), непроходимость кишечника (повышается Р-изоамилаза),
- 101. Экскреторные ферменты синтезируются в печени (ЛАП, ЩФ) и поджелудочной железе (амилаза, липаза, трипсин), в норме выделяются
- 102. оптимум рН 8,6-10,1, гидролизует разные субстраты при рН 10, цинк и магний повышают активность фермента, присутствует
- 103. Изоферменты ЩФ костный, плацентарный, кишечный. Изофермент 1 содержится в костях, Изоферменты 2 и 3 содержатся в
- 104. Диагностическое значение определения ЩФ Определение активности ЩФ в крови имеет диагностическое значение при заболеваниях печени и
- 105. Активность ЩФ возрастает при рахите, остеомаляции, остеопорозах, остеосаркомах, туберкулёзе костей, механической желтухе, циррозе печени, инфаркте миокарда,
- 106. Причины гиперферментемии ЩФ при холестазе повышенный синтез фермента, экстракция фермента с плазматической мембраны, поступление в циркуляцию
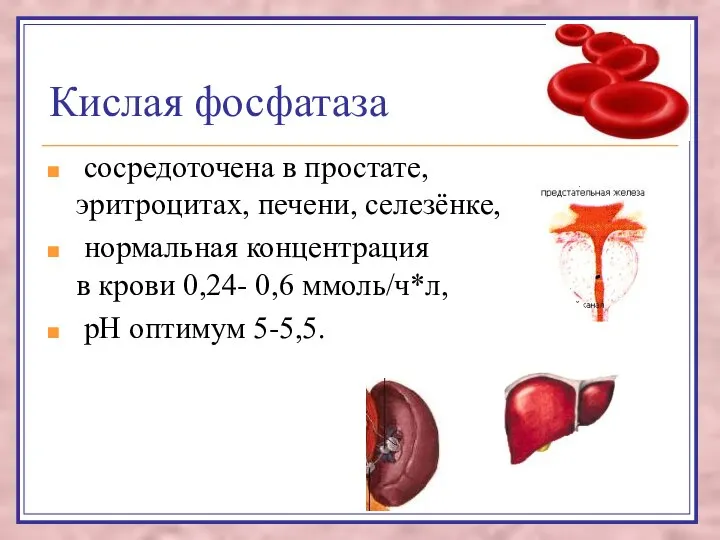
- 107. Кислая фосфатаза сосредоточена в простате, эритроцитах, печени, селезёнке, нормальная концентрация в крови 0,24- 0,6 ммоль/ч*л, рН
- 108. Кислая фосфатаза повышается при гемолитических анемиях, тромбоцитопении, тромбозах, миеломной болезни, раке простаты.
- 109. Значение определения КФ при раке простаты в 25% при раке простаты без метастазов повышается КФ, в
- 110. Г-6-ФДГ повышается при инфекционном гепатите, диабетическом кетоацидозе, отравлениях. Дефицит Г-6-ФДГ приводит к гемолитической анемии.
- 111. Холинэстераза расщепляет ацетилхолин на холин и уксусную кислоту.
- 112. Формы холинэстеразы: 1. холинэстераза в эритроцитах, нервной ткани, мозге, мышцах, 2. в плазме крови – псевдохолинэстераза,
- 113. Холинэстераза повышается в плазме при выздоровлении после поражений печени, нефрозе, гиперлипопротеинемии IV типа, столбняке, сахарном диабете.
- 114. Холинэстераза понижается в плазме при заболеваниях паренхимы печени, действии антихолинэстераз (ФОС), наследственных аномалиях холинэстеразы, инфаркте миокарда,
- 115. Диагностическое значение определения изоферментов холинэстеразы Исследование изоферментов холинэстеразы в сыворотке крови лиц, имеющих контакт с ФОС,
- 116. Липаза повышается в сыворотке при панкреатите, желчнокаменной болезни, перфорации полого органа, инфаркте кишки, кисте или псевдокисте
- 117. Фосфолипазы А и С Активность фосфолипаз А и С – критерий активности воспалительных и деструктивных изменений
- 118. Увеличение активности протеиназ в сыворотке крови сопутствует ревматизму, коллагенозам, острым воспалениям, инфекциям, ожоговой болезни, радиационным поражениям.
- 119. Трипсин повышается при остром панкреатите, язвенной болезни.
- 120. Трипсин снижается при эмфиземе лёгких, циррозе печени. цирроз
- 121. циррозе печени, хронических инфекционных заболеваниях, шизофрении, после инфаркта миокарда. Уровень церулоплазмина повышается при цирроз
- 122. Уровень церулоплазмина снижается при нефротическом синдроме, гепатоцеребральной дистрофии.
- 123. Основные ферменты печени, используемые в диагностике
- 124. Соотношение ферментов печени
- 125. Соотношение АСТ+АЛТ/ГлДГ Метастазы в печень 10 Обструктивная желтуха Билиарный цирроз 5-20 Острое начало: А. хронический гепатит
- 126. Соотношение γ-ГТ /АСТ Активный вирусный гепатит Токсический гепатит Хронический персистирующий гепатит ≤ 1 Хронический гепатит Острый
- 127. При остром вирусном гепатите Повышается в сыворотке крови активность: АЛТ, АСТ, ЛАП, γ-ГТП, аденозиндезаминазы. Коэффициент де
- 128. При некрозе гепатоцитов в крови Повышается активность: АСТ, ГЛДГ, IgM, IgG, Снижаются: альбумины, протромбин, проконвертин, антигемофильный
- 129. Энзимы в пище салат из моркови, орехов, лука порея, сельдерея, к тяжело усвояемому мясу для улучшения
- 130. Использование ферментов для лечения болезней
- 131. Заместительная терапия при дефицитах, недостатке ферментов пепсин, фестал, панзинорм.
- 132. Патогенетическая терапия Трипсин применяется для обработки гнойных ран, разжижения и удаления вязких секретов. Гиалуронидаза представлена двумя
- 133. Лечение тромбозов ферментами ПССК фибринолизином, стрептокиназой, урокиназой. Эндоваскулярная терапия тромбином способствует эмболизации сосудов при кровотечениях, лечению
- 134. Ингибиторы протеолитических ферментов: контрикал, гордокс, трансилол, ингитрил
- 135. Ингибиторы протеолитических ферментов применяются при панкреатитах, активации фибринолиза, инфаркте миокарда, артритах, аллергических заболеваниях.
- 136. Лечение острого панкреатита В лечении острого панкреатита применяется селективная сорбция протеиназ. Созданный на основе овомукоида из
- 137. Ингибитор МАО - ниаламид представляет одну из основных групп антидепрессантов. Ингибиторангиотензин-конвертирующего фермента в составе катиотена применяется
- 138. Применение микроконтейнеров (ферменты в липосоме) Разработки по увеличению степени тропности липосом введение в их оболочку антител,
- 139. Условия успешной энзимотерапии получение фермента в чистом виде, введение фермента, чтобы он достиг органа-мишени.
- 140. Иммобилизация ферментов Ковалентная иммобилизация ферментов – фермент ковалентно присоединён к полимерному носителю. Нековалентная иммобилизация ферментов –
- 141. Преимущества устойчивость к протеолитическим ферментам, термостабильность, длительное действие, снижение антигенности.
- 142. Примеры применения иммобилизации ферментов тампоны и бинты с иммобилизованными на них протеазами для ускорения заживления ран
- 143. Использование ферментов в качестве аналитических реактивов
- 145. Скачать презентацию





































































































































 Художники - передвижники
Художники - передвижники Коммуникация с подписчиком. А почему он не ответил. Тренинг
Коммуникация с подписчиком. А почему он не ответил. Тренинг Колобок
Колобок  Сетевые образовательные ресурсы как фактор повышения качества урока МОУ «Гимназия № 2» Волик Л.М., заместитель директора по У
Сетевые образовательные ресурсы как фактор повышения качества урока МОУ «Гимназия № 2» Волик Л.М., заместитель директора по У Презентация Место России на мировом рынке вооружения
Презентация Место России на мировом рынке вооружения Уильям Шекспир
Уильям Шекспир Институты демократии в РФ. (Тема 4)
Институты демократии в РФ. (Тема 4) Шесть библейских принципов
Шесть библейских принципов Victory chant
Victory chant Обычаи осетинского народа
Обычаи осетинского народа Реализация предпрофильной подготовки в условиях перехода к профильному обучению в образовательном учреждении.
Реализация предпрофильной подготовки в условиях перехода к профильному обучению в образовательном учреждении. слюнные железы, поджелудочная
слюнные железы, поджелудочная Амвросиев Николаевский Дудин монастырь
Амвросиев Николаевский Дудин монастырь Введение в веб-технологии
Введение в веб-технологии ФинЭк Анализ Профессиональная система финансового анализа 12 лет успешной работы!
ФинЭк Анализ Профессиональная система финансового анализа 12 лет успешной работы! Путешествие на остров - презентация для начальной школы_
Путешествие на остров - презентация для начальной школы_ Структура процесса обучения в центре профессионального развития в индустрии спорта и фитнеса
Структура процесса обучения в центре профессионального развития в индустрии спорта и фитнеса Политические лидеры
Политические лидеры Обслуживание и ремонт кривошипно-шатунного механизма
Обслуживание и ремонт кривошипно-шатунного механизма Презентация Немецкая классическая философия
Презентация Немецкая классическая философия Эффективность использования минеральных ресурсов
Эффективность использования минеральных ресурсов Современные образовательные технологии Технологии разноуровневого, дифференцированного обучения
Современные образовательные технологии Технологии разноуровневого, дифференцированного обучения Выполнила: Выполнила: Преподаватель спецдисциплин И.В.Морозова
Выполнила: Выполнила: Преподаватель спецдисциплин И.В.Морозова Сенсоры. Классификация сенсоров. Терморезистивные, термоэлектрические, термомеханические, пироэлектрические преобразователи
Сенсоры. Классификация сенсоров. Терморезистивные, термоэлектрические, термомеханические, пироэлектрические преобразователи Цикличность экономического развития. Причины цикличности в экономике.
Цикличность экономического развития. Причины цикличности в экономике. Управление командой проекта
Управление командой проекта Data Collection of Primary Central Nervous System (CNS) Tumors
Data Collection of Primary Central Nervous System (CNS) Tumors Презентация на тему "Сепсис" - скачать презентации по Медицине
Презентация на тему "Сепсис" - скачать презентации по Медицине