Содержание
- 2. СТРУКТУРА БЕЛКА Пептидные цепи содержат а/к остатки, соединены пептидными связями. (прочные, разрыв - фермент) Белок имеет
- 4. Первичная структура белка линейная последовательность а/к в полипептидной цепи первичная структура каждого белка закодирована в одном
- 5. Вторичная структура белка Линейные цепи а\к приобретают пространственную трёхмерную структуру -"конформацию". образуется за счёт взаимодействия функциональных
- 6. Вторичная структура белка регулярные структуры двух типов: α-спираль и β-структура.
- 7. α-Спираль пептид закручивается в виде спирали водородных связи образуются между атомами кислорода карбонильных групп и атомами
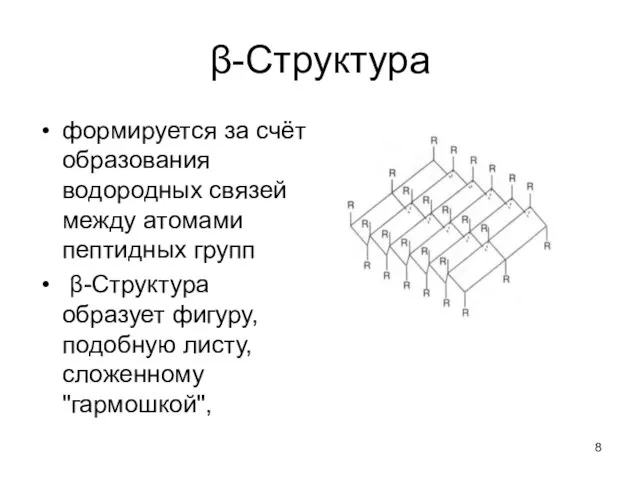
- 8. β-Структура формируется за счёт образования водородных связей между атомами пептидных групп β-Структура образует фигуру, подобную листу,
- 10. Третичная структура белков трёхмерная пространственная структура образуетсяза счёт взаимодействий между радикалами аминокислот, стоящих на значительном расстоянии
- 11. Гидрофобные взаимодействия гидрофобные радикалы аминокислот стремятся к объединению внутри белковой глобулы формируется гидрофобное ядро гидрофильные радикалы
- 12. Ионные связи могут возникать между отрицательно заряженными (анионными) карбоксильными группами радикалов асп и глу кислот и
- 13. Ковалентные связи Третичную структуру некоторых белков стабилизируют дисульфидные связи, образующиеся за счёт взаимодействия SH-групп двух остатков
- 14. Денатурация белков Гидрофобные взаимодействия, а также ионные и водородные связи относят к числу слабых Разрыв большого
- 15. Доменная структура белков Если полипептидная цепь белка содержит более 200 аминокислот, как правило, её пространственная структура
- 16. Четвертичная структура белков существуют белки, состоящие из двух и более полипептидных цепей после формирования трёхмерной структуры
- 18. Физико-химические свойства белков Индивидуальные белки различаются по своим физико-химическим свойствам: форме молекул, молекулярной массе, суммарному заряду
- 19. Различия белков по форме молекул форме молекул белки делят на глобулярные и фибриллярные. Глобулярные белки имеют
- 20. Различия белков по молекулярной массе Белки - высокомолекулярные соединения, но могут сильно отличаться по молекулярной массе,
- 21. Суммарный заряд белков Белки имеют в своём составе радикалы лизина, аргинина, гистидина, глутаминовой и аспарагиновой кислот,
- 22. Соотношение полярных и неполярных групп на поверхности нативных молекул белков На поверхности большинства внутриклеточных белков преобладают
- 23. Растворимость белков Растворимость белков в воде зависит от всех перечисленных выше свойств белков: формы, молекулярной массы,
- 24. Методы выделения и очистки белков Получение индивидуальных белков из биологического материала (тканей, органов, клеточных культур) требует
- 25. Методы разрушения тканей и экстракции белков Для разрушения биологического материала используют методы: гомогенизации ткани, метод попеременного
- 26. Экстракция белков, связанных с мембранами, и разрушение олигомерных белков на протомеры Если искомый белок прочно связан
- 27. Удаление из раствора небелковых веществ Нуклеиновые кислоты, липиды и другие небелковые вещества можно удалить из раствора,
- 28. Гель-фильтрация, или метод молекулярных сит Для разделения белков часто используют хроматографические методы, основанные на распределении веществ
- 29. Неподвижная фаза - жидкость внутри гранул, в которую способны проникать низкомолекулярные вещества и белки с небольшой
- 30. Ультрацентрифугирование Метод разделения также основан на различии в молекулярных массах белков. Скорость седиментации веществ в процессе
- 31. Электрофорез белков Метод основан на том, что при определённом значении рН и ионной силы раствора белки
- 32. Каталитическая функция Ферменты (энзимы) – белки - увеличивают скорость протекания химической реакции, при этом не расходуются
- 33. Фермент-субстратные реакции В участке связывания субстрат связывается с ферментом - фермент-субстратный комплекс. В каталитическом участке субстрат
- 34. Катализ Схематично процесс катализа можно представить следующим уравнением: Е + S ↔ ES ↔ ЕР ↔
- 38. Специфичность наиболее важное свойство ферментов. субстратная сп.- способность фермента взаимодействовать лишь с одним или несколькими определёнными
- 39. Специфичность Выделяют абсолютную субстратную специфичность (катализ 1 субстрата) - аргиназа; групповую субстратную специфичность однотипные реакции с
- 40. Каталитическая специфичность Фермент превращает субстрат по одному из возможных путей его превращения Зависит от строения каталитического
- 42. Номенклатура и классификация ферментов В настоящее время известно более 2400 ферментов. Каждый фермент, как правило, имеет
- 43. Вещество, имеющее это окончание, принимают за фермент. Ферменты, действующие на крахмал (amylum), сахарозу, мочевину (urea), пептиды
- 44. ферменты, катализирующие процессы гидролиза называют гидролазами, процессы окисления - оксидазами, перенос групп - трнсферазами и т.д.
- 45. Классы ферментов Оксидоредуктазы, катализирующие окисление или восстановление - алкогольдегидрогеназа Дегидрогеназы. В этот подкласс входят ферменты, катализирующие
- 47. Оксидазы. Акцептором электрона служит молекулярный кислород. Пример реакции, катализируемой цитохромоксидазой
- 48. Оксигеназы (гидроксилазы) - атом кислорода из молекулы кислорода присоединяется к субстрату. Пример реакции:
- 50. 2.Трансферазы, катализирующие перенос химических групп с одной молекулы субстрата на другую. Среди трансфераз выделяют киназы, переносящие
- 51. 3. Гидролазы катализирующие гидролиз химических связей. Пример: пепсин, трипсин, амилаза
- 52. Классы ферментов Лиазы, катализирующие разрыв химических связей без гидролиза с образованием двойной связи в одном из
- 53. КОФАКТОРЫ И КОФЕРМЕНТЫ Большинство ферментов для активности нуждается в: низкомолекулярных органических соединениях небелковой природы (коферментах) и/или
- 54. Регуляция работы ферментов Активность ферментов зависит от количества: молекул субстрата продукта наличия кофакторов и коферментов. Каскад
- 55. Среди множества ферментов практически каждого метаболического пути различают ключевые, или регуляторные, ферменты, активность которых может изменяться
- 56. Основные способы регуляции активности ферментов Аллостерическая регуляция. Фермент изменяет активность с помощью нековалентно связанного с ним
- 57. Регуляция активности ферментов путем фосфорилирования—дефосфорилирования . Фермент изменяет активность в результате ковалентной модификации.
- 59. Активация ферментов путем частичного протеолиза. Некоторые ферменты синтезируются первоначально неактивными и лишь после секреции из клетки
- 60. Ингибиторы ферментов Действие ферментов можно полностью или частично подавить (ингибировать) химическими веществами (ингибиторами). По характеру действия
- 61. Взаимодействие аспирина с ферментом простагландинсинтетазой
- 63. Скачать презентацию



























































 Презентация на тему "Постэмбриональный период развития" - скачать презентации по Биологии
Презентация на тему "Постэмбриональный период развития" - скачать презентации по Биологии Передвижение воды и питательных веществ в растении
Передвижение воды и питательных веществ в растении Каракал
Каракал Представление о нервной системе. Её отделы и функции
Представление о нервной системе. Её отделы и функции Онтогенез - индивидуальное развитие организма
Онтогенез - индивидуальное развитие организма Красная книга самарской области
Красная книга самарской области Борьба за существование Формы борьбы за существование
Борьба за существование Формы борьбы за существование  Биофизика дыхания. Объемы и емкости легких
Биофизика дыхания. Объемы и емкости легких Вывод продуктов обмена
Вывод продуктов обмена Исследование влияния бактерий фирмы Biolatic на жизнедеятельность сельскохозяйственных животных
Исследование влияния бактерий фирмы Biolatic на жизнедеятельность сельскохозяйственных животных Презентация на тему "Многообразие Простейших" - скачать презентации по Биологии
Презентация на тему "Многообразие Простейших" - скачать презентации по Биологии День Птиц. Синица
День Птиц. Синица Проект Красная книга
Проект Красная книга Комнатные цветы
Комнатные цветы Развитие эмоционально-волевой сферы подростков
Развитие эмоционально-волевой сферы подростков Жизнь – особое природное явление
Жизнь – особое природное явление Спор овощей
Спор овощей Качественные реакции на белки
Качественные реакции на белки Введение в микробиологию
Введение в микробиологию Достижения селекции
Достижения селекции Зоологический музей
Зоологический музей Микроорганизмы -
Микроорганизмы - Голосеменные растения
Голосеменные растения Презентация для класса Паразитические грибы и бактерии
Презентация для класса Паразитические грибы и бактерии  Хворостухина Олеся МОУ «Лицей №10», г. Пермь
Хворостухина Олеся МОУ «Лицей №10», г. Пермь Медиаторы и рецепторы в нервной системе
Медиаторы и рецепторы в нервной системе Цветок для моей мамы!!! Учитель начальных классов Чепурная Е.И. МКОУ СОШ № 8 Ставропольский край с. Тахта
Цветок для моей мамы!!! Учитель начальных классов Чепурная Е.И. МКОУ СОШ № 8 Ставропольский край с. Тахта  Путешествие по островам "Роботоландии"
Путешествие по островам "Роботоландии"