Содержание
- 2. Механизмы инактивации ферментов 1. Изменение первичной структуры: 1.1. Разрыв полипептидной цепи: Жесткие условия (длительное кипячение в
- 3. Решение: В литературе практически отсутствуют примеры удачной реактивации подобным образом инактивированных ферментов.
- 4. 1.2.Окисление функциональных групп фермента SH-группы цистеина и индольные фрагменты триптофана, при повышенной температуре, могут окисляться (сульфокси-
- 5. Решение: Реактивировать с помощью восстанавливающих агентов, в частности низкомолекулярных тиолов (например, цистеин или дитиотрейтол) .
- 6. 1.3. Расщепление дисульфидных связей Вызывают : Тиолы и другие восстановленные соединений серы, например Na2SO3, Na2S2O3. Продуктом
- 7. 1.3. Расщепление дисульфидных связей Щелочной гидролиз цистеина →дегидроаланин→ Благодаря нуклеофильным свойствам взаимодействует с NH2-группами лизина и
- 8. Решение: Добавление в среду тиолов приведет к расщеплению смешанного дисульфида и последующему образованию правильной S–S связи
- 9. 1.4. Химическая модификация каталитических SH-групп. Катионы тяжелых металлов (Hg, Pb и Cu) связываются с SH-групп активного
- 10. 1.5. Фосфорилирование белков in vivo. Под действием фосфорилазы и фосфатазы, содержащихся в полуочищенных ферментативных препаратах в
- 11. Решение: В литературе практически отсутствуют примеры удачной реактивации подобным образом инактивированных ферментов.
- 12. 1.6. Дезаминирование остатков аспарагина. При температурах (порядка 100 °С) и рН (порядка 4,0–5,0) происходит дезаминирование остатков
- 13. Решение: В литературе практически отсутствуют примеры удачной реактивации подобным образом инактивированных ферментов.
- 14. 1.7. Радиационная инактивация ферментов γ-облучение и УФ-свет Воздействуют на функциональные группы ферментов, пептидные связи и SH-группы
- 15. 2. Агрегация Наблюдается при повышенной температуре, при экстремальных значениях рН, в присутствии некоторых химических соединений. Чем
- 16. Решение: Необходимо разрушить межмолекулярные ковалентные и нековалентные контакты c помощью концентрированных растворов мочевины и гуанидинхлорида, экстремальных
- 17. 3. Инактивация ферментов поверхностным натяжением Поверхностное натяжение на границе раздела между воздухом и чистой водой составляет
- 18. Решение: Добавление ПАВ снижает поверхностное натяжение до 1 дин/см.
- 19. 4. Сорбция белка на стенках реакционного сосуда Сорбция за счет нековалентных взаимодействий приводит к уменьшению концентрации
- 20. Решение: Десорбция фермента со стенок реакционного сосуда достигается за счет разрушения неспецифических взаимодействий между белком и
- 21. 5. Диссоциация олигомерных белков на субъединицы Вызывают: Мочевина, детергенты, кислоты или же нагревание. Приводят к: конформационным
- 22. 6. Десорбция кофактора из активного центра фермента Вызывает: нагревание, действие хелаторов, диализ Если диссоциация кофактора сопровождается
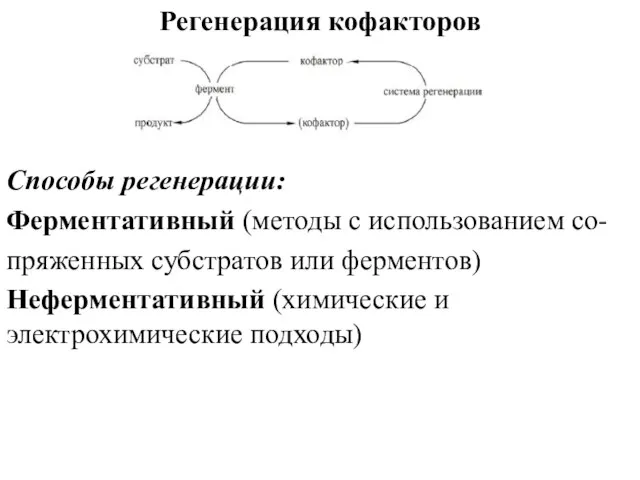
- 23. Регенерация кофакторов Способы регенерации: Ферментативный (методы с использованием со- пряженных субстратов или ферментов) Неферментативный (химические и
- 24. Ферментативный способ Использование сопряженных субстратов. В систему вводят избыточное количество сопряженного субстрата того же фермента: Пример:
- 25. Ферментативный способ Использование сопряженных субстратов. Недостатка: • используются высокие концентрации сопряженного субстрата, так как равновесие реакции
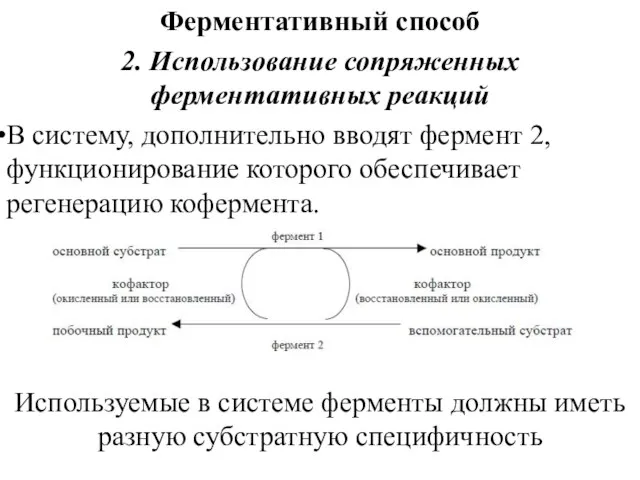
- 26. Ферментативный способ 2. Использование сопряженных ферментативных реакций В систему, дополнительно вводят фермент 2, функционирование которого обеспечивает
- 27. Неферментативные способы Химические методы. Используются дитионит натрия и некоторые соли пиридиния: + Низкая стоимость. могут ингибировать
- 28. Неферментативные способы 2. Электрохимические методы. Прямое электрохимическое восстановление или окисление. “-” появления в процессе регенерации ферментативно
- 29. СТАБИЛИЗАЦИЯ ФЕРМЕНТОВ В БИОТЕХНОЛОГИЧЕСКИХ СИСТЕМАХ
- 30. Проблемы возникающие при использовании ферментов в биотехнологических процессах: Повышенные температуры Экстремальные значения pH Высокие концентрации органических
- 31. Основные подходы для стабилизации ферментов : Добавление стабилизирующих веществ в среду, в которой хранится фермент или
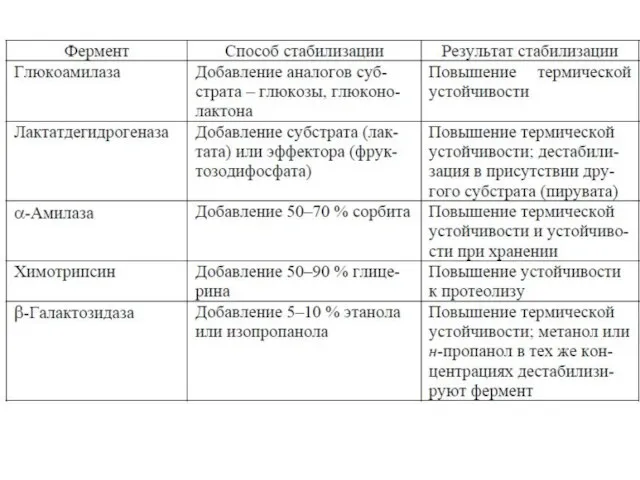
- 32. Стабилизация ферментов с помощью: Субстратов или их аналогов: Фермент-субстратный комплекс часто более устойчив, чем свободный фермент.
- 33. Стабилизация ферментов с помощью: 2. Органических растворителей: Многоатомные спирты стабилизируют некоторые ферменты за счет повышения устойчивости
- 34. Стабилизация ферментов с помощью: 3. Солей: При низких концентрациях солей ( Са2+ способен стабилизировать третичную структуру
- 36. Химическая модификация фермента 1. Фермент принимает более стабильную конформацию. 2. Введение в белок новых функциональных групп
- 37. Иммобилизация фермента позволяет: Повысить устойчивость фермента (нагреванию, автолизу, действию агрессивных сред и т. д) Многократно использовать
- 38. Иммобилизованные ферменты – это препараты ферментов, молекулы которых связаны с носителем, сохраняя при этом полностью или
- 39. Методы иммобилизации: В качестве носителей могут применяться: 1)Органические материалы: 1.1) природные (полисахариды, белки, липиды) 1.2) синтетические
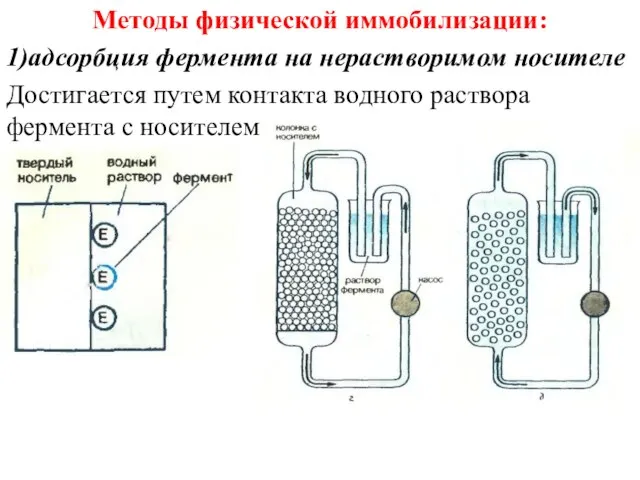
- 40. Методы физической иммобилизации: 1) адсорбция фермента на нерастворимом носителе в результате электростатических, гидрофобных, вандер-ваальсовых и др.
- 41. Методы физической иммобилизации: 1)адсорбция фермента на нерастворимом носителе Достигается путем контакта водного раствора фермента с носителем.
- 42. Методы физической иммобилизации: 1)адсорбция фермента на нерастворимом носителе Факторы влияющие на адсорбцию: Удельная поверхность и пористость
- 43. Методы физической иммобилизации: 1)адсорбция фермента на нерастворимом носителе Преимущества: Относительная простота методики Доступность носителей Недостатки: Недостаточная
- 44. Методы физической иммобилизации: 2) включение фермента в полупроницаемую капсулу, в полупроницаемую мембрану
- 45. Методы физической иммобилизации: 2) включение фермента в полупроницаемую капсулу, в полупроницаемую мембрану Преимущества: Относительная простота методики
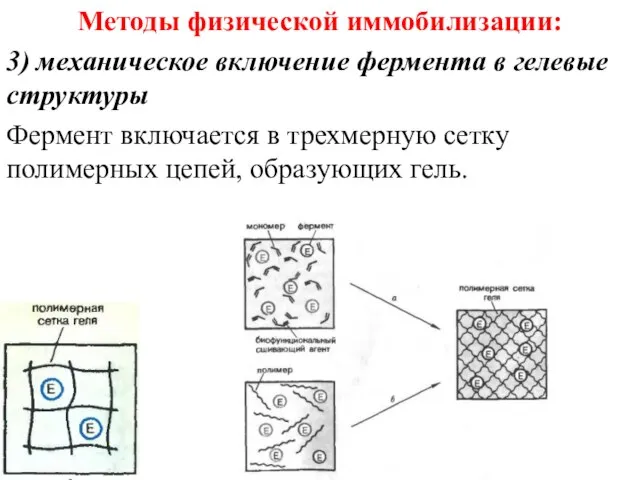
- 46. Методы физической иммобилизации: 3) механическое включение фермента в гелевые структуры Фермент включается в трехмерную сетку полимерных
- 47. Методы физической иммобилизации: 3) механическое включение фермента в гелевые структуры Необходимо учитывать: Соответствие размера пор размеру
- 48. Методы физической иммобилизации: 3) механическое включение фермента в гелевые структуры Преимущества: Относительная простота методики Повышенная механическая,
- 49. Методы физической иммобилизации: 4) Включение в двухфазную систему Фермент растворим только в одной из фаз, а
- 50. Методы химической иммобилизации: Образовании ковалентных связей между ферментом и носителем. Преимущества: 1) Высокая прочность конъюгата 2)
- 51. При иммобилизации ферментов необходимо соблюдать следующие условия: 1. Активные группы матрицы не должны блокировать каталитический центр
- 52. Весьма перспективным является использование в качестве биокатализаторов иммобилизованных клеток. Т.к. можно избежать: дорогостоящие стадии выделения и
- 53. Термозимы Стабильны в условиях высокой температуры, высоких концентраций солей и экстремальных значений рН. Гипертермофильные микроорганизмы, встречающиеся
- 54. Механизмы ответственны за термоустойчивость ферментов у термозимов: Между мезофильными и термофильными версиями ферментов - высокая степень
- 55. Было обнаружено, что дегидрогеназа из Pyrococcus furiosus (Tm == 105 °C) содержит 35 изолейцинов, в то
- 56. Возросшая термостабильность коррелирует: с увеличением жесткости белковой структуры за счет уменьшения содержания остатков глицина, с улучшением
- 57. Механизмы стабилизации: • минимизация доступной площади гидрофобной поверхности белка; • оптимизация упаковки атомов белковой молекулы (минимизация
- 58. Применение ферментов из экстремофилов Современные технологии молекулярной биологии и генной инженерии позволяет: 1) получать достаточные количества
- 59. Применение ферментов из экстремофилов: Крахмал используется для производства сахаров. Сначала процесс ведется при (95–105 °С) и
- 60. Применение ферментов из экстремофилов: Наиболее термостабильные α-амилазы были обнаружены у archaea Pyrococcus woesei, Pyrococcus furiosus, Desulfurococcus
- 61. Применение ферментов из экстремофилов: Протеолитические ферменты Сериновые щелочные протеиназы широко используются в качестве добавок к моющим
- 62. Применение ферментов из экстремофилов: ДНК-полимеразы Термостабильные ДНК-полимеразы используются в ПЦР и играют важную роль в генной
- 64. Скачать презентацию
























































 Презентация на тему "Химический состав клетки" - скачать презентации по Биологии
Презентация на тему "Химический состав клетки" - скачать презентации по Биологии Презентация на тему Ботаника наука о растениях
Презентация на тему Ботаника наука о растениях  Организм человека
Организм человека Аттестационная работа. Проект Птицы - наши друзья
Аттестационная работа. Проект Птицы - наши друзья Генетика в кошках. Курс занимательной молекулярной генетики. Лекция I
Генетика в кошках. Курс занимательной молекулярной генетики. Лекция I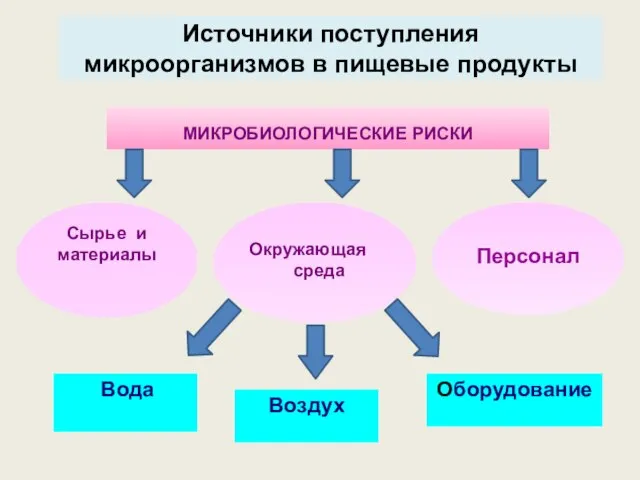 Микробиологическая безопасность продуктов
Микробиологическая безопасность продуктов Определение запаса лекарственного сырья
Определение запаса лекарственного сырья Особенности высшей нервной деятельности человека. Учение И.П. Павлова о сигнальных системах
Особенности высшей нервной деятельности человека. Учение И.П. Павлова о сигнальных системах Клеточное дыхание
Клеточное дыхание Древнеримский канон
Древнеримский канон Ботаника. Плод
Ботаника. Плод Images superbes et très émouvantes ..., un gamin qui sait parler aux marmottes
Images superbes et très émouvantes ..., un gamin qui sait parler aux marmottes Аттестационная работа. Определение кислотности почвы на пришкольном участке
Аттестационная работа. Определение кислотности почвы на пришкольном участке Для чего нужен скелет
Для чего нужен скелет Внимание 8 класс биология
Внимание 8 класс биология  Опорно-двигательная система человека
Опорно-двигательная система человека Размножение растений. Определение всхожести семян
Размножение растений. Определение всхожести семян Обмен веществ
Обмен веществ Сезонные изменения в природе. Осень. Программа Родные истоки
Сезонные изменения в природе. Осень. Программа Родные истоки Как устроен человек
Как устроен человек Перевалка комнатных растений
Перевалка комнатных растений Размножение организмов
Размножение организмов Василий Васильевич Капнист
Василий Васильевич Капнист Презентация на тему "Самые красивые птицы в мире" - скачать бесплатно презентации по Биологии
Презентация на тему "Самые красивые птицы в мире" - скачать бесплатно презентации по Биологии Изучение ценопопуляции вяза шершавого (Ulmus glabra Huds.) в долине реки Печегды
Изучение ценопопуляции вяза шершавого (Ulmus glabra Huds.) в долине реки Печегды Лекарственные растения содержащие эфирные масла
Лекарственные растения содержащие эфирные масла Слуховой анализатор
Слуховой анализатор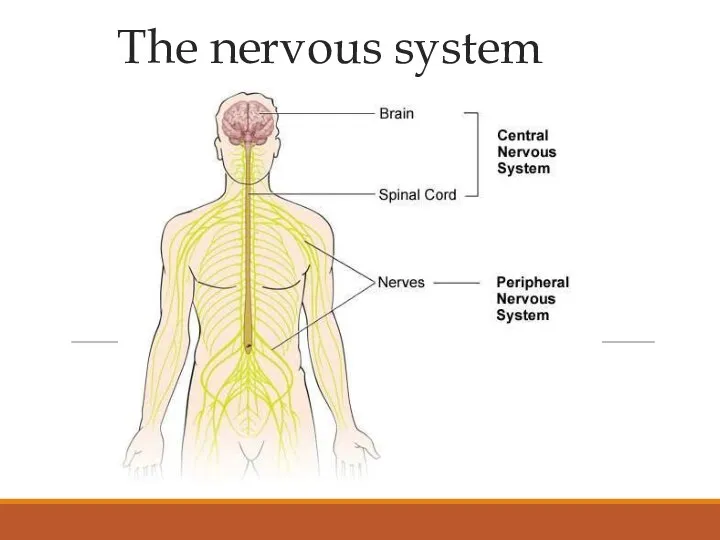 The Nervous System
The Nervous System