Содержание
- 2. Классификация патологии человека в зависимости от значимости генетических и средовых факторов Заболевания, связанные с изменением генетического
- 3. Классификация МФЗ Врожденные пороки развития – возникают внутриутробно в результате взаимодействия многочисленных генетических, неблагоприятных материнских факторов
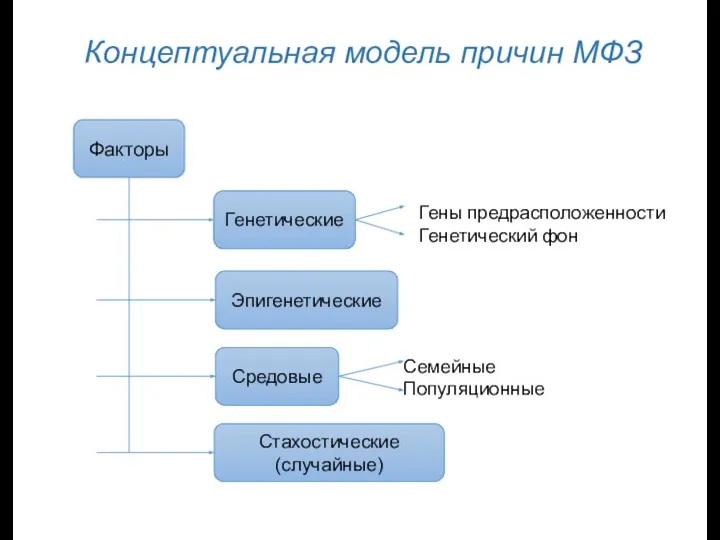
- 4. Концептуальная модель причин МФЗ Факторы Генетические Эпигенетические Средовые Стахостические (случайные) Гены предрасположенности Генетический фон Семейные Популяционные
- 5. Семейное накопление МФЗ Метод случай-контроль: сравнивают частоту, с которой болезнь обнаруживают в родословной больных, с таковой
- 6. Семейное накопление МФЗ
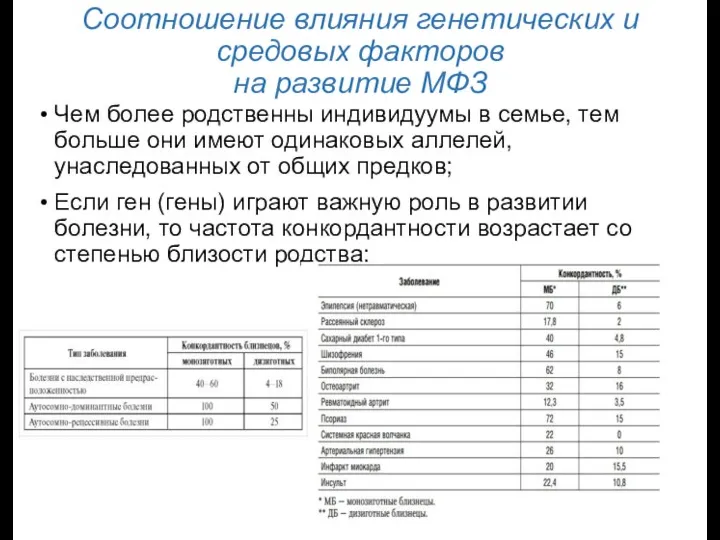
- 7. Соотношение влияния генетических и средовых факторов на развитие МФЗ Чем более родственны индивидуумы в семье, тем
- 8. Критерии МФЗ Различия популяционной и семейной частоты; Риск развития заболевания у ребенка зависит от состояния здоровья
- 9. Генетика количественных признаков МФЗ Корреляция (r) – степень сходства между родственниками по количественному признаку; Если корреляция
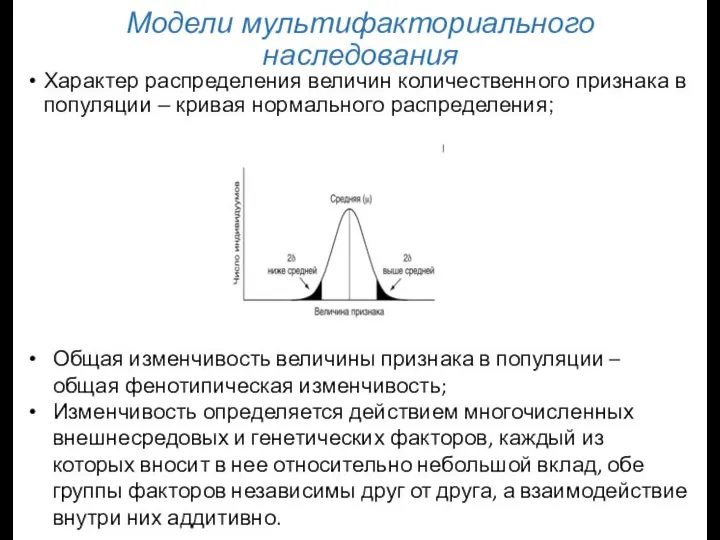
- 10. Модели мультифакториального наследования Характер распределения величин количественного признака в популяции – кривая нормального распределения; Общая изменчивость
- 11. Модели мультифакториального наследования Предрасположенность зависит от действия большого числа генов и факторов внешней среды; Для возникновения
- 12. Генетическая гетерогенность МФЗ Генетическая гетерогенность МФЗ – существование внутри клинического континуума болезни двух и более форм,
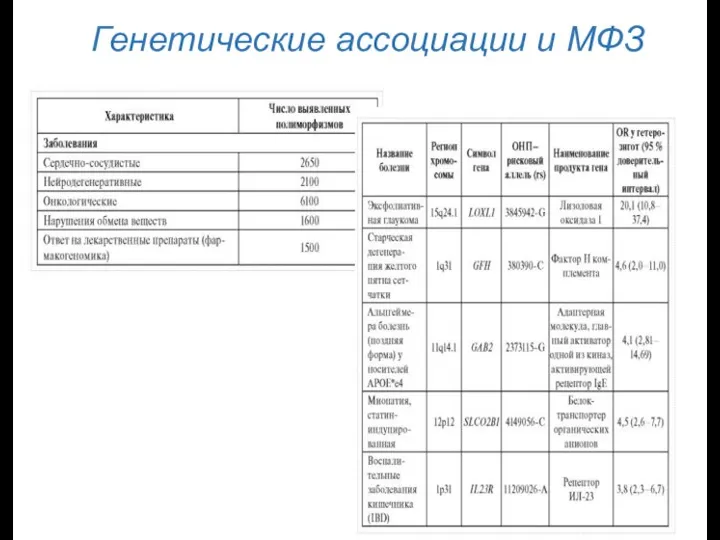
- 13. Генетические ассоциации и МФЗ OR – отношение шансов OR= 0 - ∞, OR = 1 –
- 14. Генетические ассоциации и МФЗ Особенности обнаруживаемых генетических ассоциаций: 1)Большая часть генетических ассоциаций вызывает эффекты небольшой величины
- 15. Генетические ассоциации и МФЗ
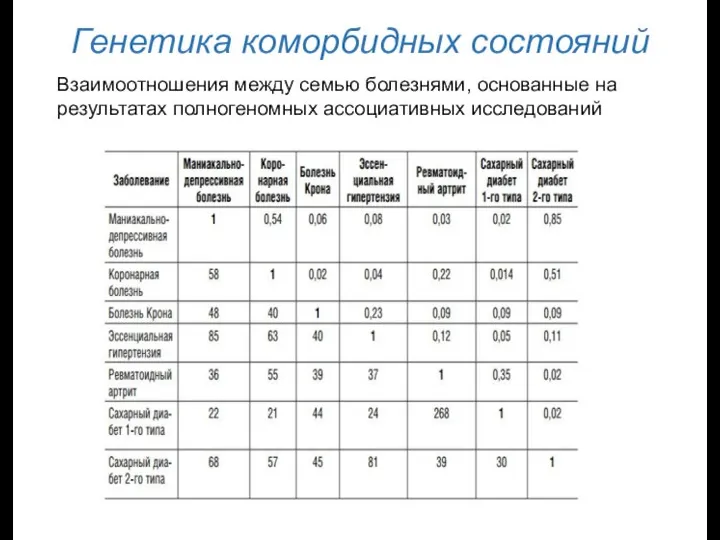
- 16. Генетика коморбидных состояний Полипатии – множественность болезней у одного пациента (коморбидность); Коморбидность составляет 17%, для метаболических
- 17. Генетика коморбидных состояний Взаимоотношения между семью болезнями, основанные на результатах полногеномных ассоциативных исследований
- 18. Идентификация генов предрасположенности к МФЗ Характеристика структуры генов и их многочисленных аллельных вариантов; Определение точной локализации
- 19. Идентификация генов предрасположенности к МФЗ Анализ сцепления - метод генетического картирования, основанный на прослеживании косегрегации генов
- 20. Идентификация генов предрасположенности к МФЗ Метод идентичных по происхождению аллелей (IBD – identical by descent) –
- 21. Гипотезы рисковых аллелей CD/CV (common disease/common variant — распространенная болезнь/распространенный вариант гена) —значительную часть аллелей подверженности
- 22. Идентификация генетических вариантов в соответствии с частотой рисковых аллелей и силой генетических эффектов Частота генетического варианта
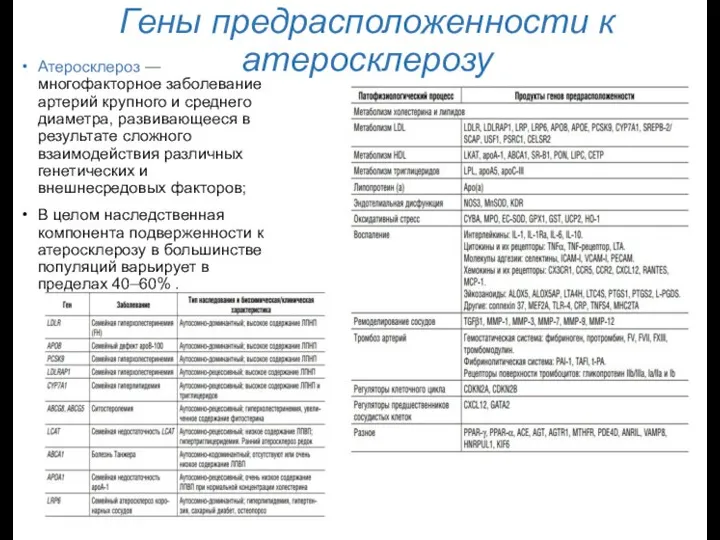
- 23. Гены предрасположенности к атеросклерозу Атеросклероз — многофакторное заболевание артерий крупного и среднего диаметра, развивающееся в результате
- 24. Гены предрасположенности к АГ
- 25. Изучение генетики МФЗ Понимание патогенетических путей развития заболевания Разработка генетических тестов, которые существенно улучшат качество медицинской
- 27. Скачать презентацию


















 Нейруляция и дифференцировка нейроэктодермы
Нейруляция и дифференцировка нейроэктодермы Эволюция растений
Эволюция растений Растения на территории нашей школы
Растения на территории нашей школы Тема урока: Конечный мозг. Структура и функции
Тема урока: Конечный мозг. Структура и функции Разведение голубей
Разведение голубей Лекарственные растения Владимирской области
Лекарственные растения Владимирской области Генетичні основи селекції організмів
Генетичні основи селекції організмів Отряд Аистообразные
Отряд Аистообразные Модификационная изменчивость
Модификационная изменчивость Экологические болезни человека.
Экологические болезни человека. Значение корней и их разнообразие
Значение корней и их разнообразие Биосинтез белка
Биосинтез белка Презентация на тему "Какие бывают жуки" - скачать бесплатно презентации по Биологии
Презентация на тему "Какие бывают жуки" - скачать бесплатно презентации по Биологии Плесневые грибы. Дрожжи
Плесневые грибы. Дрожжи Межклеточные сигнальные вещества
Межклеточные сигнальные вещества Биосфера және В.И. Вернадскийдің биосфера-ноосфералық концепциясы
Биосфера және В.И. Вернадскийдің биосфера-ноосфералық концепциясы Профессия кинолог
Профессия кинолог Генетичний контроль імунної відповіді
Генетичний контроль імунної відповіді Насекомые (морфология, анатомия, физиология)
Насекомые (морфология, анатомия, физиология) Введение в общую биологию. Особенности биологического познания
Введение в общую биологию. Особенности биологического познания Формы борьбы за существование
Формы борьбы за существование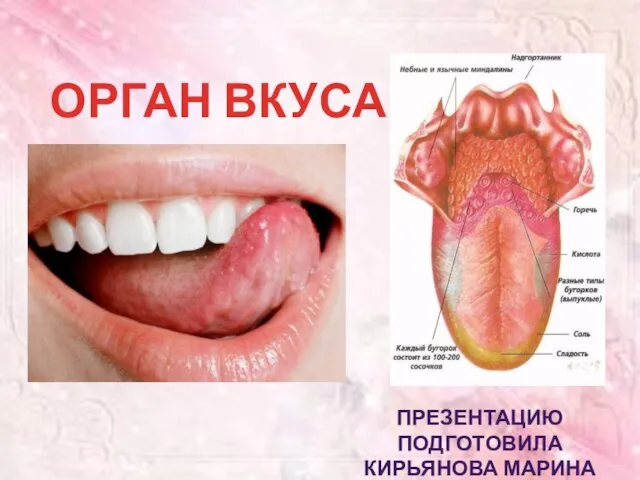 Презентация по биологии Орган вкуса
Презентация по биологии Орган вкуса Тропические бабочки. Опыт содержания в домашних условиях
Тропические бабочки. Опыт содержания в домашних условиях Подцарство Многоклеточные
Подцарство Многоклеточные Таинственные незнакомцы. Организмы со сложной ядерной клеткой - эукариоты
Таинственные незнакомцы. Организмы со сложной ядерной клеткой - эукариоты ( о рыбах) ( о рыбах)
( о рыбах) ( о рыбах)  Биология – наука о живой природе
Биология – наука о живой природе  Презентация на тему Растения – живой организм
Презентация на тему Растения – живой организм