Содержание
- 2. Задание на практические занятия Классификации генов в генотипе человека конспект: «Классификации генов в генотипе» Устные ответы:
- 3. Терминология 1920 г. - Г. Винклер – термин «геном» (совокупность генов в гаплоидном наборе – характеристика
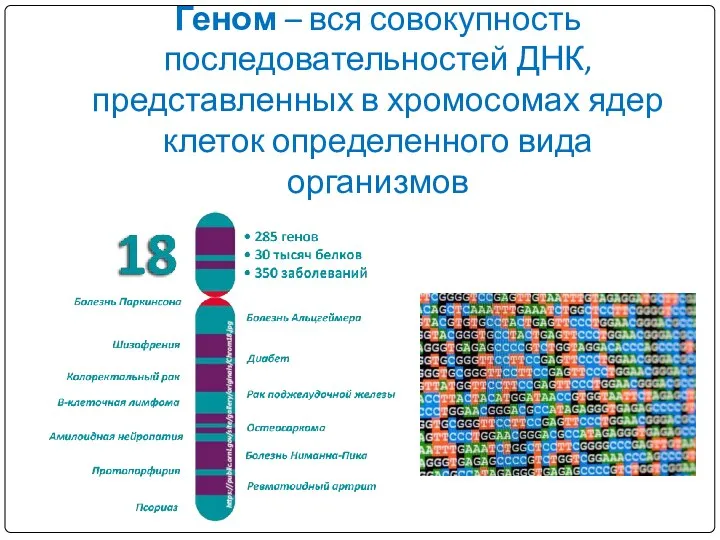
- 4. Геном – вся совокупность последовательностей ДНК, представленных в хромосомах ядер клеток определенного вида организмов
- 5. ГЕНОМЫ ЧЕЛОВЕКА и ДРУГИХ ВИДОВ ЖИВОТНЫХ (СРАВНИТЕЛЬНО-ЭВОЛЮЦИОННЫЙ АСПЕКТ) В ГЕНОМЕ ЧЕЛОВЕКА есть ГЕНЫ: = ОБЩИЕ для
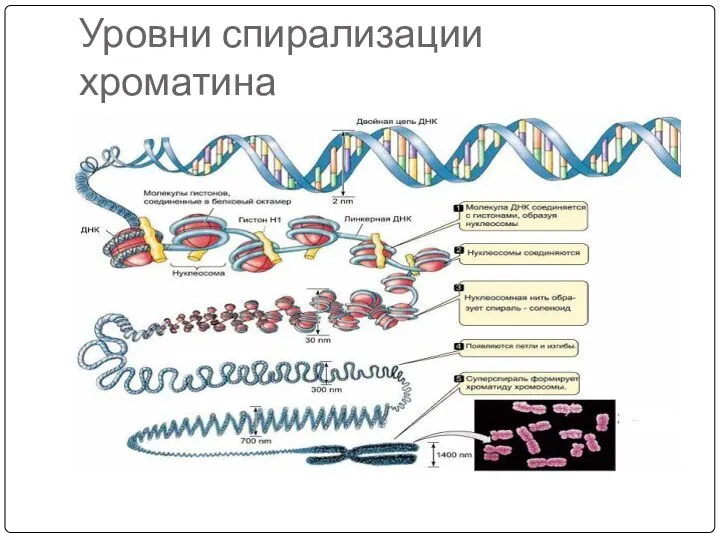
- 6. Уровни спирализации хроматина
- 7. Характеристика генома прокариот Прокариоты имеют кольцевую ДНК, которая располагается в нуклеоиде. Эта клеточная область отделена от
- 8. Геном вируса
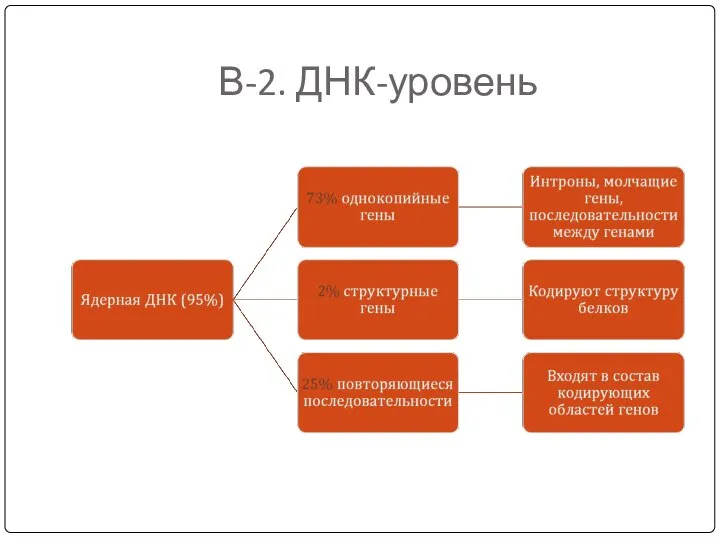
- 9. В-2. ДНК-уровень
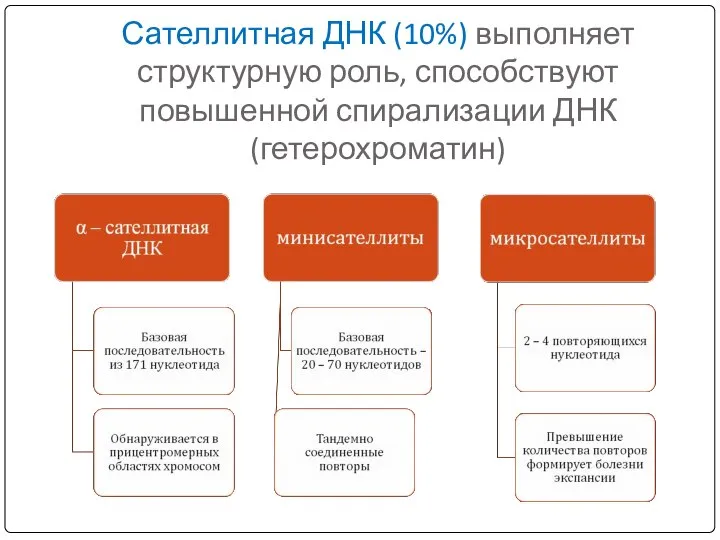
- 10. Сателлитная ДНК (10%) выполняет структурную роль, способствуют повышенной спирализации ДНК (гетерохроматин)
- 11. Болезни экспансии К болезням экспансии относятся наследственные заболевания, обусловленные динамическими мутациями. В основе динамических мутаций лежит
- 13. Болезни экспансии У некоторых больных синдромом Ушера (Ашера) идентифицирована инсерция Alu-повторов в 9 экзоне гена рецептора
- 14. Синдром Ашера (Ушера) Синдром Ашера - это сочетание врожденной нейросенсорной тугоухости, медленно прогрессирующей пигментной дегенерации сетчатки
- 16. Диспергированные повторы (15%) – выполняют регуляторные функции
- 17. Гипотезы о роли интронов Внутри интронных областей одних генов могут располагаться экзоны других генов, «прочитывающихся» в
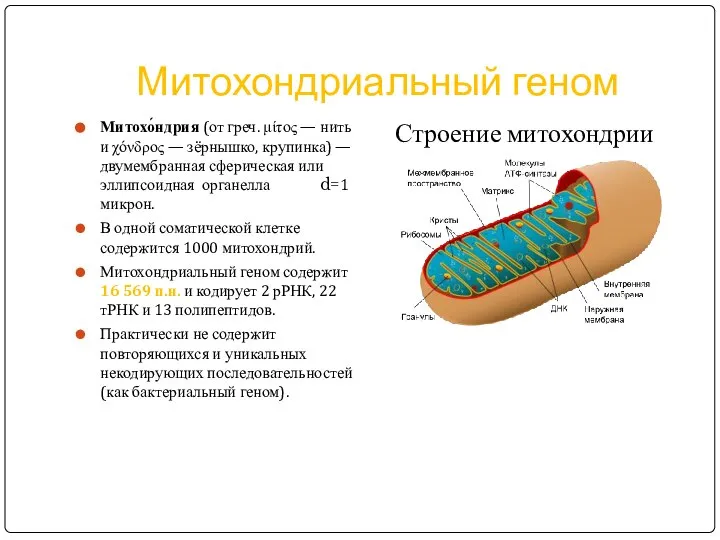
- 18. Митохондриальный геном Митохо́ндрия (от греч. μίτος — нить и χόνδρος — зёрнышко, крупинка) — двумембранная сферическая
- 19. Распределение структурных генов Митохондриальный геном
- 20. Особенности митохондриального генома 1) мтДНК наследуется по материнскому типу (доля отцовских митохондрий в зиготе – от
- 21. Митохондриальные болезни Описаны различные сочетания следующих клинических признаков: повторные коматозные состояния, сопровождающиеся ацидозом крови и увеличением
- 22. Геном как единое целое Несмотря на дискретное генетическое определение отдельных признаков, в индивидуальном развитии воссоздается единый
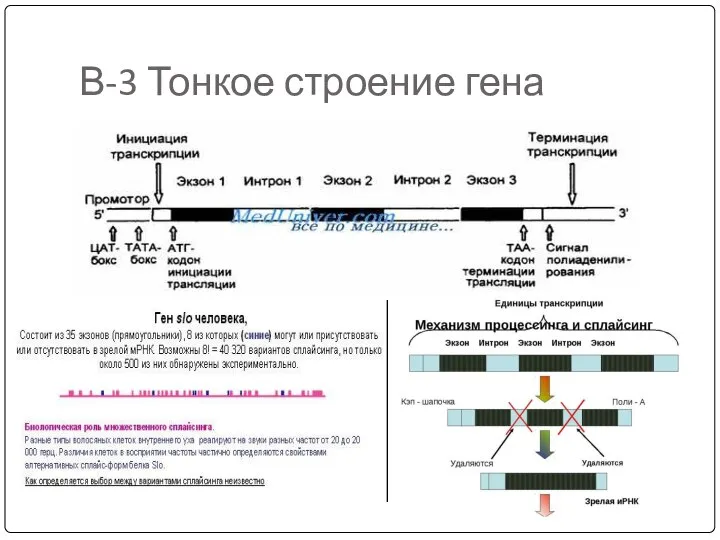
- 23. В-3 Тонкое строение гена
- 28. Регуляторные зоны Регуляторные зоны - это участки ДНК на которых не происходит синтез РНК, но которые
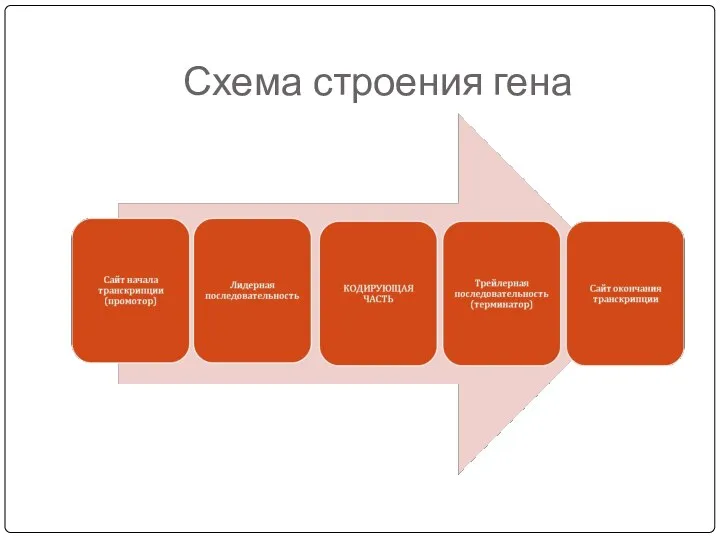
- 29. Регуляторные участки гена содержат: А. Стартовый кодон – сайт (место) начала транскрипции (распознает фермент). Б. Промотор
- 31. Контролирующие зоны Лидерной называется 5'-нетранслируемая часть мРНК. Обычно лидерная последовательность имеет в длину несколько десятков нуклеотидов,
- 32. Функции контролирующих зон Лидерная последовательность транскрибируется, но не транслируется, и может регулировать возможность самого процесса транскрипции.
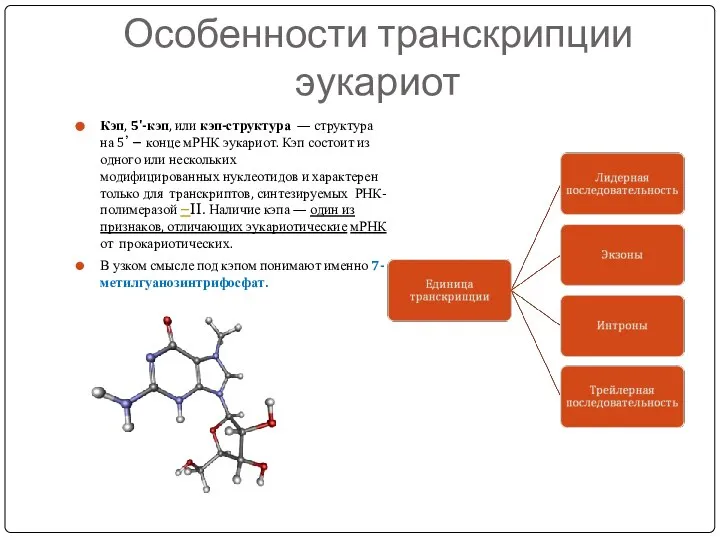
- 33. Особенности транскрипции эукариот Кэп, 5'-кэп, или кэп-структура — структура на 5’ – конце мРНК эукариот. Кэп
- 34. Роль хвоста поли-(А) Хвост поли-(А ) - полиаденильный хвост, некодируемая поли (А) -последовательность эукариотических мРНК длиной
- 35. ТАТА-бокс TATA-бокс (бокс Хогнесса, TATA-box): у эукариот последовательность ДНК, богатая А – Т парами (ТAТA(A/Т)A(A/Т)), содержащая
- 36. Схема строения гена
- 37. Виды регуляторных последовательностей Образование комплекса транскрипции и его активность в свою очередь контролируют ещё два типа
- 38. Факторы транскрипции РНК-полимераза эукариот не может самостоятельно инициировать транскрипцию. Для ее активации необходимо большое количество белков,
- 39. Виды РНК-полимераз
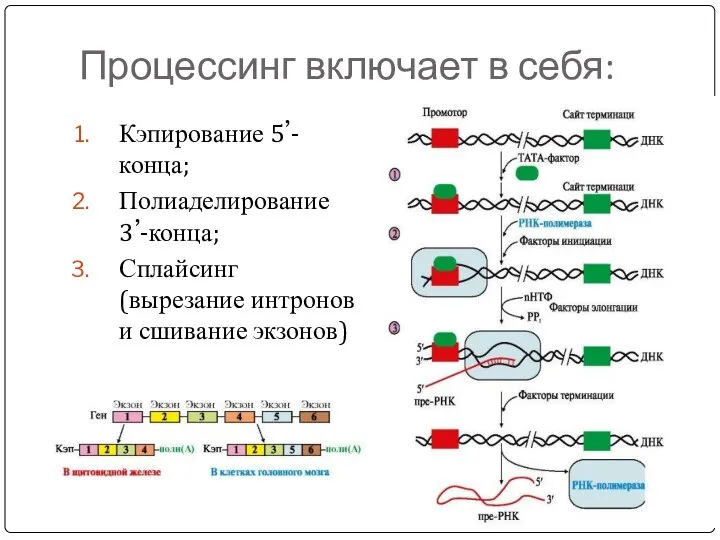
- 40. Процессинг включает в себя: Кэпирование 5’-конца; Полиаделирование 3’-конца; Сплайсинг (вырезание интронов и сшивание экзонов)
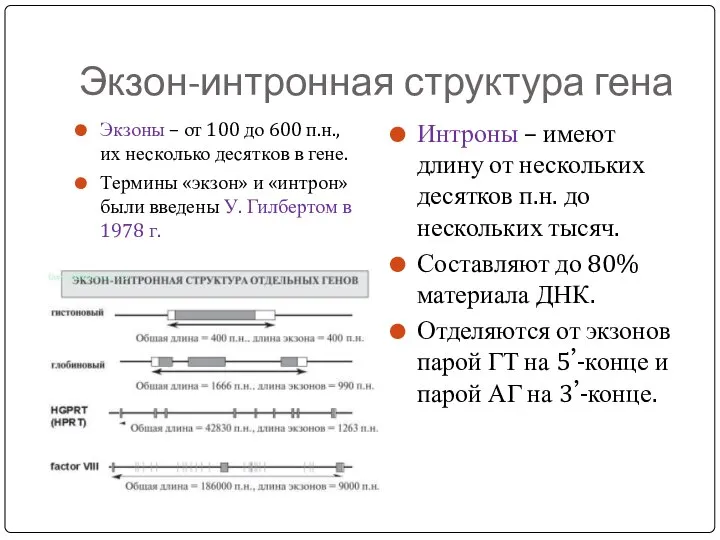
- 43. Экзон-интронная структура гена Экзоны – от 100 до 600 п.н., их несколько десятков в гене. Термины
- 44. Мультигенные семейства генов Эти гены обычно сгруппированы в кластеры в определенных районах одной или нескольких хромосом
- 45. Человеческие лейкоцитарные антигены Система генов тканевой совместимости человека ( HLA, Human Leucocyte Antigens) — группа антигенов
- 46. Система HLA представляет собой индивидуальный набор различного типа белковых молекул, находящихся на поверхности клеток. Набор антигенов
- 49. HLA-типирование – определение HLA-варианта Типирование на HLA-B27 является, пожалуй, самым известным из всех. Этот антиген относится
- 50. HLA-типирование для оценки риска сахарного диабета Ученые пришли к выводу, что некоторые аллели (варианты одного гена)
- 51. HLA-антигены и невынашивание беременности Одним из иммунологических факторов невынашивания беременности является совпадение по 3 и более
- 55. Сроки развития наследственных болезней во многом зависят от функций вовлеченного в патологию гена: - гены, кодирующие
- 56. Карты хромосом Генети́ческая ка́рта — схема взаимного расположения структурных генов, регуляторных элементов и генетических маркеров, а
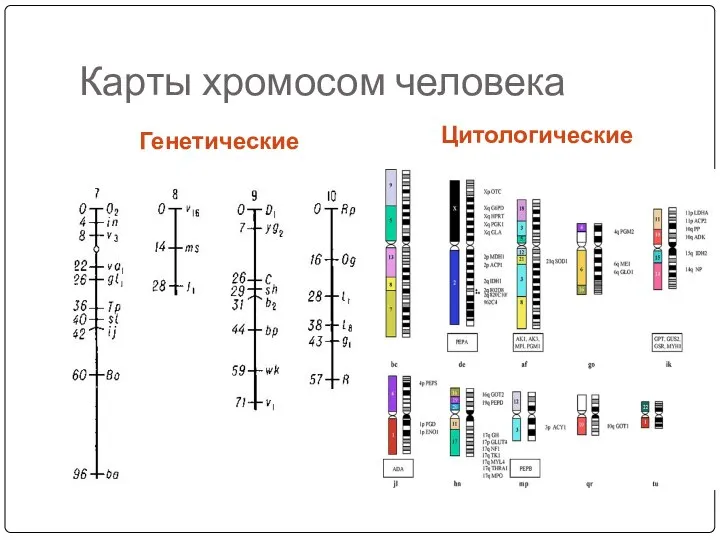
- 57. Карты хромосом человека Генетические Цитологические
- 61. Скачать презентацию















































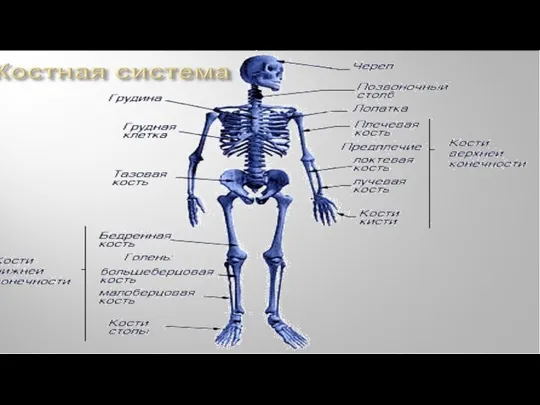 Соединение костей
Соединение костей Клетка. Единица жизни
Клетка. Единица жизни Подготовка к контрольному тестированию по теме «Дыхательная система»
Подготовка к контрольному тестированию по теме «Дыхательная система»  Зрительная система человека
Зрительная система человека Активный центр белка и его взаимодействие с лигандом
Активный центр белка и его взаимодействие с лигандом Австралопитек. Место в эволюции
Австралопитек. Место в эволюции Кролики. Домашние животные
Кролики. Домашние животные Токсикологическое значение наркотических веществ. Химико-токсикологическая характеристика психоактивных веществ. (Лекция 8)
Токсикологическое значение наркотических веществ. Химико-токсикологическая характеристика психоактивных веществ. (Лекция 8) Презентация на тему Регенерация дождевого червя
Презентация на тему Регенерация дождевого червя  Алдыңғы іш қабырғасының анатомиялық құрылымы
Алдыңғы іш қабырғасының анатомиялық құрылымы Биоритмы - внутренние часы человека Работу выполнили: ученицы 9 класса «Б» Городничева Кристина Алимова Анжелика Климова Регина.
Биоритмы - внутренние часы человека Работу выполнили: ученицы 9 класса «Б» Городничева Кристина Алимова Анжелика Климова Регина. День Птиц. Синица
День Птиц. Синица Дыхательная система человека
Дыхательная система человека Зачем мы ночью спим
Зачем мы ночью спим Мышцы предплечья, кисти
Мышцы предплечья, кисти Жители морей и океанов
Жители морей и океанов Круглые черви
Круглые черви Глід. Ліки з плодів гльоду
Глід. Ліки з плодів гльоду .
. Растения-производители Тема 19 Живые участники круговорота веществ. Глава 4.
Растения-производители Тема 19 Живые участники круговорота веществ. Глава 4. Матричные биосинтезы-2
Матричные биосинтезы-2 Классификация бактерий. Морфология бактерий
Классификация бактерий. Морфология бактерий Влияние влажности на человека
Влияние влажности на человека Возникновение и развитие жизни на Земле
Возникновение и развитие жизни на Земле Тема урока «Систематика моллюсков»
Тема урока «Систематика моллюсков» Нервная ткань
Нервная ткань Взаимодействие электромагнитных излучений с живыми системами. Фотохимические процессы, люминесценция
Взаимодействие электромагнитных излучений с живыми системами. Фотохимические процессы, люминесценция Болезни пчел
Болезни пчел