Содержание
- 2. Классификация гидроксидов и оксидов алюминия Гидроксиды алюминия Модификации тригидроксида алюминия Al(OH)3: наиболее часто встречаются гиббсит (гидраргиллит),
- 3. Оксиды алюминия Основные кристаллические фазы Al2O3: α, χ, γ, δ, η, θ и др. Низкотемпературные оксиды,
- 4. Получение гидроксида алюминия на глиноземных заводах Сырье для производства тригидрата алюминия - боксит А1(ОН)3 и нефелин
- 5. Получение гидроксида алюминия переосаждением тригидрата Алюминатный метод. Тригидрат алюминия растворяют в щелочи: Al(OH)3 + NaOH +
- 6. Получение гидроксида алюминия гидролизом алкоголятов CONDEA (в настоящее время SASOL) Синтез триэтилалюминия Al + 1/2H2 +
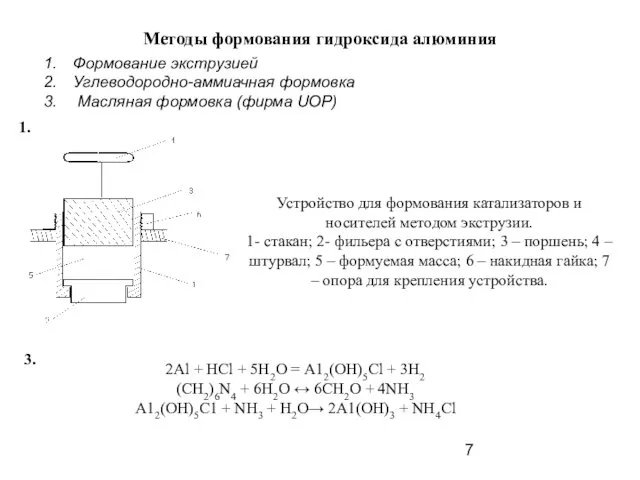
- 7. Методы формования гидроксида алюминия Устройство для формования катализаторов и носителей методом экструзии. 1- стакан; 2- фильера
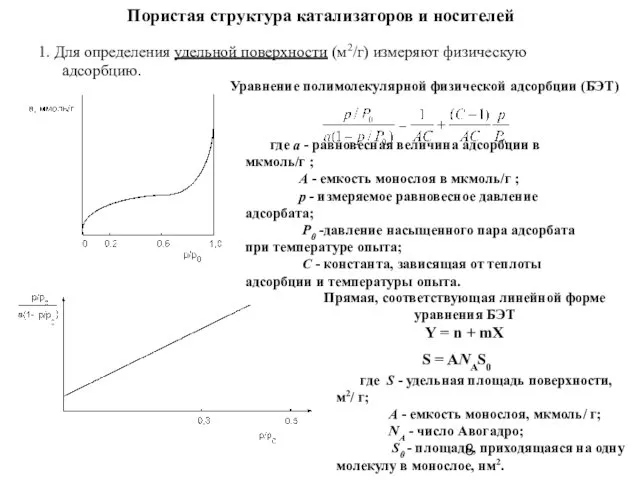
- 8. Пористая структура катализаторов и носителей 1. Для определения удельной поверхности (м2/г) измеряют физическую адсорбцию. Уравнение полимолекулярной
- 9. 2. Удельный объем пор катализатора : Vуд. = 3. Распределение пор по радиусам (эффективный радиус пор,
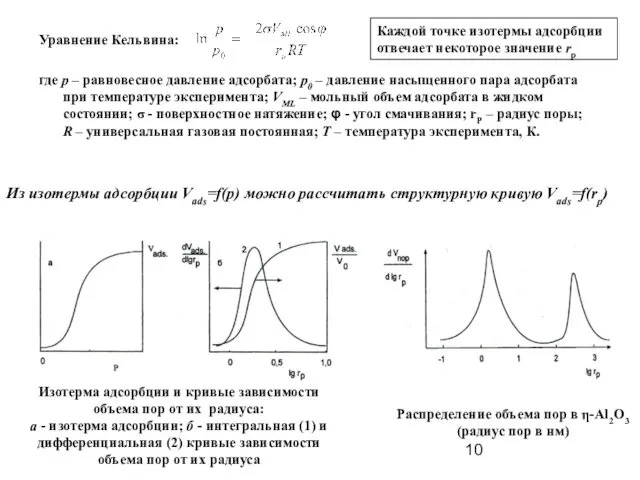
- 10. Уравнение Кельвина: где р – равновесное давление адсорбата; р0 – давление насыщенного пара адсорбата при температуре
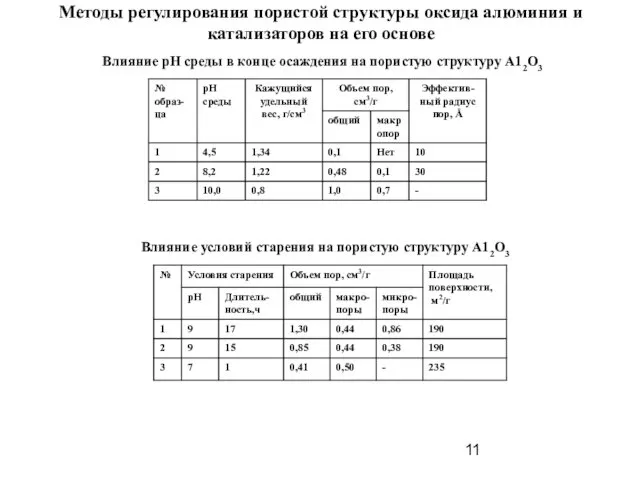
- 11. Методы регулирования пористой структуры оксида алюминия и катализаторов на его основе Влияние рН среды в конце
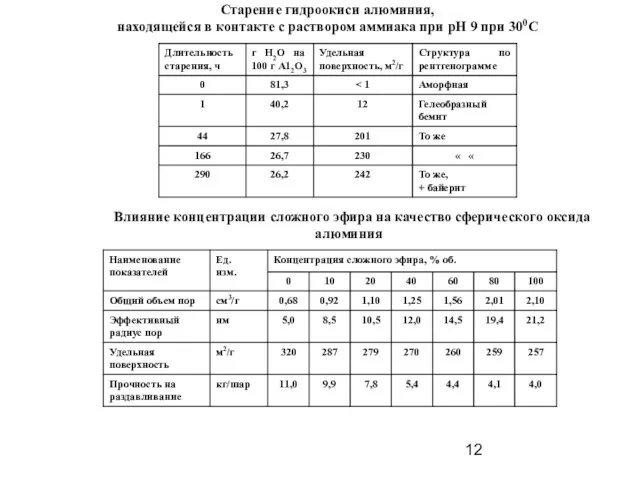
- 12. Старение гидроокиси алюминия, находящейся в контакте с раствором аммиака при рН 9 при 300С Влияние концентрации
- 13. Методы исследования катализаторов Физико-механические характеристики катализаторов Химический состав катализаторов Методы измерения каталитической активности катализаторов 3.1. Статические
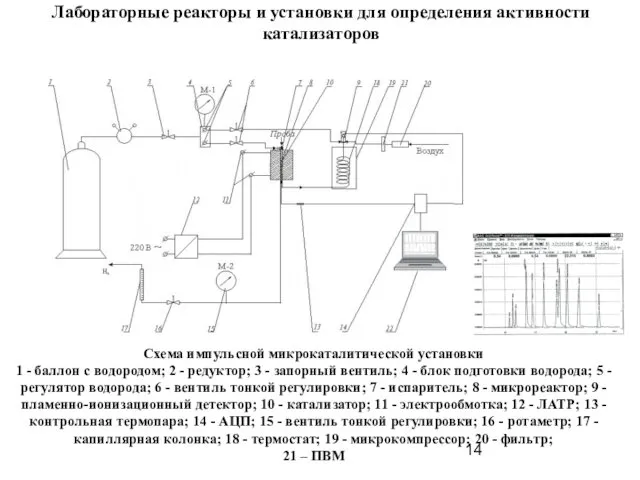
- 14. Лабораторные реакторы и установки для определения активности катализаторов Схема импульсной микрокаталитической установки 1 - баллон с
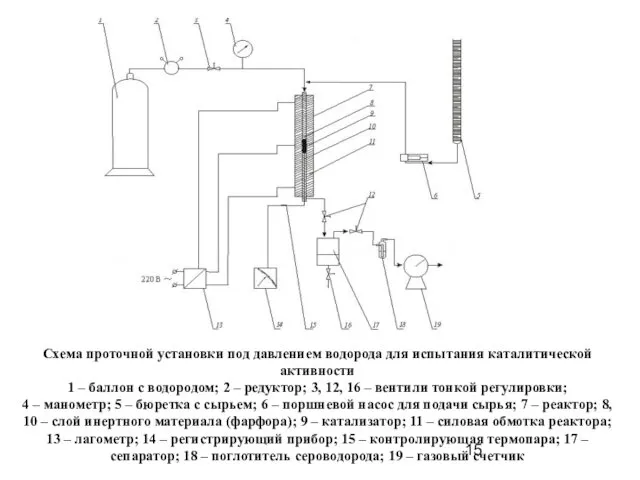
- 15. Схема проточной установки под давлением водорода для испытания каталитической активности 1 – баллон с водородом; 2
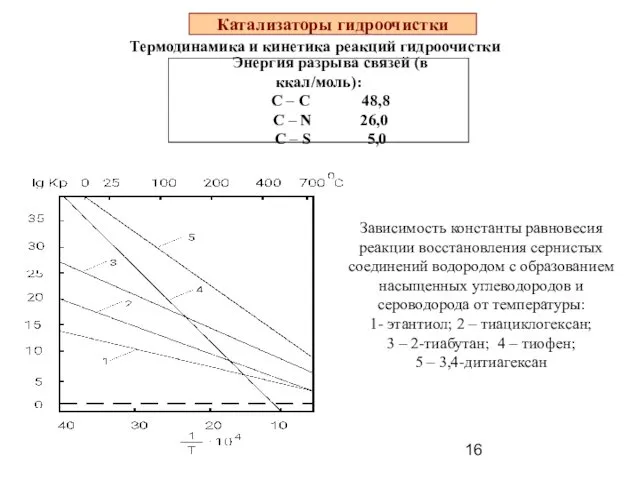
- 16. Катализаторы гидроочистки Термодинамика и кинетика реакций гидроочистки Энергия разрыва связей (в ккал/моль): С – С 48,8
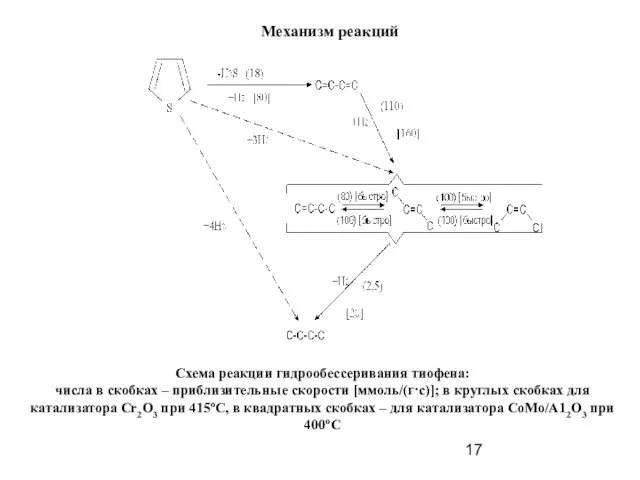
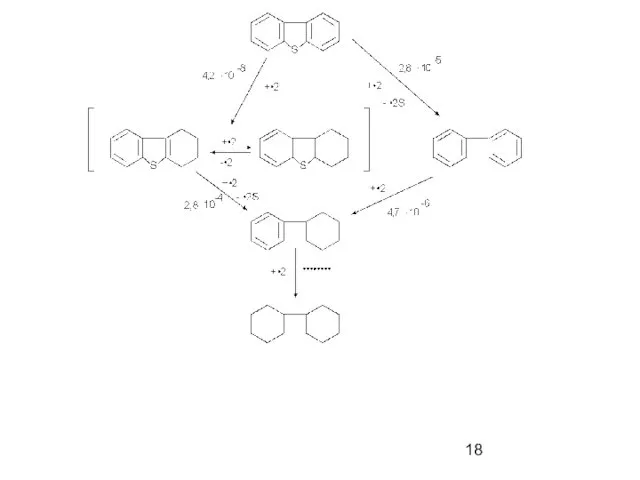
- 17. Механизм реакций Схема реакции гидрообессеривания тиофена: числа в скобках – приблизительные скорости [ммоль/(г·с)]; в круглых скобках
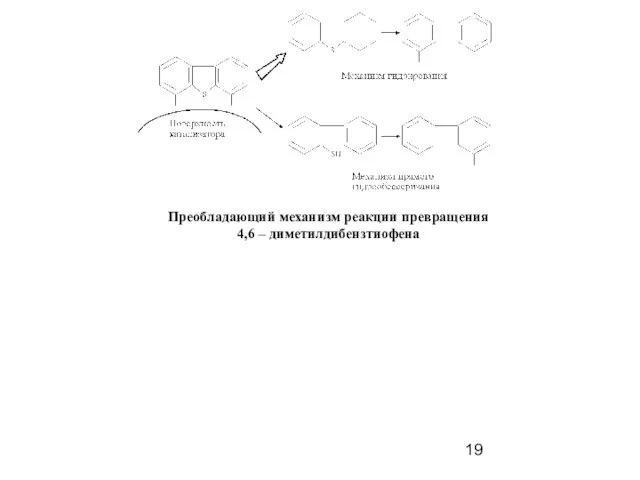
- 19. Преобладающий механизм реакции превращения 4,6 – диметилдибензтиофена
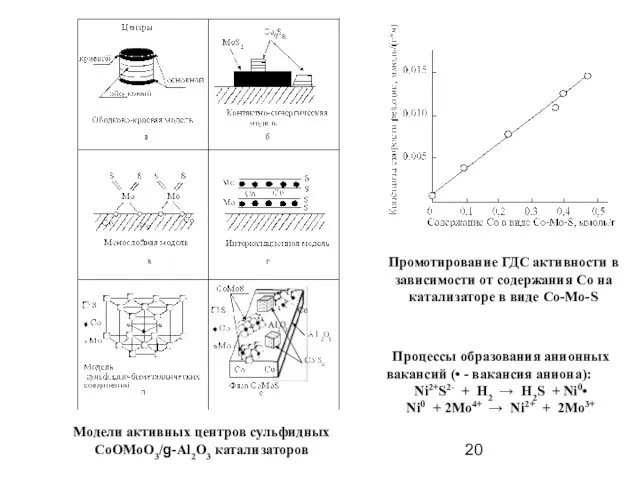
- 20. Модели активных центров сульфидных CoOMoO3/g-Al2O3 катализаторов Промотирование ГДС активности в зависимости от содержания Со на катализаторе
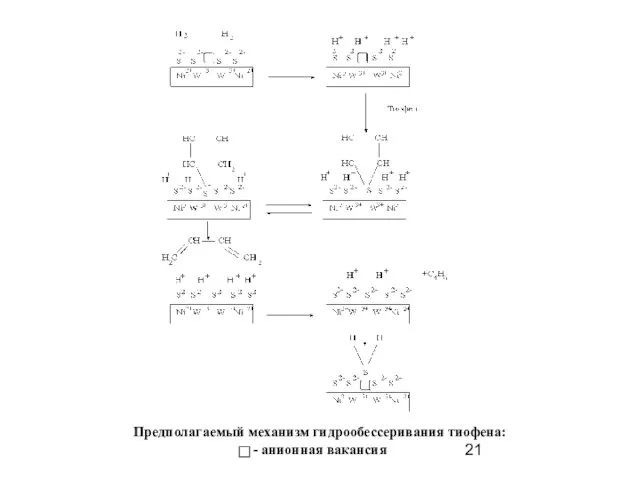
- 21. Предполагаемый механизм гидрообессеривания тиофена: - анионная вакансия
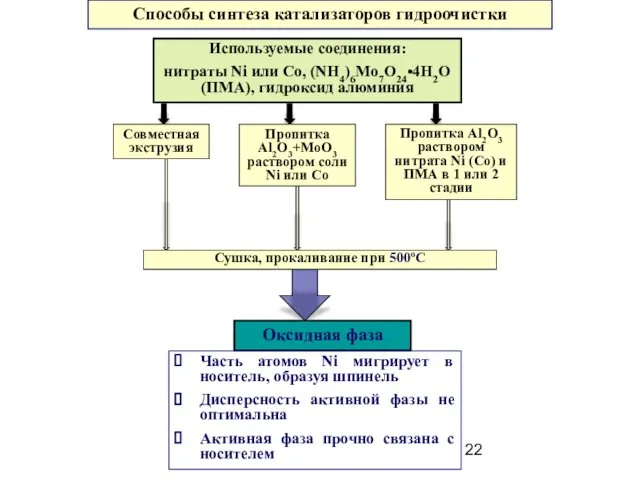
- 22. Способы синтеза катализаторов гидроочистки Оксидная фаза Часть атомов Ni мигрирует в носитель, образуя шпинель Дисперсность активной
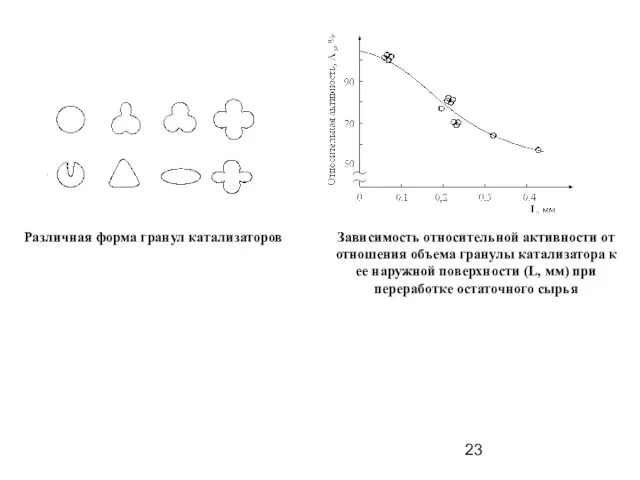
- 23. Различная форма гранул катализаторов Зависимость относительной активности от отношения объема гранулы катализатора к ее наружной поверхности
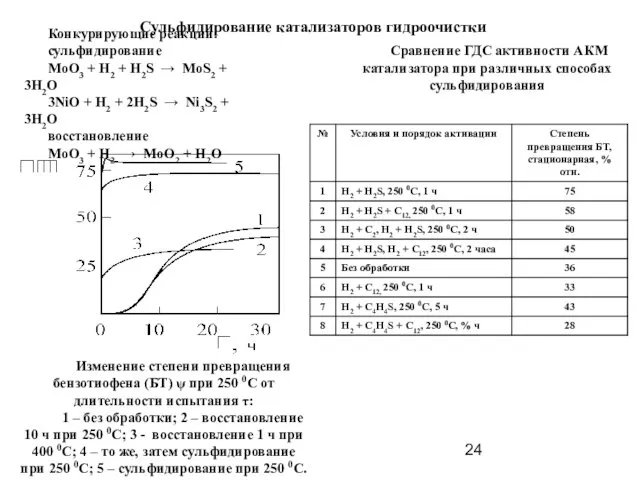
- 24. Сульфидирование катализаторов гидроочистки Конкурирующие реакции: сульфидирование MoO3 + H2 + H2S → MoS2 + 3H2O 3NiO
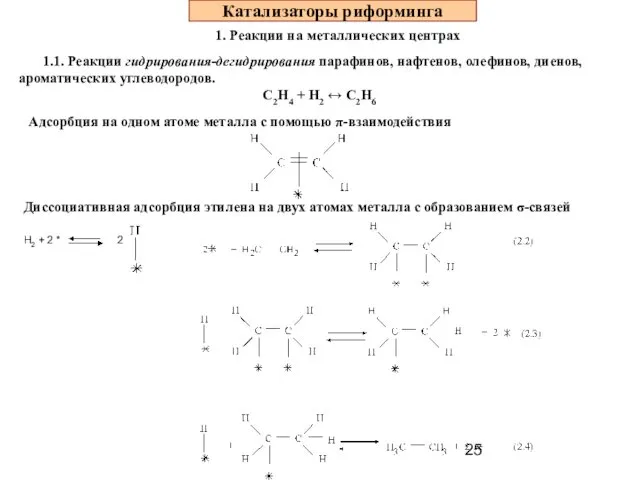
- 25. Катализаторы риформинга 1. Реакции на металлических центрах 1.1. Реакции гидрирования-дегидрирования парафинов, нафтенов, олефинов, диенов, ароматических углеводородов.
- 27. Скачать презентацию







 Полевая геофизика. Сейсморазведка
Полевая геофизика. Сейсморазведка Магнитное поле
Магнитное поле Обозначения и единицы измерения
Обозначения и единицы измерения Всемирное тяготение - притяжение всех тел во Вселенной
Всемирное тяготение - притяжение всех тел во Вселенной Система мониторинга водного баланса Балтийского моря
Система мониторинга водного баланса Балтийского моря Сейсмическая стратиграфия
Сейсмическая стратиграфия Electric charge and electric field
Electric charge and electric field Podstawy elektroniki i miernictwa elektronicznego
Podstawy elektroniki i miernictwa elektronicznego Выполнил: Ушанов Андрей
Выполнил: Ушанов Андрей Конденсатор. Энергия заряженного конденсатора
Конденсатор. Энергия заряженного конденсатора Сила трения
Сила трения Простая и интересная физика у Вас дома (Обязательно пытайтесь повторить это самостоятельно!!!)
Простая и интересная физика у Вас дома (Обязательно пытайтесь повторить это самостоятельно!!!) Опиливание. Технология. 6 класс
Опиливание. Технология. 6 класс Аттестационная работа. Программа элективного курса по физике для 10-11 класса «Решение нестандартных задач по физике»
Аттестационная работа. Программа элективного курса по физике для 10-11 класса «Решение нестандартных задач по физике» Теория решения изобретательских задач. Законы кинематики
Теория решения изобретательских задач. Законы кинематики Методические рекомендации при выполнении экспериментальных заданий ГИА по физике
Методические рекомендации при выполнении экспериментальных заданий ГИА по физике Смеси идеальных газов. I закон термодинамики. Внутренняя энергия и работа
Смеси идеальных газов. I закон термодинамики. Внутренняя энергия и работа Проектирование МДП СБИС. Структуры МДП в СБИС
Проектирование МДП СБИС. Структуры МДП в СБИС Ведучі мости, карданні передачі, коробки відбору потужності та лебідки автомобілів
Ведучі мости, карданні передачі, коробки відбору потужності та лебідки автомобілів Квантовые компьютеры
Квантовые компьютеры Кинематика. Средняя скорость
Кинематика. Средняя скорость Трёхфазные цепи
Трёхфазные цепи Презентация по физике "Электромагнетизм" - скачать
Презентация по физике "Электромагнетизм" - скачать  Классификация магнитных методов контроля
Классификация магнитных методов контроля Тема 11. Классификация весоизмерительных приборов.
Тема 11. Классификация весоизмерительных приборов. Статистична інтерпретація хвильової функції. (Лекція 4)
Статистична інтерпретація хвильової функції. (Лекція 4) Электромагнитная совместимость и средства защиты. (Лекция 21)
Электромагнитная совместимость и средства защиты. (Лекция 21) Ультрадисперсные (наноструктурные и ультрамелкозернистые) материалы
Ультрадисперсные (наноструктурные и ультрамелкозернистые) материалы