Содержание
- 2. Лекция 7. Квантовомеханическая модель атома водорода План лекции 7.1. Квантование энергии. Главное квантовое число. 7.2. Распределение
- 3. 7.1. Квантование энергии. Главное квантовое число С точки зрения квантовой механики, электрон в атоме водорода находится
- 4. U r E1 E2 E3 Потенциальная яма для электрона в атоме водорода Е – полная энергия
- 5. Уравнение Шредингера для стационарных состояний имеет вид: Электрон находится в центральном, сферически симметричном электрическом поле, поэтому
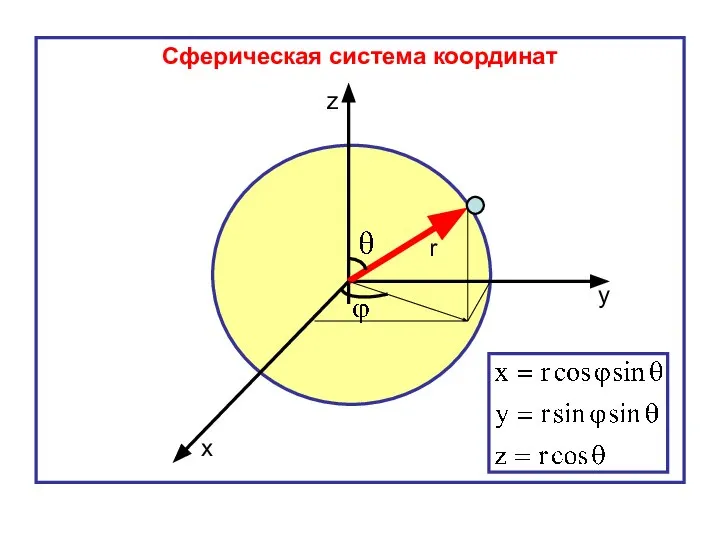
- 6. r x у z Сферическая система координат
- 7. Уравнение Шредингера в сферических координатах имеет сложный вид, но более простое математическое решение. Е – полная
- 8. При решении уравнения Шредингера в сферических координатах получены следующие результаты: собственные значения полной энергии электрона Е
- 9. Уравнение Шредингера имеет требуемые однозначные конечные и непрерывные решения в следующих случаях: при любых положительных Е;
- 10. Случай Е = 0 соответствует отрыву электрона от атома. 2. Случай E > 0 соответствует свободному
- 11. Однако в квантовой механике данные значения энергии получаются как следствие основных положений этой науки, т.е. решения
- 12. Главное квантовое число: - принимает целочисленные значения: n = 1, 2, 3, … определяет номер стационарных
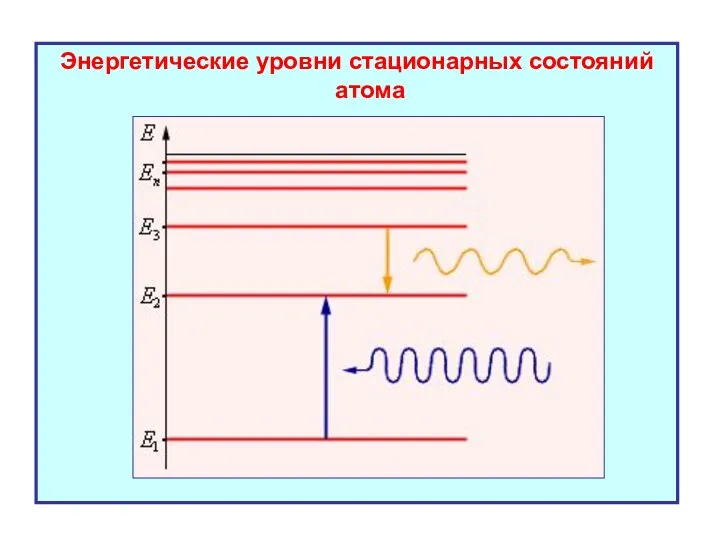
- 13. Энергетические уровни стационарных состояний атома
- 14. 7.2. Распределение электронного заряда в атоме. Орбитальное квантовое число Рассмотрим собственные волновые функции электрона, которые зависят
- 15. Радиальная часть волновой функции: Угловые части волновой функции: Квадрат модуля волновых функций определяет вероятность обнаружения электрона
- 16. Эта вероятность различна в разных частях объёма атома. Заряд электрона «размазан» по всему объёму атома, образуя
- 17. Для стационарных состояний атома волновые функции также зависят от расстояния r электрона от ядра атома. Существует
- 18. Радиальная часть волновой функции (форма орбитали) зависят от двух квантовых чисел: n, l. Орбитальное квантовое число
- 19. При условии n = 1, 2, 3… и l = 0 форма электронного облака обладает сферической
- 20. Сферическая форма электронного облака n = 1, l = 0 Вероятность обнаружить электрон на расстояниях, как
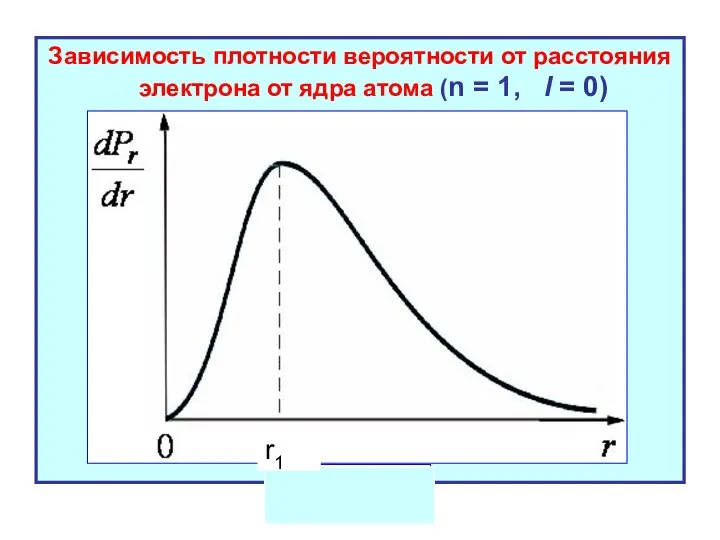
- 21. Зависимость плотности вероятности от расстояния электрона от ядра атома (n = 1, l = 0) r1
- 22. В состоянии с квантовыми числами n = 2 и l = 0 максимальная вероятность приходится на
- 23. Распределение вероятности обнаружения электрона в атоме водорода в состояниях 1s и 2s
- 24. Для р -, d -, f - состояний плотность электронного облака зависит не только от расстояния
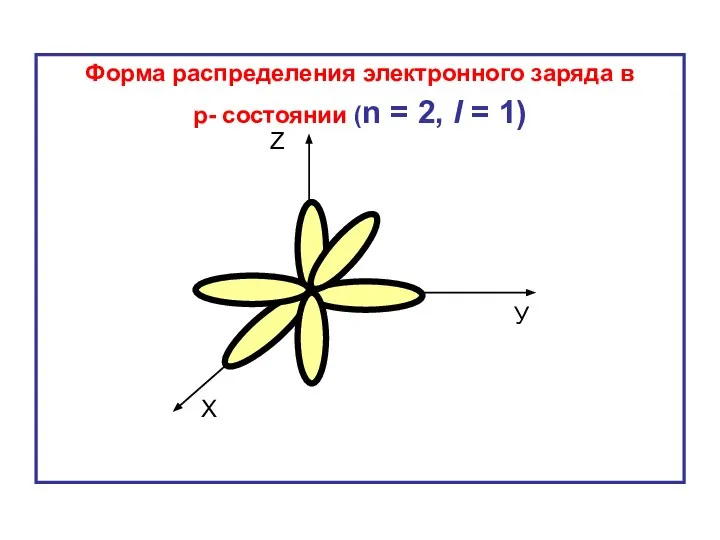
- 25. Форма распределения электронного заряда в р- состоянии (n = 2, l = 1) Х У Z
- 26. За радиус атома принято считать расстояние r, на которое приходится 95 % объёмной плотности заряда. Самый
- 27. Таким образом, волновой характер движения электрона приводит к тому, что понятие орбиты теряет классический смысл. Заряд
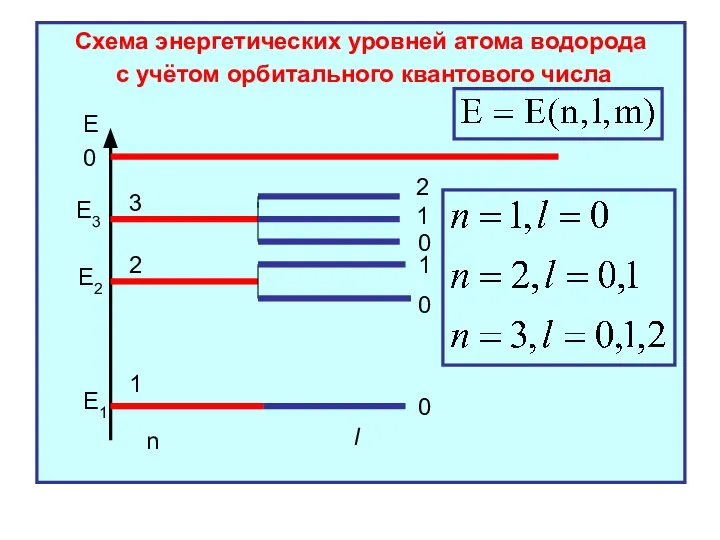
- 28. Схема энергетических уровней атома водорода с учётом орбитального квантового числа Е 0 Е1 Е2 Е3 n
- 29. 7.3. Квантование орбитального момента импульса. Согласно первому постулату Бора момент импульса электрона (L = mvr) квантуется
- 30. При больших значениях n (l ~n ) обе формулы практически дают одинаковый ответ. Магнитный момент импульса
- 31. Единицей квантования орбитального механического момента импульса L является перечёркнутая постоянная Планка. Единицей квантования орбитального магнитного момента
- 32. 7.4. Пространственное квантование. Магнитное квантовое число Рассмотрим атом, помещённый в магнитное поле. Направления как механического ,
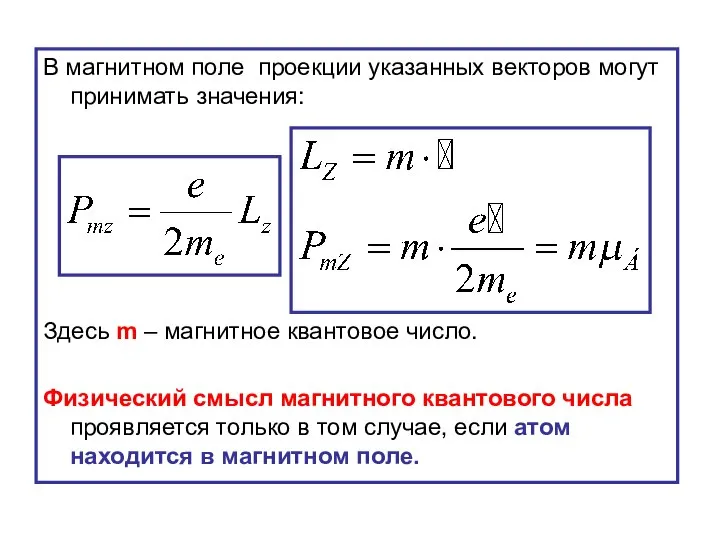
- 33. В магнитном поле проекции указанных векторов могут принимать значения: Здесь m – магнитное квантовое число. Физический
- 34. Магнитное квантовое число принимает целочисленные значения: принимает всего (2l +1) значение при заданном значении орбитального квантового
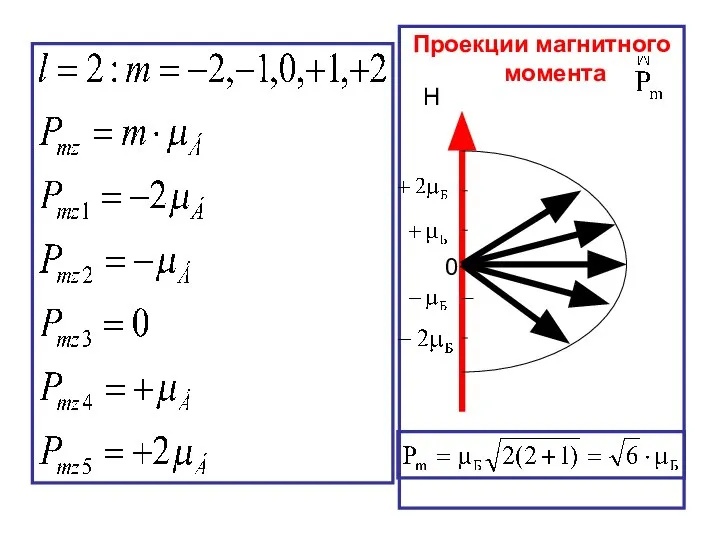
- 35. Рассмотрим случай, когда l = 2. Магнитное число примет всего (2l +1) = 5 значений. Значит
- 36. Проекции механического момента 0 Н
- 37. Проекции магнитного момента H 0
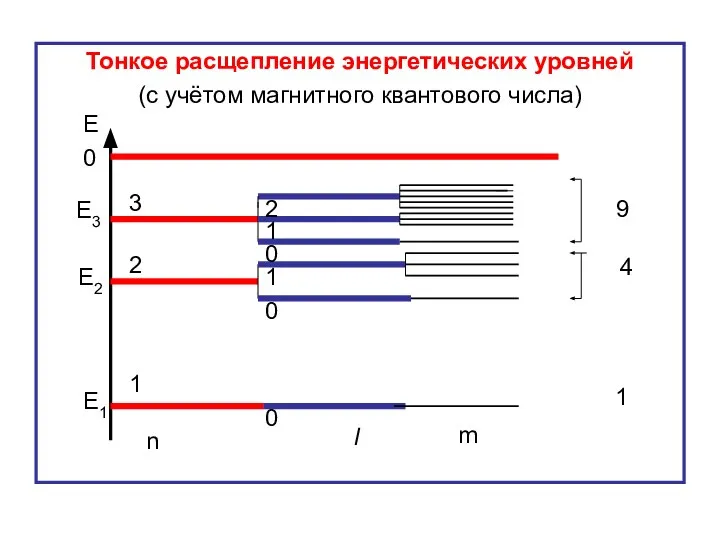
- 38. Тонкое расщепление энергетических уровней (с учётом магнитного квантового числа) Е 0 Е1 Е2 Е3 n l
- 39. 7.5. Квантование собственного момента импульса. Спиновое квантовое число В 1925 году американские физики Уленбек и Гоудсмит
- 40. По современным представлениям всем элементарным частицам природы (микрочастицам) приписывают наличие спина. Спин: следует считать внутренним свойством,
- 41. Спин: собственный момент импульса частицы; - имеет одно единственное значение: .. S – спиновое квантовое число.
- 42. К фермионам относятся микрочастицы с полуцелым спином: К ним принадлежат электроны, протоны, нейтроны и другие элементарные
- 43. Для электрона: Собственный механический момент импульса электрона имеет одно единственное значение:
- 44. Собственные магнитный и механический моменты электрона связаны соотношением: Тогда для собственного магнитного момента имеем:
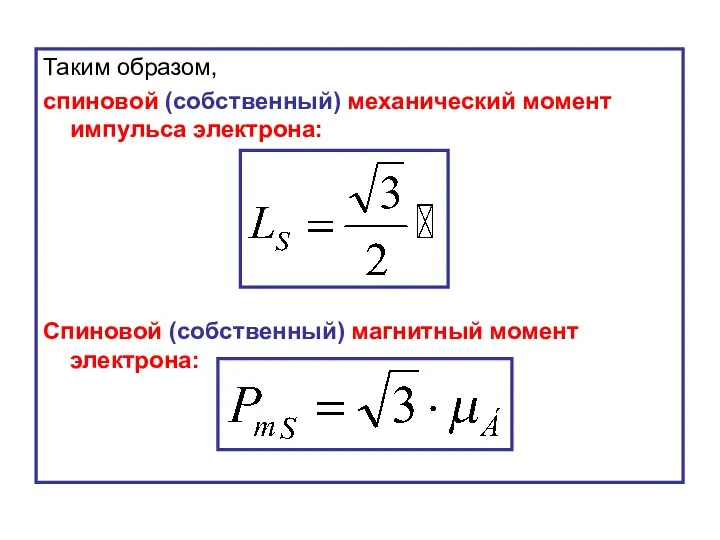
- 45. Таким образом, спиновой (собственный) механический момент импульса электрона: Спиновой (собственный) магнитный момент электрона:
- 46. В пространстве спин электрона на направление внешнего магнитного поля принимает только две проекции.
- 47. В пространстве спиновой магнитный момент электрона на направление внешнего магнитного поля принимает только две проекции.
- 48. Н Проекции спинового механического момента (спина) Проекции спинового магнитного момента 0 Н 0
- 49. Сверхтонкое расщепление энергетических уровней (с учётом спинового квантового числа) Е 0 Е1 Е2 Е3 n l
- 50. Число возможных энергетических состояний атома ( с учётом всех четырёх квантовых чисел) где n – главное
- 51. 7.6. Энергетический спектр атома водорода Значения полной энергии электрона в атоме водорода зависят от всех четырёх
- 52. Главное квантовое число определяет энергию стационарных состояний: . Принято говорить, что энергетические уровни с данным числом
- 53. Энергетические уровни стационарных состояний атома
- 54. Расщепление уровней по орбитальному квантовому числу Е 0 Е1 Е2 Е3 n l 1 2 3
- 55. Расщепление энергетических уровней по магнитному квантовому числу происходит в магнитном поле и названо тонким расщеплением. Такое
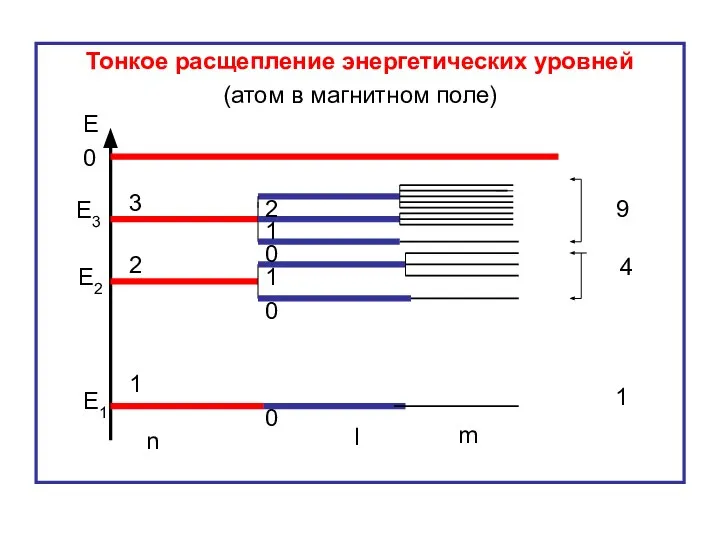
- 56. Тонкое расщепление энергетических уровней (атом в магнитном поле) Е 0 Е1 Е2 Е3 n l 1
- 57. С учётом трёх квантовых чисел уровень с заданным числом n расщепляется на n2 подуровней. Число возможных
- 58. Кратность тонкого вырождения уровней: первого: n = 1 равна 1; второго: n = 2 равна 4;
- 59. Сверхтонким называется расщепление энергетических уровней по спиновому квантовому числу. Оно было обнаружено П. Зееманом в слабых
- 60. Сверхтонкое расщепление энергетических уровней (с учётом спинового квантового числа) Е 0 Е1 Е2 Е3 n l
- 61. С учётом всех четырёх квантовых чисел число возможных энергетических состояний электрона в атоме водорода и любом
- 63. Скачать презентацию


















































 Технологический процесс ремонта генератора переменного тока автомобиля ГАЗ - 3307
Технологический процесс ремонта генератора переменного тока автомобиля ГАЗ - 3307 Динамометр. Взаимодействие тел. Урок 29/20 7 класс Учитель: Ермакова Мира Владимировна МОУ «ООШ х.Малая Скатовка Саратовского рай
Динамометр. Взаимодействие тел. Урок 29/20 7 класс Учитель: Ермакова Мира Владимировна МОУ «ООШ х.Малая Скатовка Саратовского рай Брейн-ринг «Юные знатоки физики»
Брейн-ринг «Юные знатоки физики» Относительная, удельная и характеристическая вязкость. Их определение
Относительная, удельная и характеристическая вязкость. Их определение Презентация Тепловые электростанции
Презентация Тепловые электростанции  Строение атомного ядра. Ядерные силы
Строение атомного ядра. Ядерные силы G. Рулевое управление
G. Рулевое управление Презентация по физике "Тепловые явления" - скачать бесплатно
Презентация по физике "Тепловые явления" - скачать бесплатно Расчет требуемой мощности электродвигателя привода при различных режимах работы
Расчет требуемой мощности электродвигателя привода при различных режимах работы Радиоактивные батарейки
Радиоактивные батарейки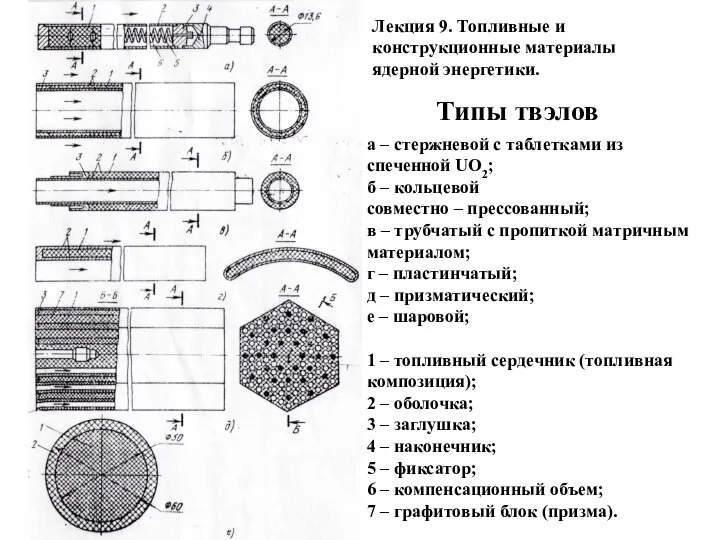 Типы твэлов. Лекция 9
Типы твэлов. Лекция 9 Закон Архимеда
Закон Архимеда Квантовая физика
Квантовая физика Лазер. Принцип действия лазера. Лазерное излучение
Лазер. Принцип действия лазера. Лазерное излучение Презентация Сила тока
Презентация Сила тока  Радио и радиоволны в нашей жизни Веб-квест Руководители: Учителя физики, информатики, истории, литературы. Участники: Ученики
Радио и радиоволны в нашей жизни Веб-квест Руководители: Учителя физики, информатики, истории, литературы. Участники: Ученики  ПОЛЯРИЗАЦИЯ И ДИФРАКЦИЯ СВЕТА ФИЗИКА, 11 КЛАСС
ПОЛЯРИЗАЦИЯ И ДИФРАКЦИЯ СВЕТА ФИЗИКА, 11 КЛАСС Решение задач. Закон сохранения энергии
Решение задач. Закон сохранения энергии Изотермический процесс, нагрев
Изотермический процесс, нагрев Постоянные магниты
Постоянные магниты День Радио
День Радио Твердотельные лазеры
Твердотельные лазеры Обслуживание ВС на перроне
Обслуживание ВС на перроне Корпускулярно-волновой дуализм света
Корпускулярно-волновой дуализм света Динамика материальной точки
Динамика материальной точки Обслуживание, символы и термины Jatco 4AT
Обслуживание, символы и термины Jatco 4AT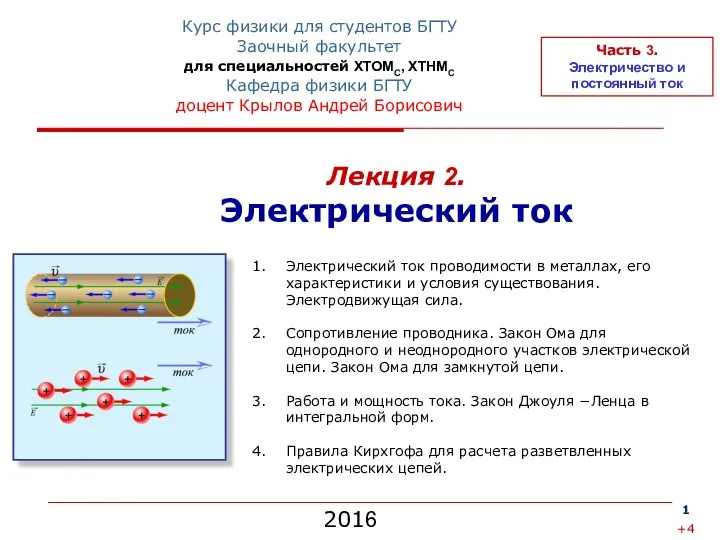 Электрический ток. (лекция 2)
Электрический ток. (лекция 2) Особенности водно-химического режима в контурах ЯЭУ
Особенности водно-химического режима в контурах ЯЭУ