Содержание
- 2. Атом водорода является простейшим атомом. Он состоит из протона и электрона, удерживаемых рядом электричес-кой силой. Эта
- 5. Интересно оценить величину энергии по (41.16). Подставив значения величин, получим: Е=-21.8*10-19 Дж. В микромире энергия измеряется
- 7. Связь их с декартовыми показана на рисунке. Кроме того вместо параметров поступательного движения (масса, импульс) используются
- 8. На рисунке показан график зависимости квадрата модуля радиальной компоненты волновой функции от расстояния –r до ядра.
- 10. На рисунке показаны рассчитанные формы орбита-лей для различных значений l. Спектроскописты присвоили каждому из возможных значений
- 11. Магнитное квантовое число (mℓ) характеризует пространственную ориентацию атомной орбитали принимает значения: целых чисел от –l до
- 12. Каждому значению главного квантового числа n соответствует энергетический уровень. Кроме то-го, каждому n соответствует n возможных
- 13. Для каждого значения l разрешено (2l + 1) значений m. Например, l=4 (f – подуровень). Тогда
- 14. Излучение и поглощение света атомами. Электрон, находящийся на энергетическом уровне выше основного (n>1), может с определенной
- 15. Если фотон испускается в результате перехода между уровнями с энергиями Еn1> и Еn2, то его энергия
- 17. Стрелками показаны переходы атома водорода между различными энергетическими уровнями и соответствующие этим переходам спектральные серии. Серия
- 19. Пятиминутка: Рассчитать длины волн в спектре излучения атома водорода, соответствующих переходам серии Бальмера. Постоянную Ридберга для
- 20. Фундаментальные природные закономерности: законы сохранения энергии, импульса, момента импульса являются выражением свойств времени и пространства. Закон
- 21. Аналогичный сюрприз можно ожидать от враща-тельного движения частицы. Ее момент импульса также будет квантован и иногда
- 22. Значение спинового числа (s) определяется свойствами симметрии частицы. Если она абсолютно симметрична, т.е. при повороте на
- 23. С учетом спинового числа состояние электрона в атоме характеризуется 4 квантовыми числами, которые обозначаются n, l,
- 25. Скачать презентацию






















 Лекция 3. Возможные случаи приведения к равнодействующей сил произвольно расположенных в пространстве
Лекция 3. Возможные случаи приведения к равнодействующей сил произвольно расположенных в пространстве Alternative Energy Sources
Alternative Energy Sources Гамма-излучение
Гамма-излучение Элементная база электронных устройств
Элементная база электронных устройств Механические волны
Механические волны Магнитно-резонансная томография и спектроскопия ЯМР. Биомедицинские приложения
Магнитно-резонансная томография и спектроскопия ЯМР. Биомедицинские приложения Законы динамики. Уравнения движения
Законы динамики. Уравнения движения Тема: Приборы по физике своими руками и простые опыты с ними. Работу выполнил: ученик 9 класса- Давыдов Рома Руководитель: учит
Тема: Приборы по физике своими руками и простые опыты с ними. Работу выполнил: ученик 9 класса- Давыдов Рома Руководитель: учит Ионизирующие излучения
Ионизирующие излучения Задача № 1 на расчет плотности тела
Задача № 1 на расчет плотности тела Оценка механических свойств покрытия
Оценка механических свойств покрытия День Моля
День Моля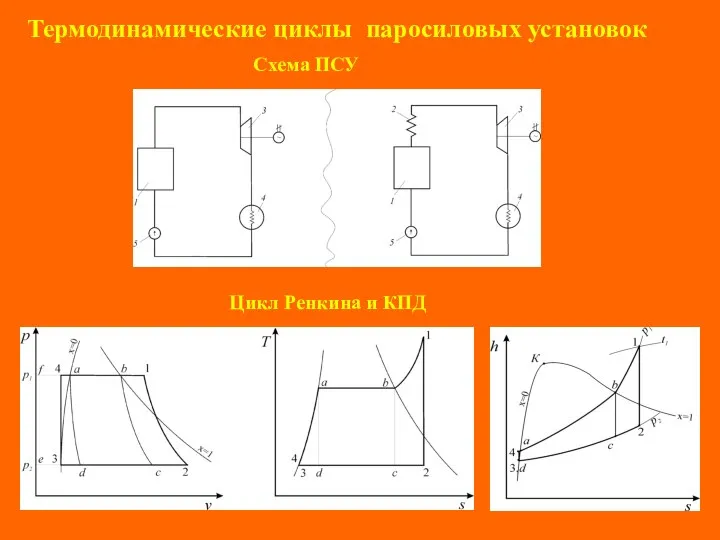 Термодинамические циклы паросиловых установок
Термодинамические циклы паросиловых установок Уравнения Максвелла для электромагнитного поля
Уравнения Максвелла для электромагнитного поля Работа по физике Тема: «Циклоны и антициклоны»
Работа по физике Тема: «Циклоны и антициклоны» Физика. Вопросы. Практическая работа
Физика. Вопросы. Практическая работа Истоирия создания реле. Вклад Дж.Генри
Истоирия создания реле. Вклад Дж.Генри Презентация по физике Острота зрения
Презентация по физике Острота зрения  Специальная теория относительности
Специальная теория относительности Шикізат базасы және химия өндірісінің бастапқы заттары
Шикізат базасы және химия өндірісінің бастапқы заттары История развития электрического освещения
История развития электрического освещения Лекция 10.7. Фазовые диаграммы
Лекция 10.7. Фазовые диаграммы Типы химических реакций
Типы химических реакций 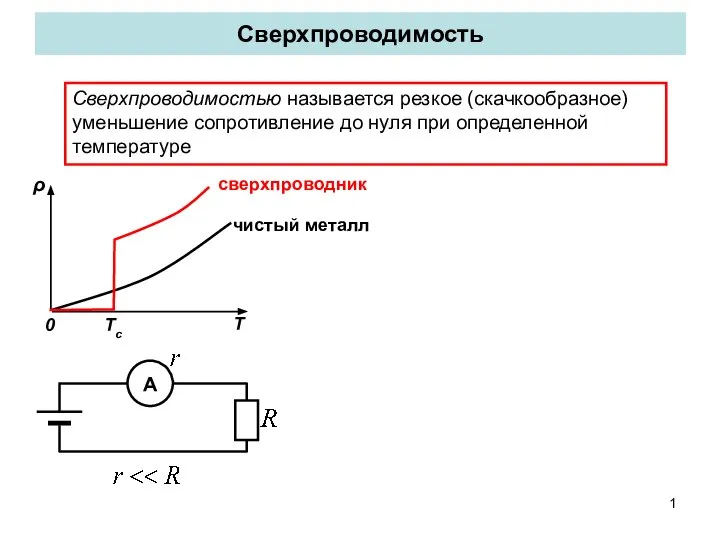 Сверхпроводимость. Криопроводники
Сверхпроводимость. Криопроводники Физико-химическое явление электролиз
Физико-химическое явление электролиз Динамика материальной точки. (Лекция 1)
Динамика материальной точки. (Лекция 1) Электромагнетизм
Электромагнетизм Лекция 13
Лекция 13