Содержание
- 2. 1.Статистический и термодинамический методы
- 4. Идеальный газ
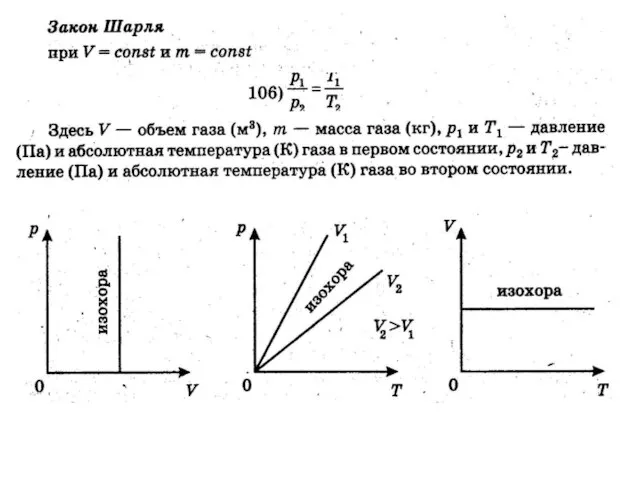
- 5. 2. Изопроцессы
- 6. Уравнение Клапейрона
- 10. ЗАКОН ДАЛЬТОНА: Давление смеси идеальных газов равно сумме парциальных давлений, входящих в нее газов.
- 11. Уравнение Клапейрона – Менделеева
- 12. Основное уравнение молекулярно-кинетической теории газов
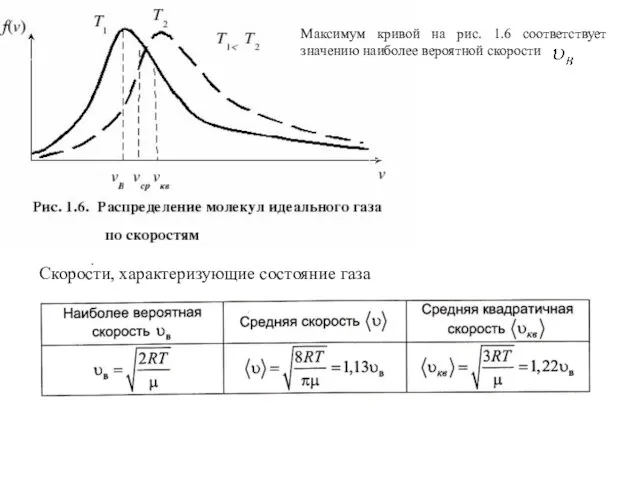
- 13. Закон Максвелла о распределении молекул идеального газа по скоростям
- 14. Скорости, характеризующие состояние газа Максимум кривой на рис. 1.6 соответствует значению наиболее вероятной скорости .
- 15. 1. Из формулы наиболее вероятной скорости следует, что при повышении температуры максимум функции распределения молекул по
- 16. Барометрическая формула
- 17. Распределение Больцмана
- 18. Средняя длина свободного пробега молекул
- 19. Явление переноса
- 20. Теплопроводность
- 21. Диффузия
- 22. Внутреннее трение (вязкость)
- 23. Основы термодинамики
- 24. Важной характеристикой термодинамической системы является ее внутренняя энергия. Внутренняя энергия - однозначная функция термодинамического состояния системы
- 25. Внутренняя энергия для произвольной массы идеального газа:
- 26. Первое начало термодинамики
- 27. Закон сохранения и превращения энергии, получил название первого начала термодинамики: количество теплоты , переданное системе, идет
- 28. Удельная теплоемкость вещества – величина, равная количеству теплоты, необходимому для нагревания 1 кг вещества на 1
- 29. Молярная теплоемкость - величина, равная количеству теплоты, необходимому для нагревания 1 моля вещества на 1 К:
- 30. Уравнение Майера - постоянная Пуассона.
- 31. Применение первого начала термодинамики к изопроцессам.
- 32. Изотермический процесс.
- 33. Изобарный процесс.
- 34. Изохорный процесс.
- 35. Адиабатный процесс - процесс, при котором отсутствует теплообмен между системой и окружающей средой. Все быстропротекающие процессы
- 36. Термодинамический процесс называется обратимым, если он может происходить как в прямом, так и в обратном направлении.
- 37. Энтропией называется функция состояния системы, дифференциалом которой является :
- 38. Для обратимых процессов изменение энтропии: - это выражение называется равенство Клаузиуса.
- 39. это неравенство Клаузиуса. При любом необратимом процессе в замкнутой системе энтропия возрастает (dS > 0).
- 40. Тогда для замкнутой системы – математическая запись второго начала термодинамики. Таким образом, для произвольного процесса, где,
- 41. Изменение энтропии в изопроцессах:
- 42. Второе начало термодинамики 1) по Кельвину: невозможен круговой процесс, единственным результатом которого является превращение теплоты, полученной
- 43. Математической формулировкой второго начала является выражение Энтропия замкнутой системы при любых происходивших в ней процессах не
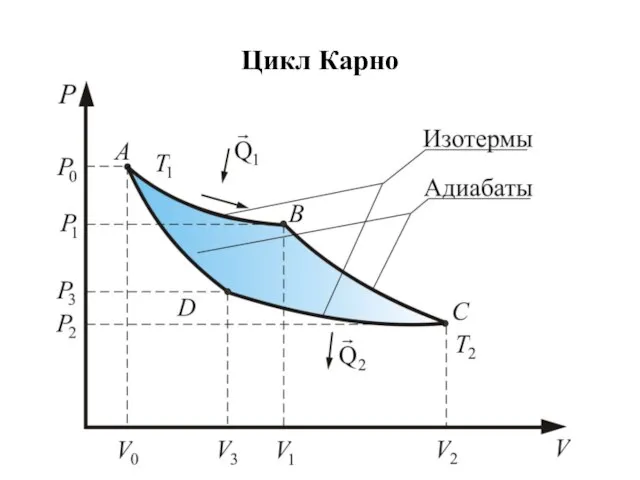
- 44. Цикл Карно
- 46. Скачать презентацию








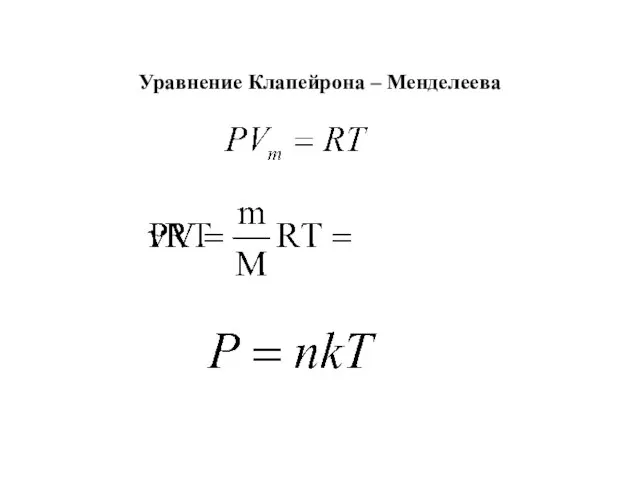





















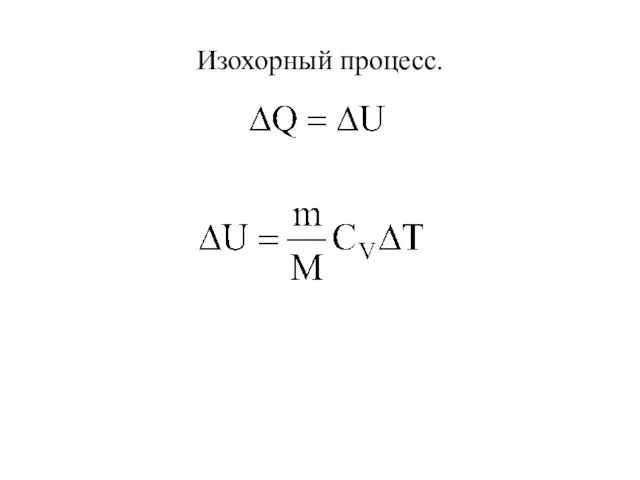









 Гирокомпас на основе лазерного гироскопа с магнитооптическим управлением
Гирокомпас на основе лазерного гироскопа с магнитооптическим управлением Синтез механизмов. Основные задачи и методы синтеза
Синтез механизмов. Основные задачи и методы синтеза Лазеры. Принцип действия
Лазеры. Принцип действия Гидрогазодинамика
Гидрогазодинамика Горение в карбюраторных ДВС
Горение в карбюраторных ДВС Конкурс «Интерактивная мозаика» Pedsovet.su Журун Татьяна Юрьевна Интерактивная презентация сопровождения игры по физике и химии
Конкурс «Интерактивная мозаика» Pedsovet.su Журун Татьяна Юрьевна Интерактивная презентация сопровождения игры по физике и химии  Сверхпроводники. Эффект Мейснера
Сверхпроводники. Эффект Мейснера Физическая картина мира
Физическая картина мира Магнитное поле
Магнитное поле Технология изготовления кессона крыла из КМ Истребитель EAP КЕССОН
Технология изготовления кессона крыла из КМ Истребитель EAP КЕССОН Тести по КЕ
Тести по КЕ Работа и мощность
Работа и мощность Твердотельные реле
Твердотельные реле Квантовая радиофизика
Квантовая радиофизика Энергия. Кинетическая и потенциальная энергия. Вывод закона сохранения механической энергии
Энергия. Кинетическая и потенциальная энергия. Вывод закона сохранения механической энергии Анализ и расчет методом комплексных амплитуд линейных цепей переменного тока
Анализ и расчет методом комплексных амплитуд линейных цепей переменного тока Основные положения МКТ (молекулярная физика)
Основные положения МКТ (молекулярная физика) Қанның реологиялық қасиеттері. (Дәріс 12)
Қанның реологиялық қасиеттері. (Дәріс 12) Физика пластической деформации кристаллов
Физика пластической деформации кристаллов Thermometers
Thermometers Автотрансформаторы. Повышающий и понижающий автотрансформаторы
Автотрансформаторы. Повышающий и понижающий автотрансформаторы Подготовка к ЕГЭ на уроках физики
Подготовка к ЕГЭ на уроках физики Релейная защита и автоматика
Релейная защита и автоматика Электромагнитная картина мира (ЭМКМ). Специальная и общая теории относительности
Электромагнитная картина мира (ЭМКМ). Специальная и общая теории относительности Развитие представлений о движении
Развитие представлений о движении Законы сохранения в механике
Законы сохранения в механике Понятие динамической системы станка. Динамическое качество станка. Основные задачи динамики станков
Понятие динамической системы станка. Динамическое качество станка. Основные задачи динамики станков Расчет силовой установки речного судна
Расчет силовой установки речного судна