Содержание
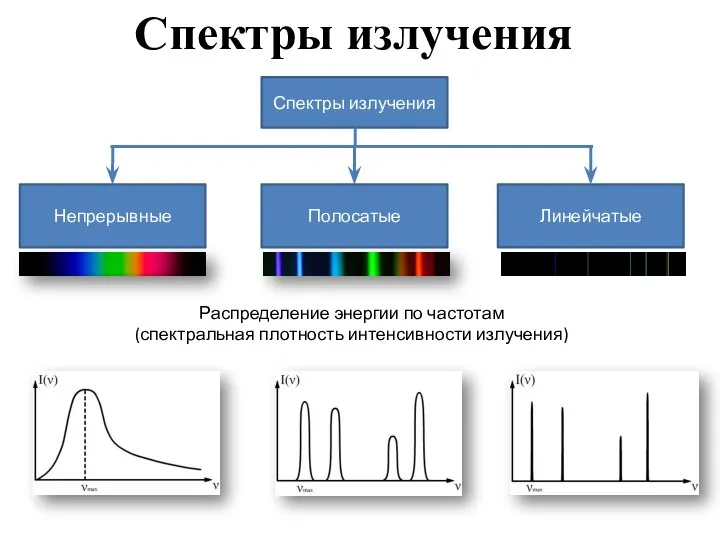
- 2. Спектры излучения Распределение энергии по частотам (спектральная плотность интенсивности излучения)
- 3. Непрерывный спектр Дают тела, находящиеся в твердом, жидком состоянии, а также плотные газы. Чтобы получить, надо
- 4. Линейчатый спектр Дают все вещества в газообразном атомарном (но не молекулярном) состоянии (атомы практически не взаимодействуют
- 5. Полосатый спектр Спектр состоит из отдельных полос, разделенных темными промежутками. Каждая полоса представляет собой совокупность большого
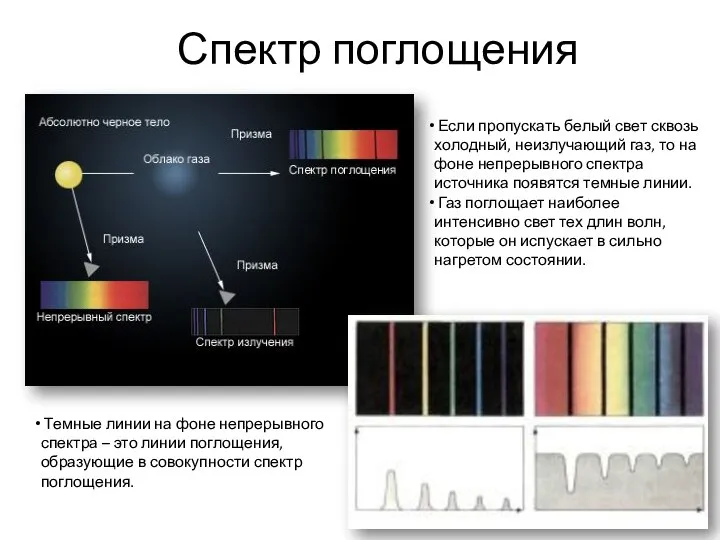
- 6. Спектр поглощения Темные линии на фоне непрерывного спектра – это линии поглощения, образующие в совокупности спектр
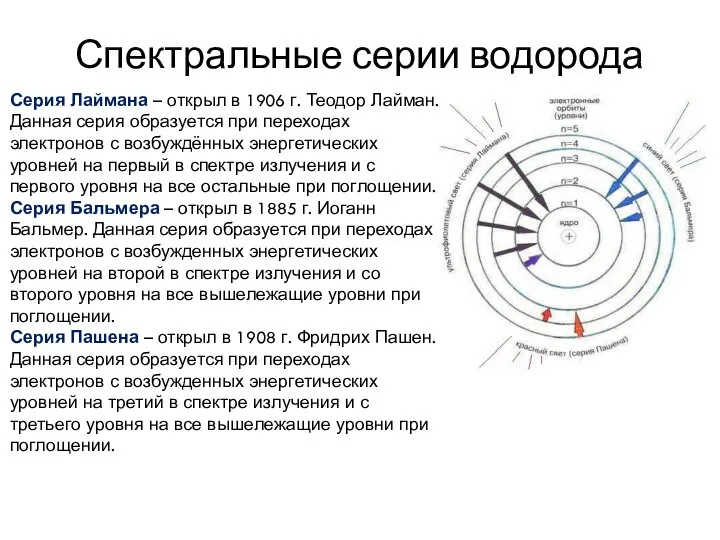
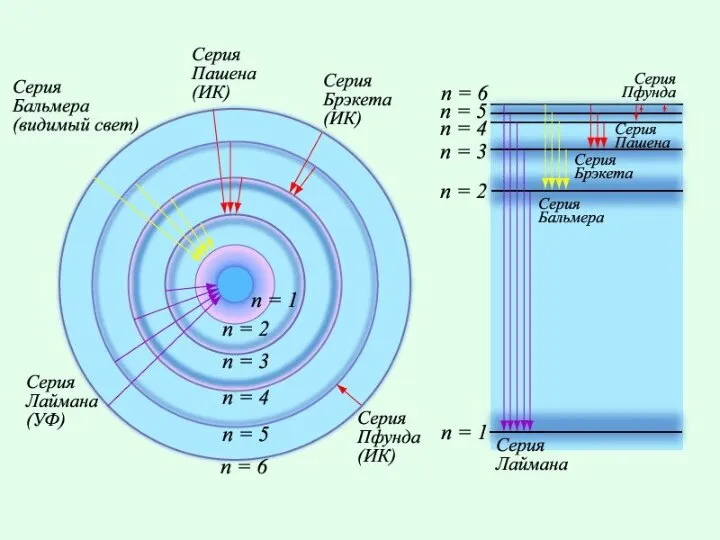
- 7. Спектральные серии водорода Серия Лаймана – открыл в 1906 г. Теодор Лайман. Данная серия образуется при
- 8. Строение атома Из истории: Демокрит: существует предел деления атома. Аристотель: делимость вещества бесконечна. Париж, 1626 г.:
- 9. Толчком к подробному изучению строения атома послужили: открытие рентгеновского излучения (1895 г., В.К. Рентген); открытие радиоактивности
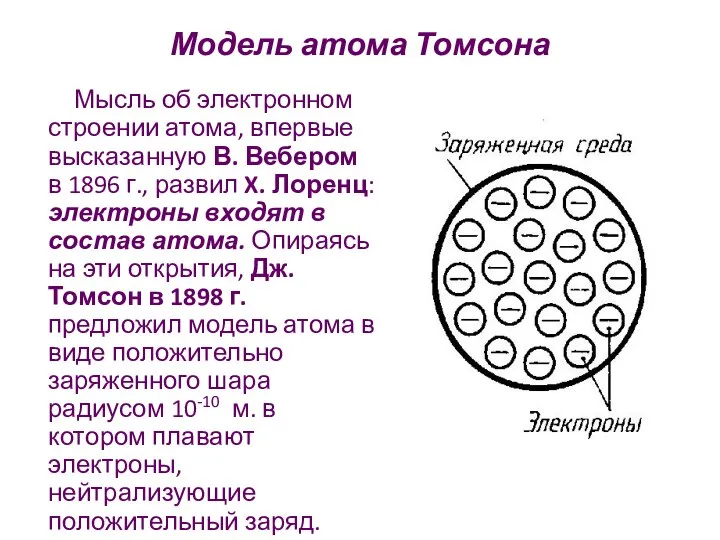
- 10. Модель атома Томсона Мысль об электронном строении атома, впервые высказанную В. Вебером в 1896 г., развил
- 11. Ядерная модель атома Экспериментальная проверка модели Томсона была осуществлена в 1911 г. английским физиком Э. Резерфордом.
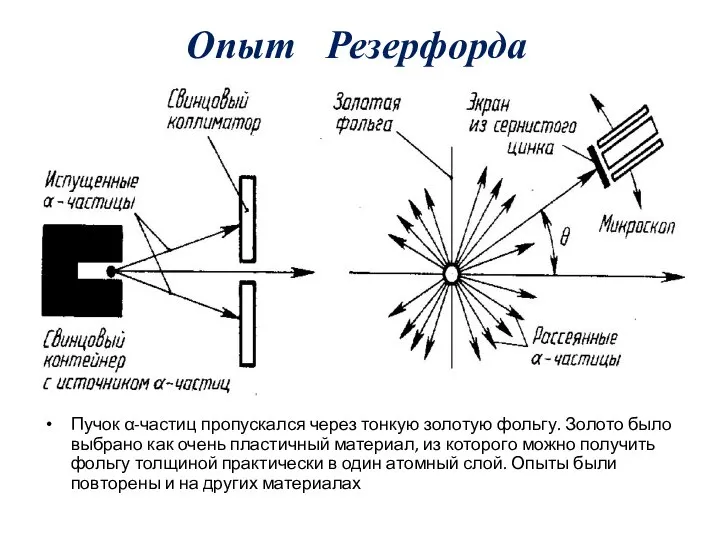
- 12. Опыт Резерфорда Пучок α-частиц пропускался через тонкую золотую фольгу. Золото было выбрано как очень пластичный материал,
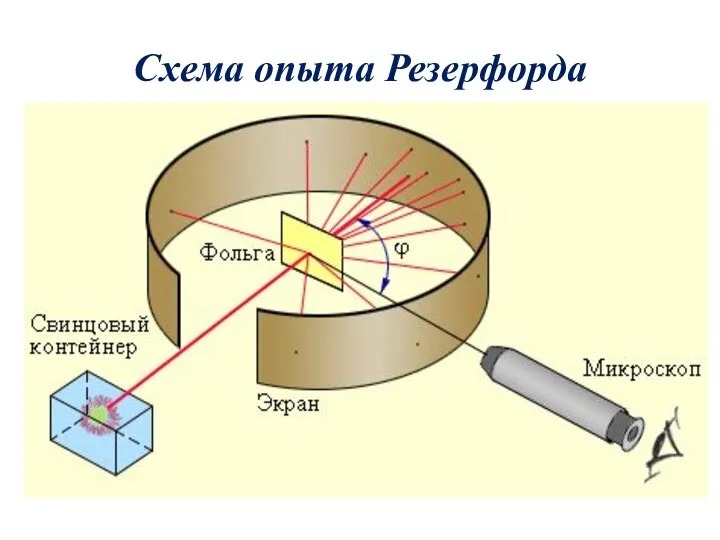
- 13. Схема опыта Резерфорда
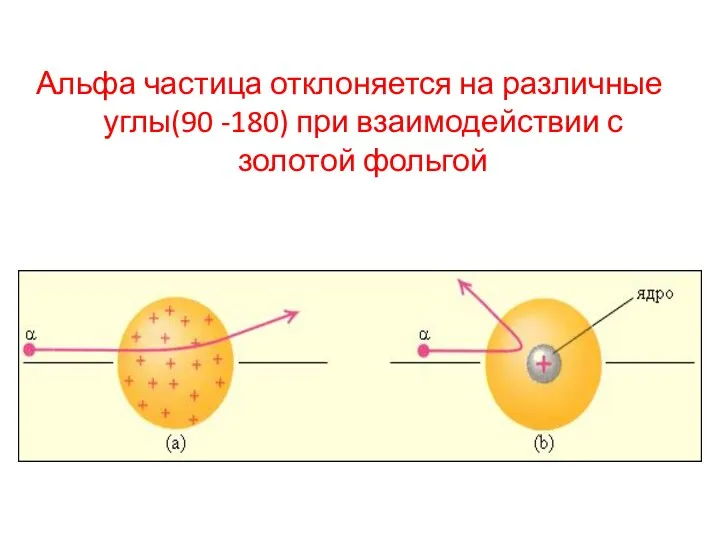
- 14. Альфа частица отклоняется на различные углы(90 -180) при взаимодействии с золотой фольгой
- 15. Выводы из опыта Резерфорда Э. Резерфорд и его помощники обнаружили, что какая-то часть α-частиц отклоняется на
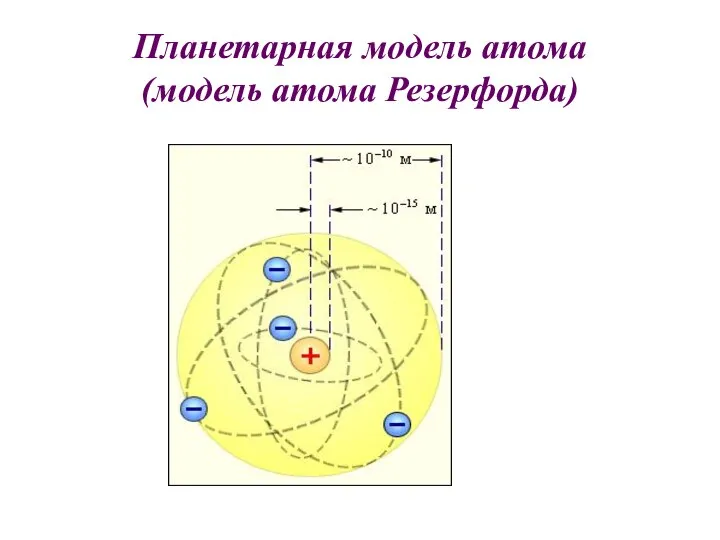
- 16. Планетарная модель атома (модель атома Резерфорда)
- 17. Недостатки планетарной модели Предложенная модель строения атома не позволила объяснить устойчивость атома: ускоренное движение электрона согласно
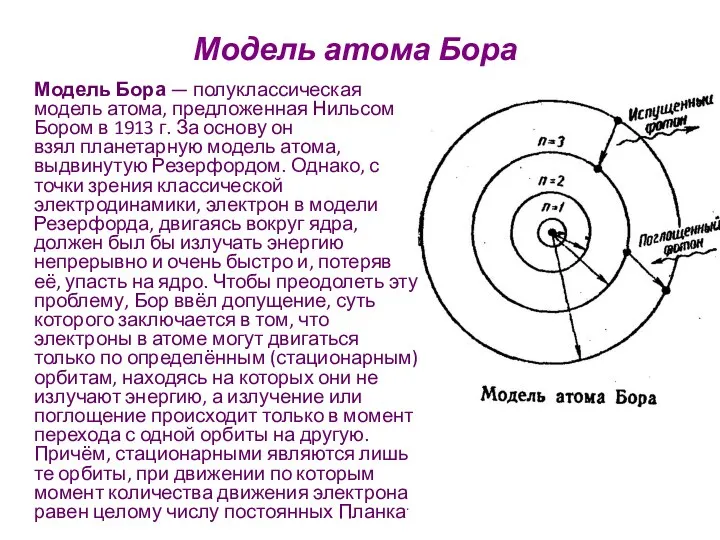
- 18. Модель атома Бора Модель Бора — полуклассическая модель атома, предложенная Нильсом Бором в 1913 г. За
- 20. Модель атома водорода по Бору Бор рассматривал простейшие круговые орбиты. - потенциальная энергия взаимодействия электрона с
- 22. ПОСТУЛАТЫ БОРА 1. Атомная система может находиться только в особых стационарных квантовых состояниях, каждому из которых
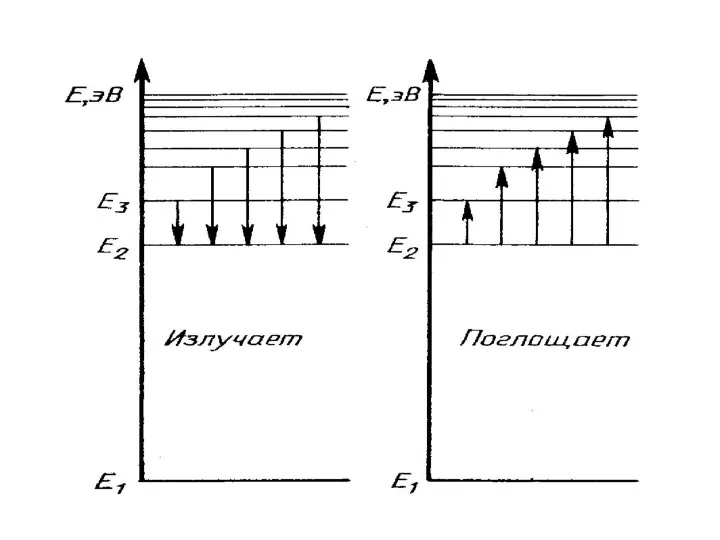
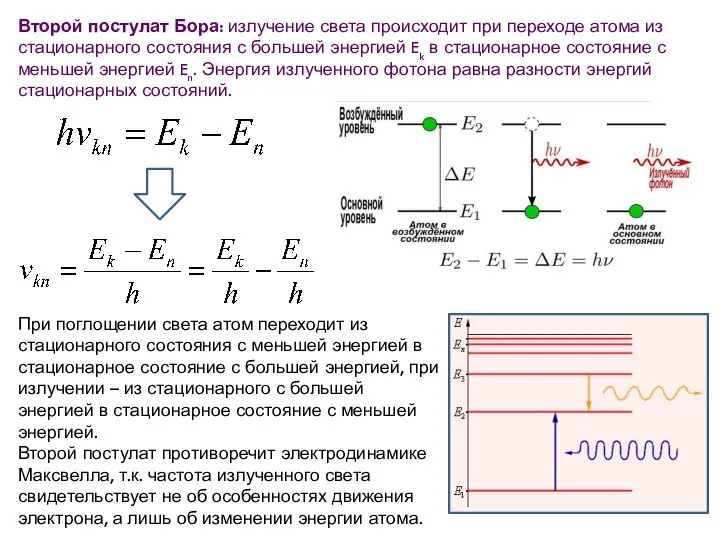
- 24. Второй постулат Бора: излучение света происходит при переходе атома из стационарного состояния с большей энергией Ek
- 25. Правило квантования Из первого постулата Бора энергия может принимать только определенное значение En. Электрон движется по
- 26. Правило квантования орбит: Электроны могут двигаться в атоме только по определённым орбитам, которые определяются условием: где
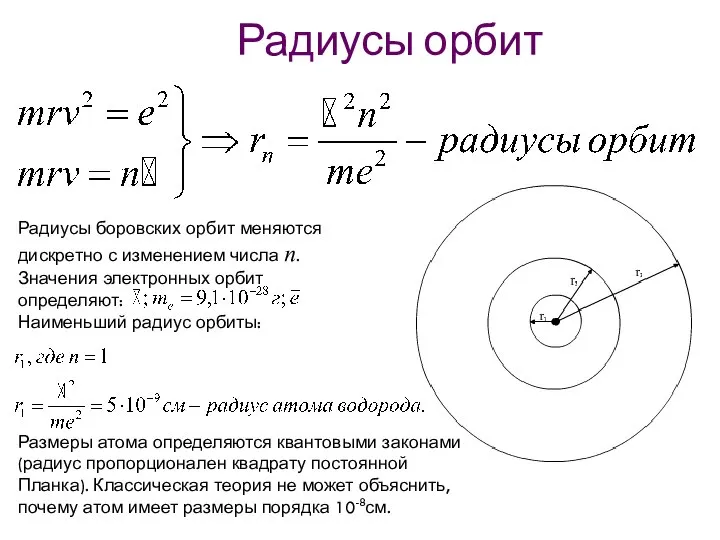
- 27. Радиусы орбит Радиусы боровских орбит меняются дискретно с изменением числа n. Значения электронных орбит определяют: Наименьший
- 28. Квантованные значения радиусов орбит:
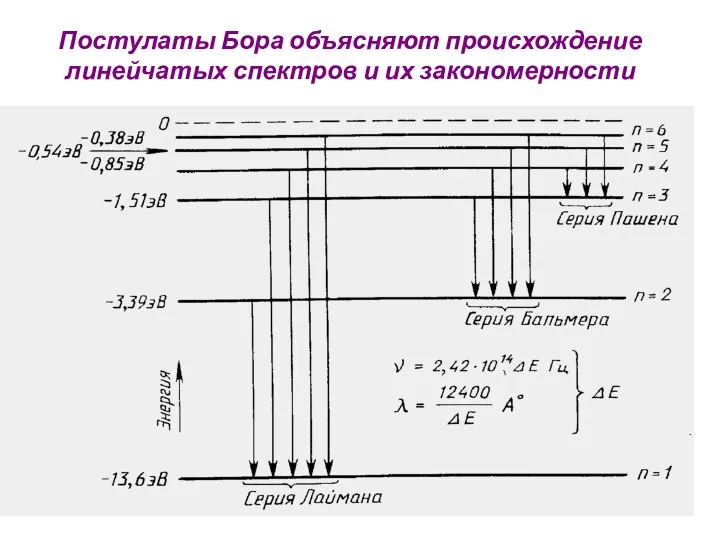
- 29. Постулаты Бора объясняют происхождение линейчатых спектров и их закономерности
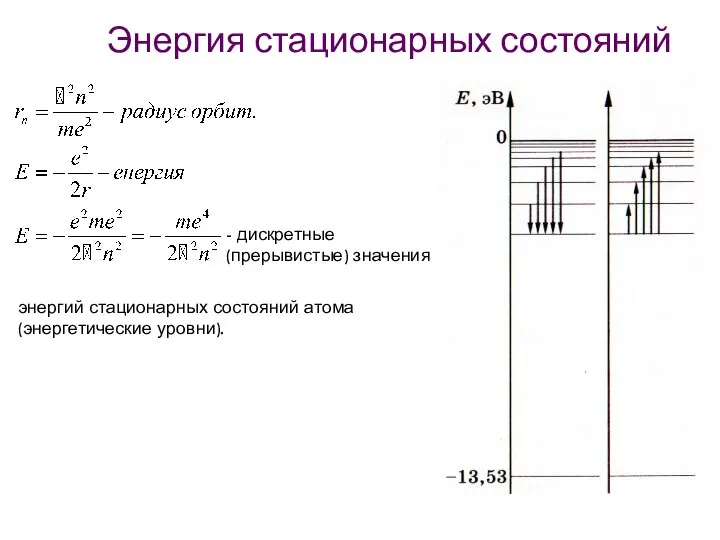
- 31. Энергия стационарных состояний - дискретные (прерывистые) значения энергий стационарных состояний атома (энергетические уровни).
- 32. Низшее энергетическое состояние Атом может находится сколь угодно долго. Чтобы ионизировать атом водорода, ему нужно сообщить
- 33. Излучение света Возможные частоты излучения атома водорода: где - постоянная Ридберга R = 109737,316 см-1. Теория
- 34. По второму постулату Бора возможные частоты излучения водорода равны: где R – постоянная Ридберга, равна 3,2*1015
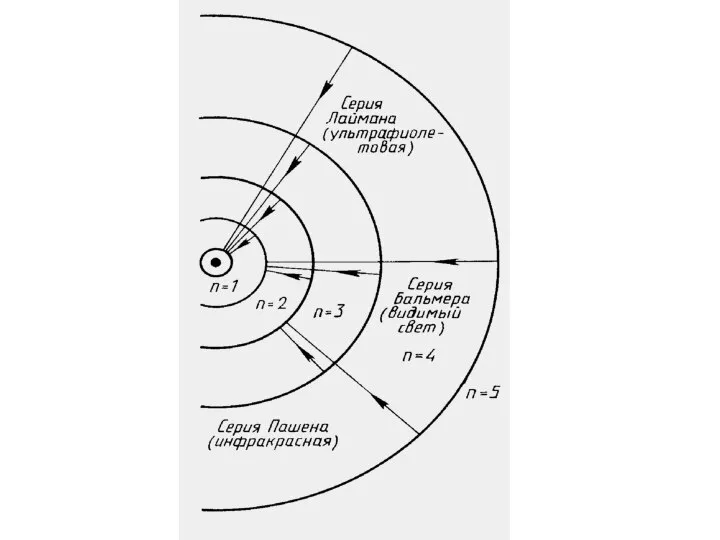
- 35. П = 3, 4, 5 и т.д., R= 3,2*1015 Гц Видимый свет И. Бальмер (1885г.)
- 36. Ультрафиолетовая серия Т. Лайман п= 2, 3, 4, 5 и т.д.
- 37. Инфракрасная серия Ф. Пашен п= 4, 5 и т.д.
- 39. Скачать презентацию









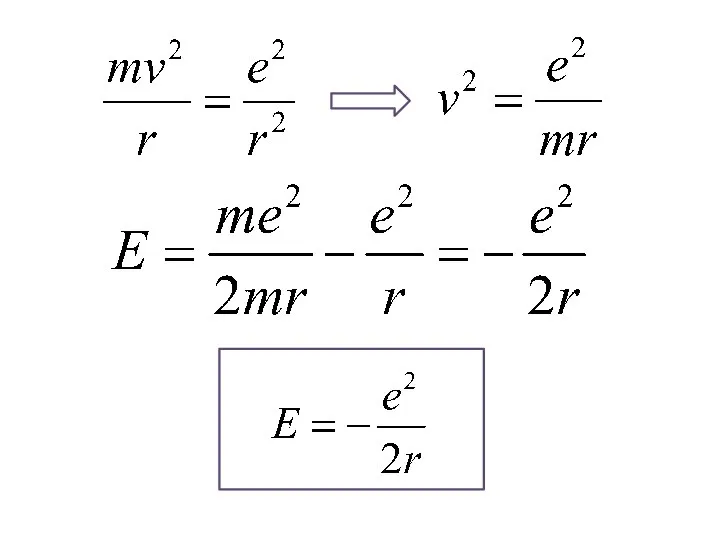










 Решение задач по теме Механические колебания и волны. Звук
Решение задач по теме Механические колебания и волны. Звук Электромагнитные колебания. Закрытый колебательный контур
Электромагнитные колебания. Закрытый колебательный контур Альтернативные источники энергии. Ветровые станции
Альтернативные источники энергии. Ветровые станции Истоирия создания реле. Вклад Дж.Генри
Истоирия создания реле. Вклад Дж.Генри Презентация по физике "Процесс многократного рассеяния" - скачать
Презентация по физике "Процесс многократного рассеяния" - скачать  Сергеева Л. Ф. Профессиональный лицей № 21 Г. Георгиевск
Сергеева Л. Ф. Профессиональный лицей № 21 Г. Георгиевск Задачи по физике
Задачи по физике Механическая работа. Единицы работы
Механическая работа. Единицы работы ВИХРЕВОЕ ЭЛЕКТРИЧЕСКОЕ ПОЛЕ
ВИХРЕВОЕ ЭЛЕКТРИЧЕСКОЕ ПОЛЕ  Приборы для измерения давления
Приборы для измерения давления Электрическая ёмкость проводника. Единица электроёмкости. Конденсатор. Ёмкость плоского конденсатора
Электрическая ёмкость проводника. Единица электроёмкости. Конденсатор. Ёмкость плоского конденсатора Электролиз. История создания. Применение
Электролиз. История создания. Применение Лекции по физике. Молекулярная физика и основы термодинамики
Лекции по физике. Молекулярная физика и основы термодинамики Аттестационная работа. Организация исследовательской деятельности обучающихся по физике Главное не табличка, а привычка
Аттестационная работа. Организация исследовательской деятельности обучающихся по физике Главное не табличка, а привычка Полное отражение света 11 класс - Презентация_
Полное отражение света 11 класс - Презентация_ Схемы электрических соединений на стороне 35 кВ и выше. (Лекция 13)
Схемы электрических соединений на стороне 35 кВ и выше. (Лекция 13) Презентация по физике "Ядерна зброя" - скачать бесплатно
Презентация по физике "Ядерна зброя" - скачать бесплатно Источники энергии. Тепловые двигатели
Источники энергии. Тепловые двигатели Ионные двигатели схемы Кауфмана, двигатели NSTAR, NEXT, NEXIS, T-6
Ионные двигатели схемы Кауфмана, двигатели NSTAR, NEXT, NEXIS, T-6 «Электродинамика» бөлімі бойынша оқу материалын қайталау, қорытындылау және жүйелеу
«Электродинамика» бөлімі бойынша оқу материалын қайталау, қорытындылау және жүйелеу Светотехнические величины
Светотехнические величины Презентация по физике "Путешествие по стране Электрония" - скачать
Презентация по физике "Путешествие по стране Электрония" - скачать  Физика ядерных реакторов
Физика ядерных реакторов Автор работы: Камскова Екатерина Автор работы: Камскова Екатерина МОУ СОШ №6, 9Б класс
Автор работы: Камскова Екатерина Автор работы: Камскова Екатерина МОУ СОШ №6, 9Б класс Элементы квантовой механики
Элементы квантовой механики Технологическая подготовка производства держателя измерителя для условий СНО Машиностроитель
Технологическая подготовка производства держателя измерителя для условий СНО Машиностроитель Презентация по физике "«Легенда о законе Архимеда»" - скачать
Презентация по физике "«Легенда о законе Архимеда»" - скачать  Закон сохранения энергии в механике
Закон сохранения энергии в механике