Содержание
- 2. 1. Квантовомеханическая картина строения атома Согласно квантовой механике, не существует определенных круговых орбит электронов. В силу
- 3. Электронное облако в основном состоянии водорода сферически-симметрично Электронное облако грубо характеризует «размеры» атома Квантовая механика утверждает,
- 4. Электронное облако можно интерпретировать как с корпускулярной, так и с волновой точки зрения. Размытое в пространстве
- 5. Не возможно предсказать траектории, по которым будет двигаться электрон Можно вычислить вероятность обнаружить электрон в различных
- 6. Потенциальная энергия взаимодействия электрона с ядром, обладающим зарядом Ze (для атома водорода Z=1) где r –
- 7. Состояние электрона в атоме водорода описывается волновой функцией Ψ, удовлетворяющей стационарному уравнению Шредингера: E – полная
- 8. Решение уравнения Шредингера для атома водорода приводит к появлению дискретных энергетических уровней: При E E1, (n
- 9. Итак, если Бору пришлось вводить дополнительные гипотезы (постулаты), то в квантовой механике дискретные значения энергии, являясь
- 10. Квантовые числа В квантовой механике доказывается, что уравнению Шредингера удовлетворяют собственные функции , определяемые тремя квантовыми
- 11. Главное квантовое число n характеризует расстояние электрона от ядра – радиус орбиты. В атомной физике состояния
- 12. Состояния, соответствующие орбитальному числу l = 0, 1, 2, 3,…, также обозначаются буквами s, p, d,
- 13. Квадрат модуля функции характеризует вероятность найти электрон в заданной точке. Область пространства, в которой высока вероятность
- 15. Орбитали часто называют подоболочками оболочек, поскольку они характеризуют формы разных орбит, на которых можно обнаружить электроны,
- 16. Для электрона в потенциальном поле Стационарное уравнение Шредингера Уравнение имеет решение при всех значениях E >
- 17. В квантовой механике широко используется понятие – оператор. Под оператором понимают правило, посредством которого одной функции
- 18. С помощью оператора стационарное уравнение Шредингера можно записать в виде Здесь – оператор энергии. Это традиционный
- 19. и три оператора проекций момента импульса на оси координат Воздействуя на Ψ – функцию оператором момента
- 20. Собственное значение орбитального момента импульса электрона Le l – орбитальное квантовое число (l = 0, 1,
- 21. 2. Пространственное квантование (магнитное квантовое число) Известно, что орбитальный момент импульса электрона и пропорциональный ему магнитный
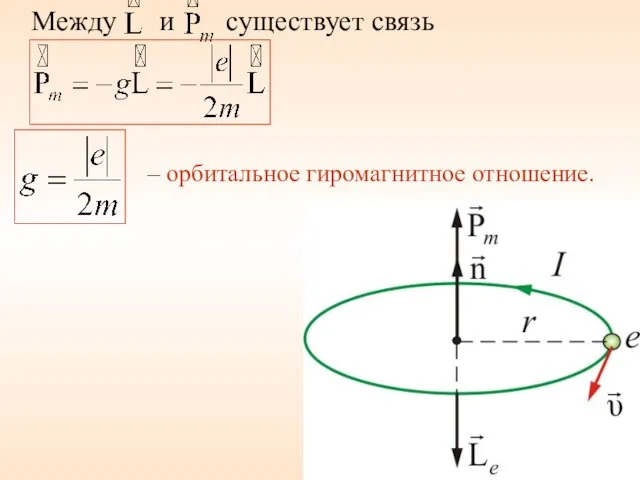
- 22. Между и существует связь – орбитальное гиромагнитное отношение.
- 23. Для задания ориентации L и Pm должно быть выбрано некоторое направление в пространстве. За указанное направление
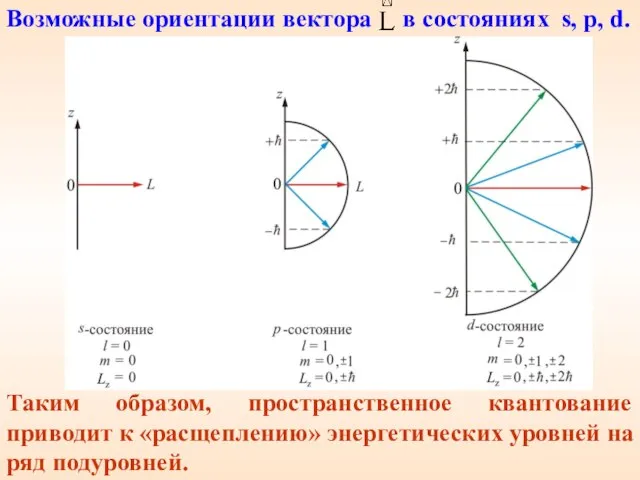
- 24. В квантовой механике строго доказывается (это следует из решения уравнения Шредингера), что проекция (Lz) вектора L
- 25. Таким образом, пространственное квантование приводит к «расщеплению» энергетических уровней на ряд подуровней. Возможные ориентации вектора в
- 26. Расщепление энергетических уровней в магнитном поле было обнаружено в 1896 г. голландским физиком П. Зееманом и
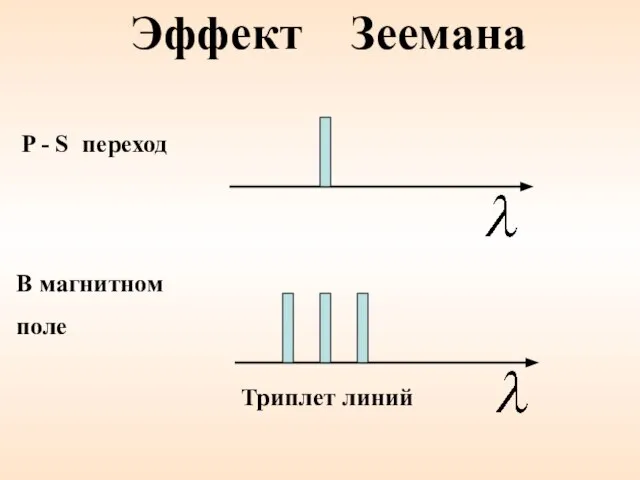
- 27. Эффект Зеемана В магнитном поле P - S переход Триплет линий
- 28. Вектор индукции магнитного поля В Возможные ориентации вектора орбитального магнитного момента (для орбиты с l =
- 29. 3. Опыт Штерна и Герлаха В 1922 году Штерн и Герлах поставили опыты, целью которых было
- 30. Идея опыта заключалась в измерении силы, действующей на атом в сильно - неоднородном магнитном поле. Неоднородность
- 31. В колбе вакуум 10–5 мм. рт. ст., К – серебреный шарик, который нагревался до температуры испарения.
- 32. Если бы момент импульса атома (и его магнитный момент ) мог принимать произвольные ориентации в пространстве,
- 33. Этим доказывался квантовый характер магнитных моментов электронов. Количественный анализ показал, что проекция магнитного момента электрона равна
- 34. Опыты Штерна и Герлаха не только подтвердили пространственное квантование моментов импульсов в магнитном поле, но и
- 35. Кроме того, в этих опытах было обнаружено новое явление. Валентный электрон в основном состоянии атома серебра
- 36. В 1925 г. студенты Геттингенского университета Гаудсмит и Уленбек предложили существование собственного механического момента импульса у
- 37. Спин электрона S Собственный магнитный момент электрона
- 38. S –спиновое квантовое число. Авторы дали такое толкование спина: электрон вращающийся волчок. Но тогда следует, что
- 39. Аналогично, проекция спина на ось z (LSz) (ось z совпадает с направлением внешнего магнитного поля) должна
- 40. Для атомов первой группы, валентный электрон которых находится в s – состоянии (l = 0) момент
- 41. Численное значение спина электрона По аналогии с пространственным квантованием орбитального момента (L) проекция LSz = mSħ,
- 42. Таким образом: 1. Магнитное спиновое квантовое число ms может принимать два значения. 2. Спиновое квантовое число
- 43. Проекция магнитного момента электрона на направление внешнего поля: (часто говорят о собственном магнитном моменте электрона) Отношение
- 46. 4. Принципы неразличимости тождественных частиц. Фермионы и бозоны Пусть квантовомеханическая система состоит из одинаковых частиц, например
- 47. Из соотношения неопределенности вытекает, что для микрочастиц вообще не применимо понятие траектории; состояние микрочастицы описывается волновой
- 48. где x1 и x2 – соответственно совокупность пространственных и силовых координат первой и второй частиц. Из
- 49. Установлено, частицы с полуцелым спином (например, электроны, нейтроны и протоны) описываются антисимметричными волновыми функциями и подчиняются
- 50. ПАУЛИ Вольфганг (1900 – 1958)–немецкийфизик-теоретик. Работы относятся ко многим разделам современной теоретической физики, в развитии которых
- 51. 5. Принципы Паули. Распределение электронов в атоме по состояниям В. Паули сформулировал принцип, согласно которому системы
- 52. Состояние электрона в атоме однозначно определяется набором четырех квантовых чисел: Главного n (n = K, L,
- 53. Распределение электронов в атоме происходит по принципу Паули: в одном и том же атоме, не может
- 54. Максимальное число Z2 (n, l, ms) электронов, находящихся в состояниях, описываемых набором трех квантовых чисел n,
- 55. Совокупность электронов в многоэлектронном атоме, имеющих одно и то же главное квантовое число n, называется электронной
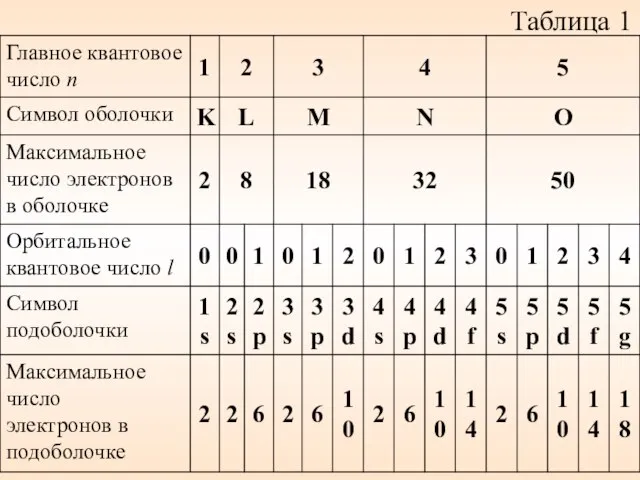
- 56. Область пространства, в которой высока вероятность обнаружить электрон (не менее 0,95), называют подоболочкой или орбиталью. Основные
- 57. Таблица 1
- 58. 6. Периодическая система элементов Д. И. Менделеева В начале XIX в., с развитием идей химической атомистики
- 60. 114 Discovered at JINR in 1999 115 Discovered at JINR in 2003 118 Discovered at JINR
- 61. Физический смысл порядкового номера Z элемента периодической системы Менделеева был выяснен в ядерной модели атома Резерфорда.
- 62. Теория периодической системы основывается на следующих положениях: общее число электронов в атоме данного химического элемента равно
- 63. Система электронов, построенная на таких основах, должна иметь структуру и число элементов в одном периоде (длину
- 65. Z = 1 (водород, Н). Единственный электрон атома водорода находится в состоянии 1s, характеризуемом квантовыми числами
- 66. Z = 3 (литий, Li). Третий электрон атома лития, согласно принципу Паули, уже не может разместиться
- 67. Z = 11 (натрий, Na). Одиннадцатый элемент натрий размещается в M оболочке (n = 3), занимая
- 68. Z = 19 (калий, K). Калий должен был бы занять 3d-состояние в M-оболочке. Однако и в
- 69. Это означает, что в результате взаимодействия электронов состояния n = 4, l = 0 имеет меньшую
- 70. Каждую из двух групп элементов – лантаноиды (Z = 57 (лантан, La) до Z = 71
- 72. Скачать презентацию

































































 Радиационная биофизика
Радиационная биофизика Трение. Силы трения
Трение. Силы трения Динамика материальной точки
Динамика материальной точки Структура и спектрально-люминесцентные характеристики керамики Y2O3:Er
Структура и спектрально-люминесцентные характеристики керамики Y2O3:Er Намагничивание магнетиков. Классификация магнетиков
Намагничивание магнетиков. Классификация магнетиков Механическая энергия. Закон сохранения энергии
Механическая энергия. Закон сохранения энергии Қатты денелерден зарядталған бөлшектерді шығару əдістері (эмиссия)
Қатты денелерден зарядталған бөлшектерді шығару əдістері (эмиссия) Воздухоплавание Учитель физики ГБОУ СОШ № 128 г.Санкт-Петербург Андронова Екатерина Вл
Воздухоплавание Учитель физики ГБОУ СОШ № 128 г.Санкт-Петербург Андронова Екатерина Вл Механические колебания и волны. Звук
Механические колебания и волны. Звук Поперечные и продольные волны
Поперечные и продольные волны Fast and Simple Physics using Sequential Impulses
Fast and Simple Physics using Sequential Impulses Двигатель внутреннего сгорания. Паровая турбина
Двигатель внутреннего сгорания. Паровая турбина Рух в природі та основа відліку часу
Рух в природі та основа відліку часу Брейн-ринг Юные знатоки физики
Брейн-ринг Юные знатоки физики Альфа-, бета- и гамма-излучение. Радиоактивность
Альфа-, бета- и гамма-излучение. Радиоактивность Основы гидродинамического подобия
Основы гидродинамического подобия Интерференция - презентация_
Интерференция - презентация_ Единицы измерения энергии
Единицы измерения энергии Физика Нового времени
Физика Нового времени Электростатика. Диэлектрики. Диэлектрическая поляризация. (Лекция 3)
Электростатика. Диэлектрики. Диэлектрическая поляризация. (Лекция 3) ГИА тренировочные задания № 24 и 25 МОСКВА 2010 ЭКСМО Диагностика 2013
ГИА тренировочные задания № 24 и 25 МОСКВА 2010 ЭКСМО Диагностика 2013 Оптика. Подготовка к ЕГЭ
Оптика. Подготовка к ЕГЭ Основной закон электростатики. Закон Кулона
Основной закон электростатики. Закон Кулона Аттестационная работа. Программа курса по выбору Мои открытия. (7 класс)
Аттестационная работа. Программа курса по выбору Мои открытия. (7 класс) Презентация по физике "Припливні електростанції (ПЕС)" - скачать бесплатно
Презентация по физике "Припливні електростанції (ПЕС)" - скачать бесплатно Электрическое поле. Напряжённость электрического поля
Электрическое поле. Напряжённость электрического поля Structures of water-soluble globular proteins
Structures of water-soluble globular proteins Курс физики. Введение
Курс физики. Введение