Содержание
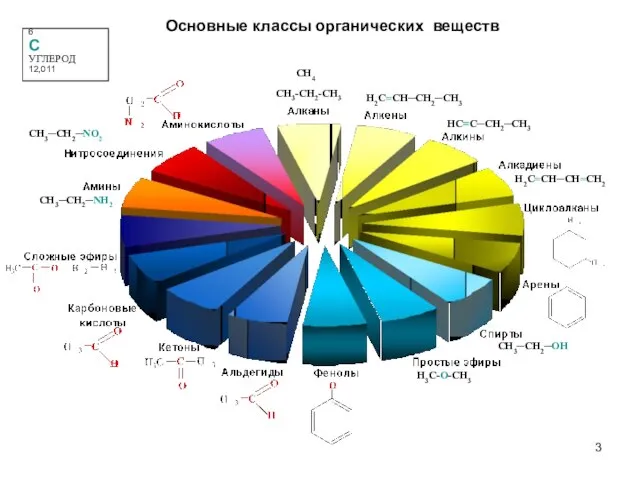
- 3. H3C-O-CH3 CH3-CH2-CH3 6 C УГЛЕРОД 12,011 Основные классы органических веществ H2C=CH─CH2─CH3 HC≡C─CH2─CH3 H2C=CH─CH=CH2 CH3─CH2─OH CH3─CH2─NH2 CH3─CH2─NO2
- 4. Состав УМК Программа 10-11 класс (с учетом последних требований к программам) Учебник 10 класса Учебник 11
- 5. Учебник 10 класса Введение в курс органической химии Алканы Непредельные УВ и циклоалканы Ароматические углеводороды Галогенпроизводные
- 6. Учебник 10 класса Карбоновые кислоты Углеводы Амины Аминокислоты. Белки Гетероциклические соединения. НК * Теоретические основы курса
- 7. Учебник 11 класса Глава 1. Строение вещества Глава 2. Основы теории химических процессов Глава 3. Растворы.
- 8. Учебник 11 класса Глава 6. Неметаллы Глава 7. Металлы Глава 8. Стехиометрические и газовые законы в
- 9. Свойства веществ определяются их строением и наоборот, зная строение, можно прогнозировать свойства Состав Строение Свойства 1861
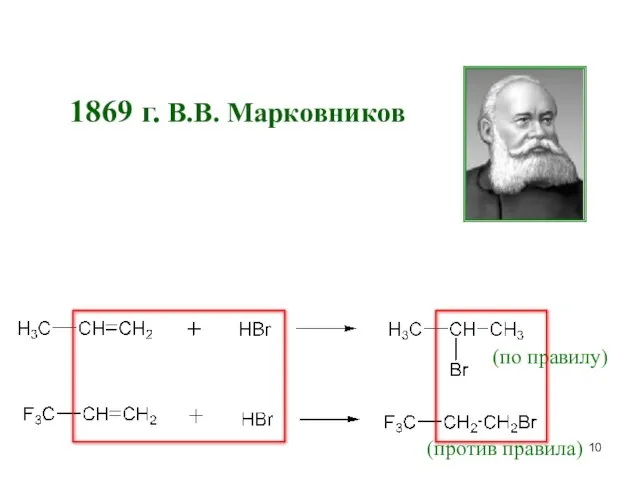
- 10. 1869 г. В.В. Марковников (по правилу) (против правила)
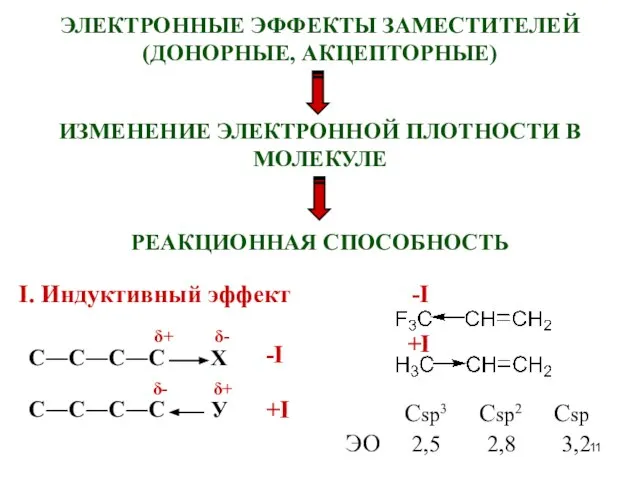
- 11. ЭЛЕКТРОННЫЕ ЭФФЕКТЫ ЗАМЕСТИТЕЛЕЙ (ДОНОРНЫЕ, АКЦЕПТОРНЫЕ) ИЗМЕНЕНИЕ ЭЛЕКТРОННОЙ ПЛОТНОСТИ В МОЛЕКУЛЕ РЕАКЦИОННАЯ СПОСОБНОСТЬ Сsp3 Csp2 Csp ЭО
- 12. II. Эффект сопряжения (мезомерный эффект, ± М) а) π-π-сопряжение б) р-π-сопряжение Бутадиен-1,3 бензол +М +М фенол
- 13. ЭЛЕКТРОННАЯ ИНТЕРПРЕТАЦИЯ ПРАВИЛА МАРКОВНИКОВА 1 а) б) а) б) AdE ?
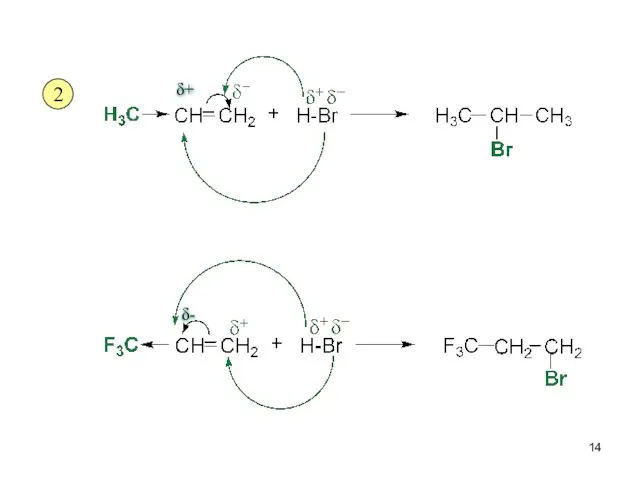
- 14. 2 δ+ δ-
- 15. радикал аллильного типа Радикальное замещение в алкенах SR (реакция Львова)
- 16. Глава 4. Ароматические углеводороды § 36. Бензол. История открытия 18 июня 1825 г. С H 6
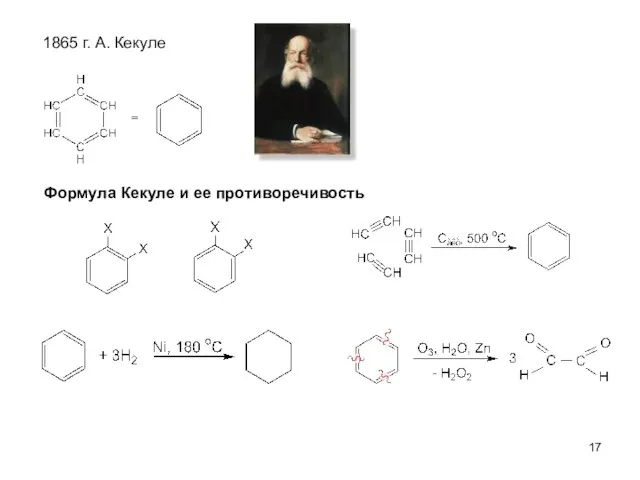
- 17. 1865 г. А. Кекуле Формула Кекуле и ее противоречивость
- 18. ОСНОВНЫЕ ВЫВОДЫ 1.Бензол (С6Н6) – жидкость, огнеопасная и токсичная, с характерным запахом. 2.Структурная формула бензола, предложенная
- 19. § 37. Электронное и пространственное строение бензола. Изомерия и номенклатура гомологов бензола
- 20. §39. Химические свойства бензола §40. Ориентационные эффекты заместителей §41 . Получение аренов § 42. Особенности химических
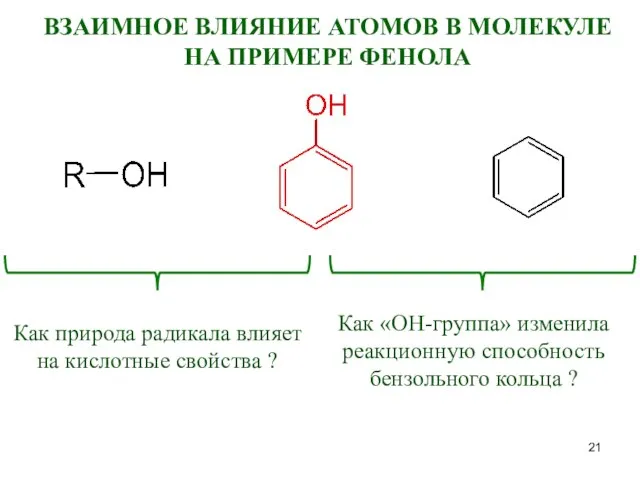
- 21. ВЗАИМНОЕ ВЛИЯНИЕ АТОМОВ В МОЛЕКУЛЕ НА ПРИМЕРЕ ФЕНОЛА Как природа радикала влияет на кислотные свойства ?
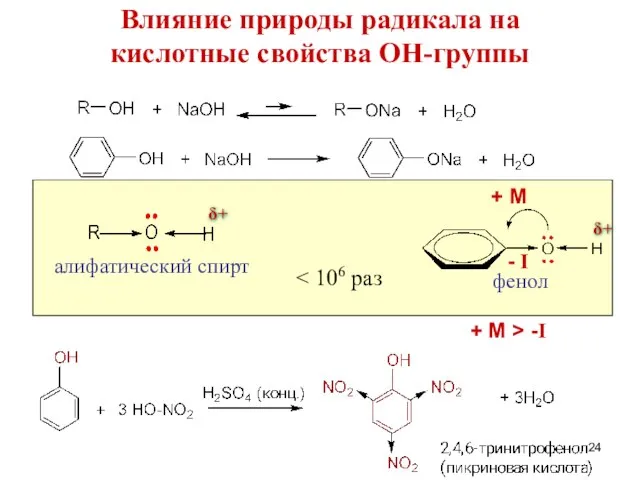
- 22. Влияние природы радикала на кислотные свойства ОН-группы фенол алифатический спирт + М - I δ+ δ+
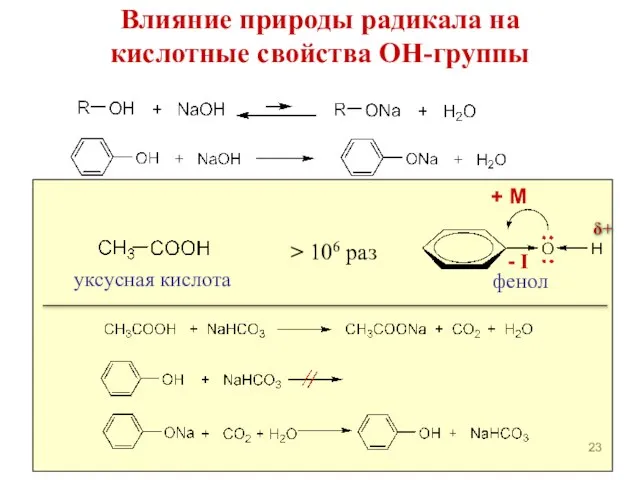
- 23. Влияние природы радикала на кислотные свойства ОН-группы фенол уксусная кислота > 106 раз + М -
- 24. Влияние природы радикала на кислотные свойства ОН-группы фенол алифатический спирт + М - I + М
- 25. бромбензол Влияние ОН-группы на реакционную способность бензольного кольца в реакциях SE I. II.
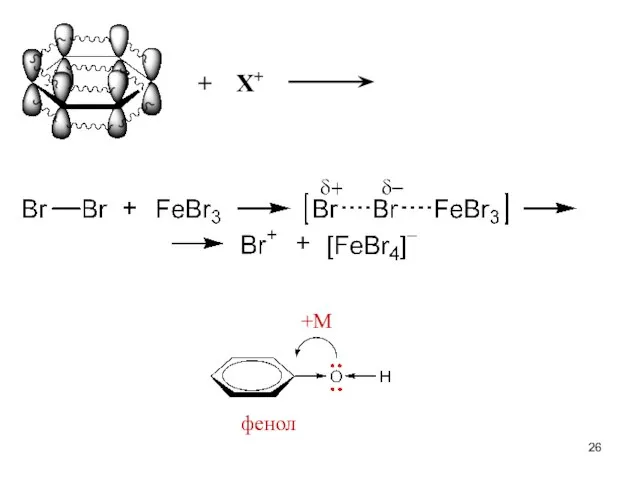
- 26. +М фенол + Х+
- 27. Кислотные свойства спиртов и фенолов фенол алифатический спирт + М - I + М > -I
- 28. ? С6Н12О6 Глюкоза – пятиатомный альдегидоспирт
- 30. ВМЕСТО ЭПИЛОГА
- 31. Цель: помощь в профориентации, готовность к адаптации, постоянному самообразованию. Что способствует реализации этой цели? Формирование значимых
- 37. Скачать презентацию

























 Химический элемент алюминий
Химический элемент алюминий Соли. Классификация
Соли. Классификация Углеводы (сахариды)
Углеводы (сахариды) Физические и химические явления
Физические и химические явления Гидроксилпроизводные углеводородов
Гидроксилпроизводные углеводородов Декарбонизаторы. Декарбонизация
Декарбонизаторы. Декарбонизация Определение понятия сплавов. Сплавы на основе железа и меди
Определение понятия сплавов. Сплавы на основе железа и меди Функциональные производные карбоновых кислот
Функциональные производные карбоновых кислот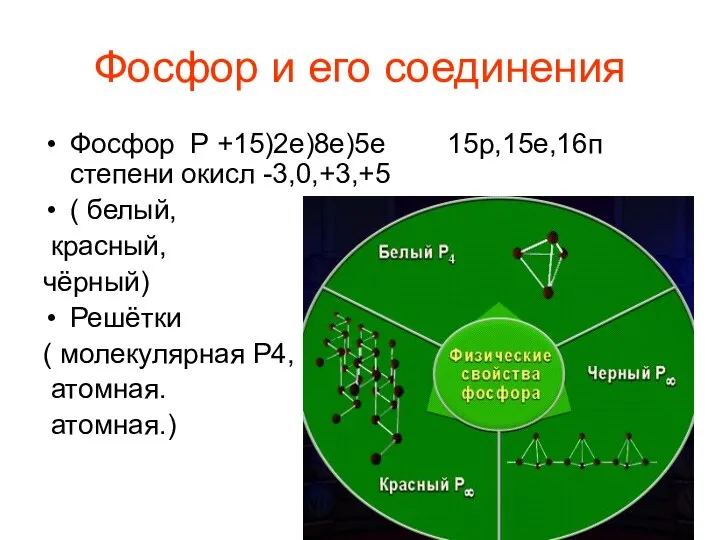 Фосфор и его соединения Фосфор Р +15)2е)8е)5е 15р,15е,16п степени окисл -3,0,+3,+5 ( белый, красный, чёрный) Решётки ( молекулярная Р4,
Фосфор и его соединения Фосфор Р +15)2е)8е)5е 15р,15е,16п степени окисл -3,0,+3,+5 ( белый, красный, чёрный) Решётки ( молекулярная Р4,  Периодический закон Д.И. Менделеева
Периодический закон Д.И. Менделеева Задача №9. Глицерин. Команда «Карбораны»
Задача №9. Глицерин. Команда «Карбораны» Сложные эфиры Урок химии в 10 классе
Сложные эфиры Урок химии в 10 классе The phenomenon of radioactivity. Radioisotopes. The nuclear reaction
The phenomenon of radioactivity. Radioisotopes. The nuclear reaction Геометрия молекул
Геометрия молекул Алкены. Пропилен
Алкены. Пропилен Электрохимические анализаторы медицинского назначения
Электрохимические анализаторы медицинского назначения Технология оптического стекла
Технология оптического стекла Лактоза
Лактоза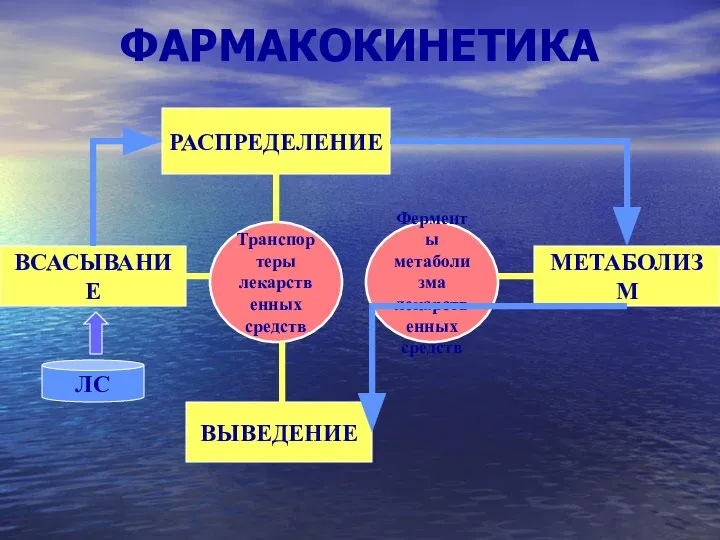 Фармакокинетика
Фармакокинетика Презентацию составила учитель МОУ «Ягринская гимназия» г.Северодвинска Шапошникова Т.С.
Презентацию составила учитель МОУ «Ягринская гимназия» г.Северодвинска Шапошникова Т.С.  Оксиды углероды
Оксиды углероды Рідкі кристали
Рідкі кристали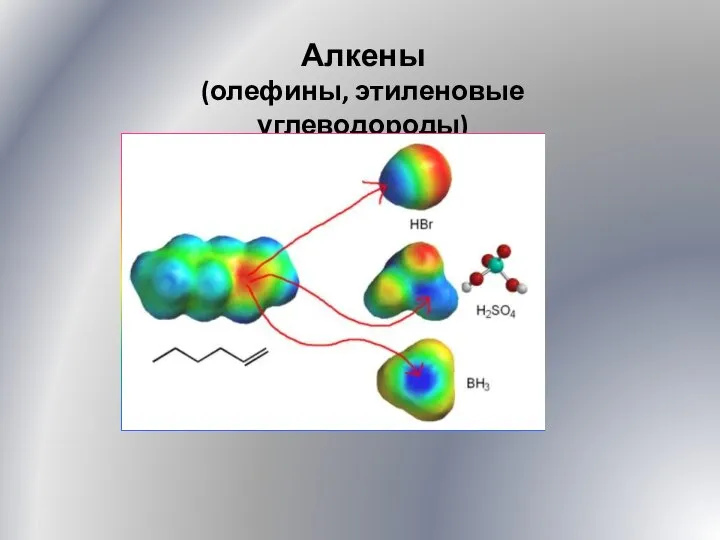 Алкены. Олефины, этиленовые углеводороды. (Лекция 5)
Алкены. Олефины, этиленовые углеводороды. (Лекция 5) Протолитическая теория кислот и оснований
Протолитическая теория кислот и оснований Натуральный комплекс минералов
Натуральный комплекс минералов Алюминий и его соединения
Алюминий и его соединения Введение в общую химию. Основные понятия химии
Введение в общую химию. Основные понятия химии Химия морской воды
Химия морской воды