Содержание
- 2. Запишем уравнение обратимости в общем виде: В ходе экспериментальных наблюдений установлено, что скорость химической реакции в
- 3. Уравнение (13) можно записать в другой форме и получить выражение для константы равновесия (К): В реальных
- 4. Применение кислотно-основных реакций в аналитической химии Кислотно-основные аналитические реакции делятся на: 1) Кислотно-основное взаимодействие в чистом
- 5. Кислотно-основное взаимодействие в чистом растворителе можно представить следующим образом: , или в сокращенной форме: , ,
- 6. Величина K очень мала, что говорит о том, что H2O очень слабый электролит, плохо диссоциирует на
- 7. (9) (10) (11) (12) (13) , ,
- 8. Умножим правую и левую части уравнения (13) на (-1) При 25 oC Для чистой воды и
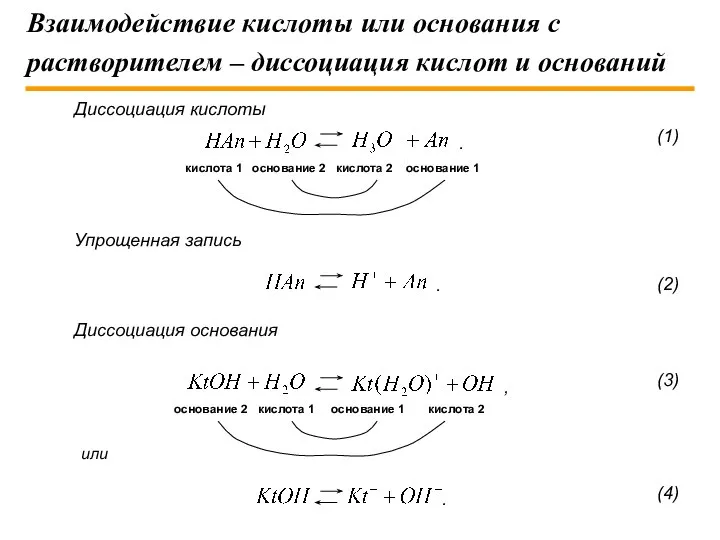
- 9. Взаимодействие кислоты или основания с растворителем – диссоциация кислот и оснований Диссоциация кислоты Упрощенная запись Диссоциация
- 10. Приведенные выше равновесия в системе кислота – растворитель, основание – растворитель описываются константами равновесия, называемыми константами
- 11. Вычисление рН растворов кислот, оснований в связи с их диссоциацией Сильные электролиты Слабые электролиты где С
- 12. Сильные электролиты Слабые электролиты Если кислота является очень слабой, то [H+] ( [An-] ) гораздо меньше
- 14. Скачать презентацию









![Сильные электролиты Слабые электролиты Если кислота является очень слабой, то [H+]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1404844/slide-11.jpg)
 Кристаллофизика, кристаллохимия
Кристаллофизика, кристаллохимия Массовая доля элемента в веществе
Массовая доля элемента в веществе Ферросплавы. Феррохром
Ферросплавы. Феррохром Курс «Неорганическая химия» Лектор: Третьяков Юрий Дмитриевич Расписание лекций: вторник – 10:50 – 12:25 пятни
Курс «Неорганическая химия» Лектор: Третьяков Юрий Дмитриевич Расписание лекций: вторник – 10:50 – 12:25 пятни Урок :Углерод (9 класс) Автор:Ахметвалиева НаиляМисбаховна , учитель химии ГБОУ ООШ п.Приморский м.р.Ставропольский Самарской области Углерод Углеро́д — химический элемент 4-ой группы главной подгруппы 2-го периода периодической системы Менделеева, по
Урок :Углерод (9 класс) Автор:Ахметвалиева НаиляМисбаховна , учитель химии ГБОУ ООШ п.Приморский м.р.Ставропольский Самарской области Углерод Углеро́д — химический элемент 4-ой группы главной подгруппы 2-го периода периодической системы Менделеева, по Шкала рН
Шкала рН Медицинская биохимия как наука. Вводная лекция
Медицинская биохимия как наука. Вводная лекция Формирование УУД на уроках химии
Формирование УУД на уроках химии Предмет и задачи биохимии. Ферменты, энзимы. (Лекция 2)
Предмет и задачи биохимии. Ферменты, энзимы. (Лекция 2) Непредельные углеводороды. (Лекция 6)
Непредельные углеводороды. (Лекция 6) Круговорот углерода в природе. Изготовлено: А.С.Большаков
Круговорот углерода в природе. Изготовлено: А.С.Большаков Производные ксантина (дипрофиллин, ксантинола никотинат, пентоксифиллин) и гедантоина (фенитоин)
Производные ксантина (дипрофиллин, ксантинола никотинат, пентоксифиллин) и гедантоина (фенитоин) Методические рекомендации по изучению темы «Азот как простое вещество»
Методические рекомендации по изучению темы «Азот как простое вещество» Химические реакции. Тепловой эффект
Химические реакции. Тепловой эффект Двойной электрический слой (ДЭС)
Двойной электрический слой (ДЭС) Глюкоза. Будова глюкози та її властивості
Глюкоза. Будова глюкози та її властивості Общие способы получения металлов
Общие способы получения металлов Алюминий. История получения. Свойства алюминия. Корунд, бокситы
Алюминий. История получения. Свойства алюминия. Корунд, бокситы Химическая связь в кристаллах
Химическая связь в кристаллах Химический состав яблока
Химический состав яблока Дисперсные системы
Дисперсные системы Ағзалар мен биосұйықтар минерализатындағы металдық улар
Ағзалар мен биосұйықтар минерализатындағы металдық улар Взаимодействие галогенов с водородом
Взаимодействие галогенов с водородом Коллекция учебных динамических слайдов по химии (8 класс)
Коллекция учебных динамических слайдов по химии (8 класс) Строение атома алюминия. Физические и химические свойства алюминия
Строение атома алюминия. Физические и химические свойства алюминия Боевые отравляющие вещества
Боевые отравляющие вещества Переводной экзамен по химии «Качественные реакции в органической химии» Толмачевой Кати 11а
Переводной экзамен по химии «Качественные реакции в органической химии» Толмачевой Кати 11а Гума
Гума