Биологическое окисление 2. Оксигеназные, пероксидазные и радикальные пути использования кислорода. (Лекция 5)
Содержание
- 2. план Оксигеназные реакции Монооксигеназные реакции Диоксигеназные реакции. Радикальные и пероксидазные реакции
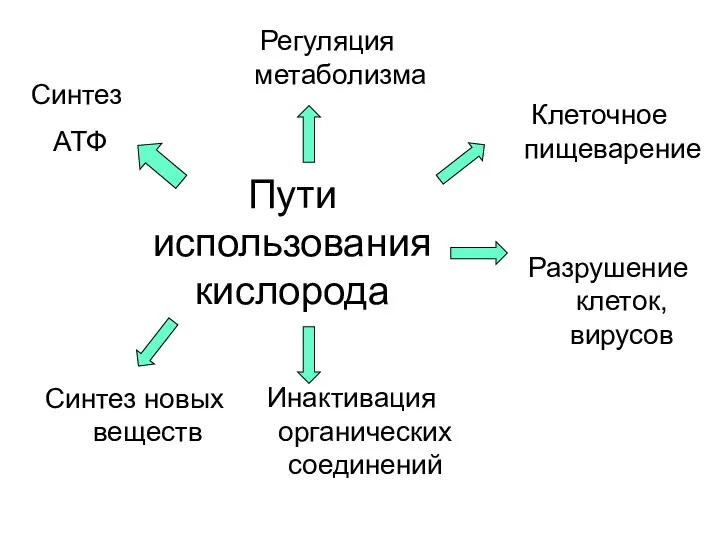
- 3. Пути использования кислорода Синтез АТФ Синтез новых веществ Инактивация органических соединений Разрушение клеток, вирусов Клеточное пищеварение
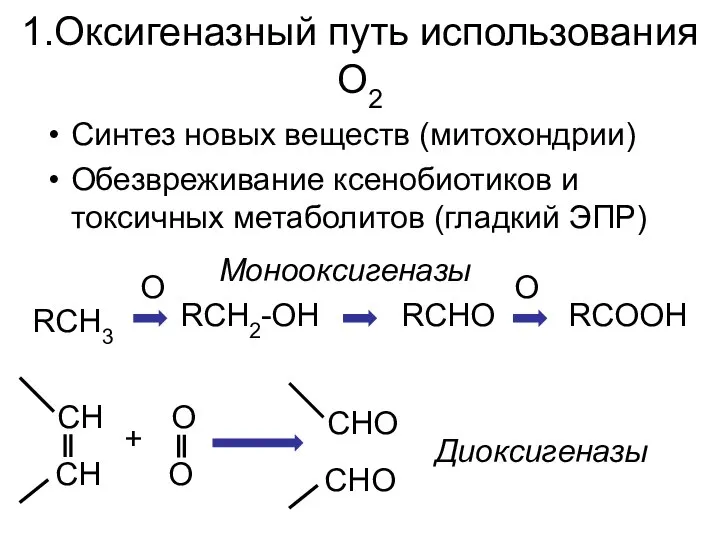
- 4. 1.Оксигеназный путь использования О2 Синтез новых веществ (митохондрии) Обезвреживание ксенобиотиков и токсичных метаболитов (гладкий ЭПР) RCH3
- 5. Ксенобиотики – чужеродные для организма вещества, которые он не может использовать для собственных нужд. Полезные –
- 6. химические элементы (ртуть, свинец, кадмий, др.); радионуклиды; Пестициды; нитраты, нитриты и нитрозосоединения; вещества, применяемые в животноводстве;
- 7. Биотрансформация Биотрансформация (Bios - жизнь, transformatio - превращение, видоизменение) - совокупность химических превращений ксенобиотиков (xenos -
- 8. Локализация биотрансформации 90-95% всех чужеродных липофильных веществ подвергается биотрансформации в гладком эндоплазматическом ретикулуме клеток печени. 5-10%
- 9. Виды биотрансформации Метаболическая трансформация Реакции - окисления - восстановления - гидролиза образуются функциональные группы -ОН, -СООН,
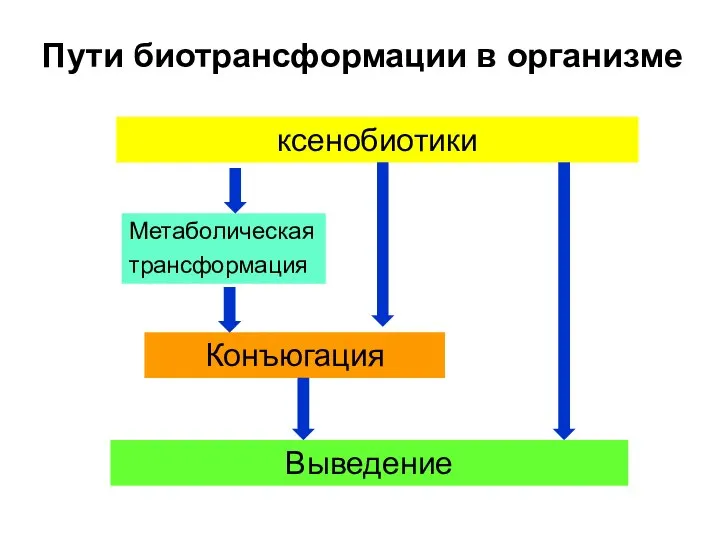
- 10. Пути биотрансформации в организме Метаболическая трансформация ксенобиотики Конъюгация Выведение
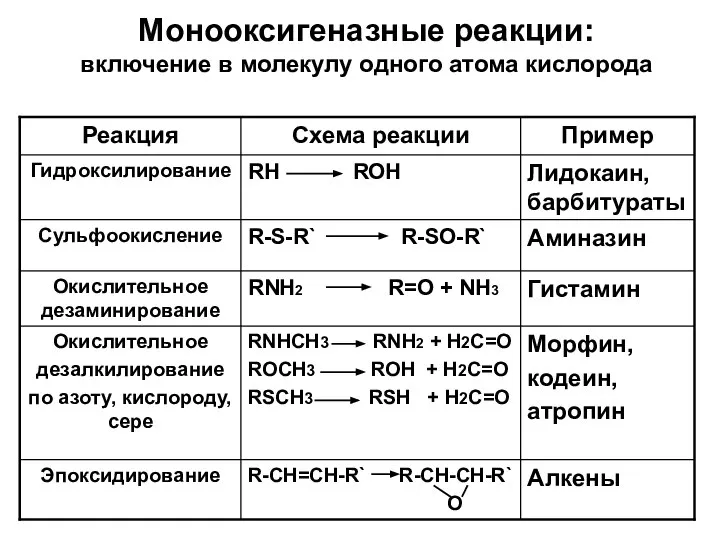
- 11. Монооксигеназные реакции: включение в молекулу одного атома кислорода
- 12. А. Цепь НАДФН2-Р450 редуктаза–Цитохром Р450 Катализируются микросомальными монооксигеназами печени с участием О2 Субстратами являются гидрофобные вещества
- 13. Пример реакции гидроксилирования Фенобарбитал Н2О НАДФН+Н НАДФ Открыто 150 генов, кодирующих различные изоформы цитохрома Р450 у
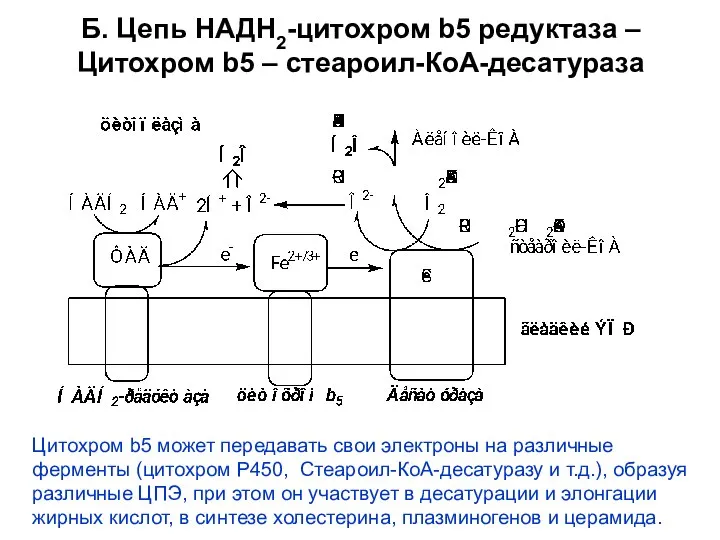
- 14. Б. Цепь НАДН2-цитохром b5 редуктаза – Цитохром b5 – стеароил-КоА-десатураза Цитохром b5 может передавать свои электроны
- 15. Биологическая роль микросомального окисления: Инактивация ксенобиотиков, т.е. уменьшение их фармакологической активности и токсичности. Повышение активности ксенобиотиков
- 16. 2. Митохондриальные монооксигеназные системы локализованы на внутренней поверхности внутренней мембране митохондрий и катализируют высокоспецифичные реакции Митохондриальные
- 17. Факторы, влияющие на активность ферментов биотрансформации Есть соединения, которые индуцируют скорость синтеза микросомальных ферментов – барбитураты,
- 18. Диоксигеназные реакции Диоксигеназы это ферменты, которые включают в субстрат оба атома молекулы кислорода: Таким путем окисляются
- 19. L-триптофандиоксигеназа печени, содержит гем, участвует в катаболизме триптофана:
- 20. ПЕРОКСИДАЗНЫЙ И РАДИКАЛЬНЫЙ ПУТИ ИСПОЛЬЗОВАНИЯ КИСЛОРОДА Химические соединения, в составе которых кислород имеет промежуточную степень окисления,
- 21. Образование АФК Соединения О + высокая энергия АФК Рентген УФИ Температура Гомолитический разрыв связей под действием
- 22. Основная часть АФК образуются в неферментативных и ферментативных реакциях в результате последовательного присоединения е- к кислороду
- 23. Неферментативные реакции образования АФК Электроны, необходимые для образования АФК могут давать: 1). Металлы переменной валентности. Hb(Fe2+)
- 24. Ферментативные реакции образования АФК В ЦОФ: Q + 1е- → НQ∙ (семихинон), при реоксигенации ишемических тканей
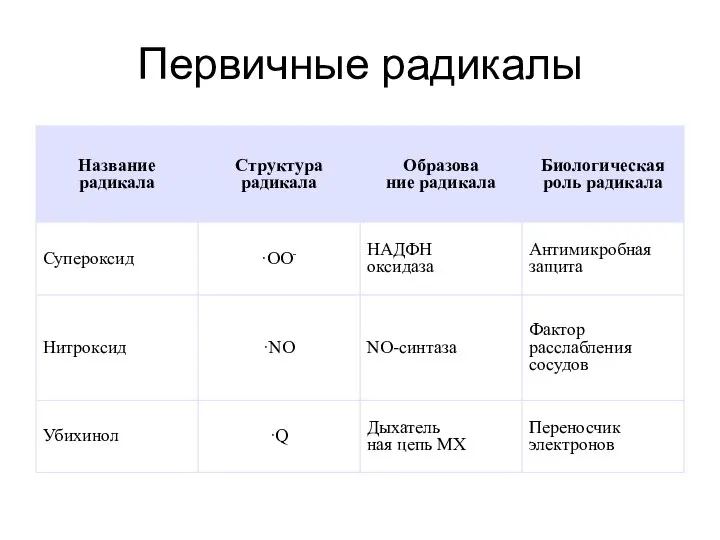
- 25. Первичные радикалы
- 26. Вторичные радикалы
- 27. Использование АФК в организме 1. Иммунная система. АФК используются фагоцитами - тканевыми макрофагами, моноцитами и гранулоцитами
- 28. Повреждающее действие АФК в организме Радикалы гидроксила химически исключительно активны и вызывают повреждение белков, нуклеиновых кислот
- 29. Субстраты ПОЛ – полиненасыщенные ЖК Линоленовая кислота — CH3(CH2CH=CH)3(CH2)7COOH. Арахидоновая кислота, витамин F, CH3(CH2)4(CH=CHCH2)4(CH2)2COOH и др.
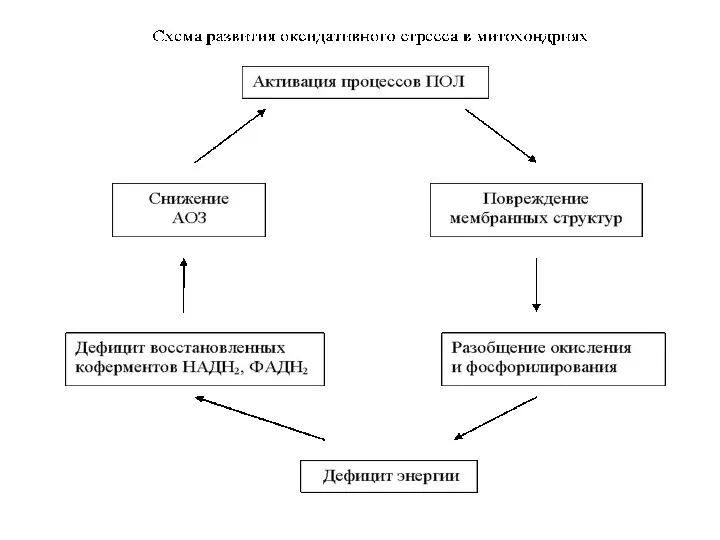
- 32. Антиоксидантная защита В нормальных условиях процесс СРО находится под строгим контролем ферментативных и неферментативных систем клетки,
- 33. АНТИОКИСЛИТЕЛЬНЫЕ ФЕРМЕНТЫ Супероксиддисмутаза (СОД) О*2 + О*-2 + 2Н+ → Н2О2 + О2 Каталаза 2Н2О2 →
- 34. пероксидазы Пероксидаза Н2О2 + НО-S-ОН → 2Н2О + О= S=О Глутатионпероксидаза (Se ) 2GSH + ROOH
- 35. Фосфолипаза в мембране отщепляет от фосфолипидов окисленные жирные кислоты, содержащие гидроперекисную группу (ROOH), тем самым разрушаются
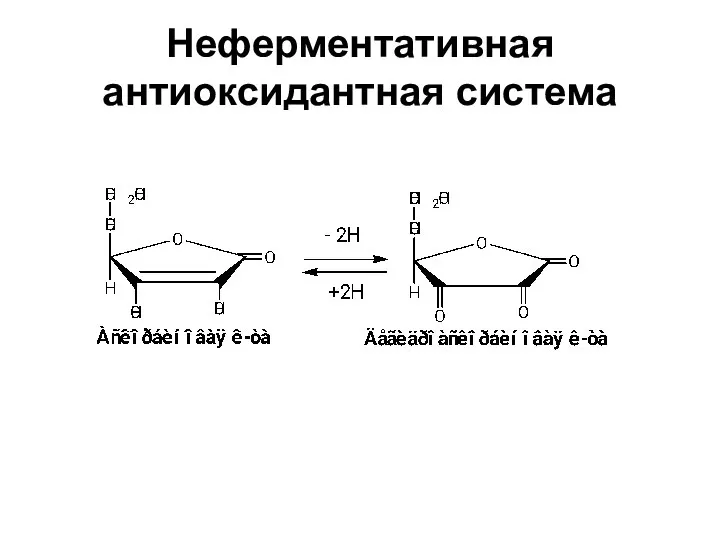
- 36. Неферментативная антиоксидантная система
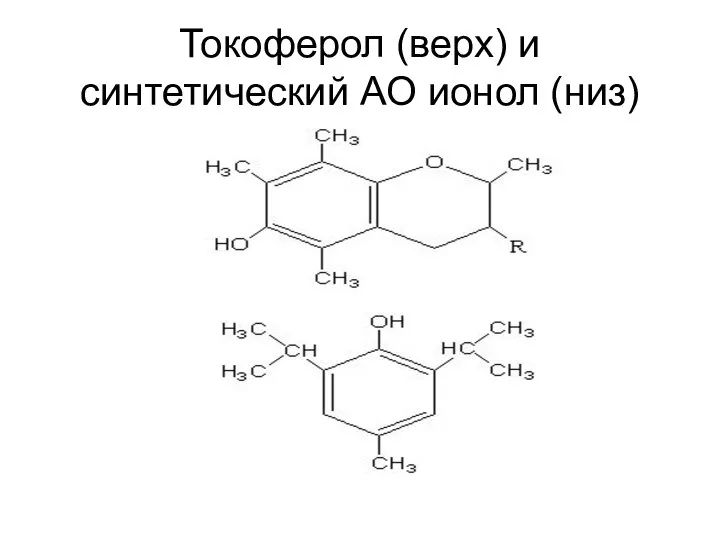
- 37. Токоферол (верх) и синтетический АО ионол (низ)
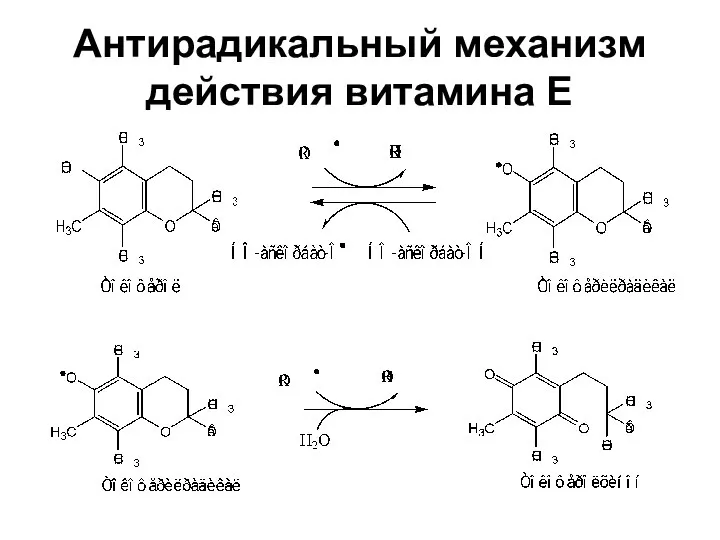
- 38. Антирадикальный механизм действия витамина Е
- 39. Антиоксиданты крови и цитоплазмы Церулоплазмин (плазма крови) -окисляет Fe2+ до Fe3+ молекулярным кислородом Апо-белок трансферрина (плазма
- 40. Глутатион- восстановает пероксиды Аскорбиновая кислота - регенерирует окисленные токоферол и убихинон Глутатионредуктаза - восстанавливает окисленный глутатион
- 42. Скачать презентацию





























 Топливо и его свойства
Топливо и его свойства Квалификация химических реактивов, принятая в РФ
Квалификация химических реактивов, принятая в РФ Термокаталитические процессы. Каталитический крекинг. Классификация и основные факторы процесса
Термокаталитические процессы. Каталитический крекинг. Классификация и основные факторы процесса Комплексные соединения. Лекция № 3
Комплексные соединения. Лекция № 3 Ферменти мікробіологічного синтезу
Ферменти мікробіологічного синтезу Анілін. Фізичні властивості
Анілін. Фізичні властивості Биохимия нервной и мышечной ткани
Биохимия нервной и мышечной ткани Реакции горения и материальный баланс котла
Реакции горения и материальный баланс котла Устойчивость и коагуляция коллоидных растворов
Устойчивость и коагуляция коллоидных растворов Молекулярная адсорбция. (Лекция 2)
Молекулярная адсорбция. (Лекция 2) Железо Железо не только основа всего мира, самый главный металл окружающей нас природы, оно – основа культуры и промышленности,
Железо Железо не только основа всего мира, самый главный металл окружающей нас природы, оно – основа культуры и промышленности,  Симметрия, структура и свойства твердых тел – кристаллография и кристаллофизика
Симметрия, структура и свойства твердых тел – кристаллография и кристаллофизика ГИА. А1: Строение атомов первых 20 химических элементов ПСХЭ
ГИА. А1: Строение атомов первых 20 химических элементов ПСХЭ Стартап. Производство минерального удобрения
Стартап. Производство минерального удобрения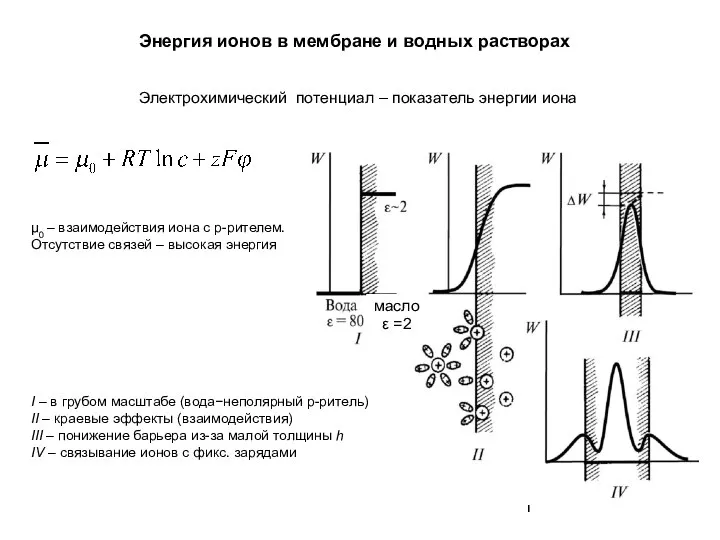 Энергия ионов в мембране и водных растворах
Энергия ионов в мембране и водных растворах Правила техники безопасности. Приемы обращения с лабораторным оборудованием
Правила техники безопасности. Приемы обращения с лабораторным оборудованием Карбонові кислоти. Насичені карбонові кислоти
Карбонові кислоти. Насичені карбонові кислоти Регуляция и патология липидного обмена
Регуляция и патология липидного обмена Количество вещества
Количество вещества Окислительно - восстановительные реакции
Окислительно - восстановительные реакции Химиялық реакцияның жылдамдығы. Катализ
Химиялық реакцияның жылдамдығы. Катализ Автоматизована мікропроцесорна система контролю концентрації речовин в розчинах
Автоматизована мікропроцесорна система контролю концентрації речовин в розчинах “ КОРОЗІЯ МЕТАЛІВ. ЗАХИСТ ВІД КОРОЗІЇ ” Підготував: Учень 10-А класу ЗОШ №25 м. Луцька Матвійчук Роман
“ КОРОЗІЯ МЕТАЛІВ. ЗАХИСТ ВІД КОРОЗІЇ ” Підготував: Учень 10-А класу ЗОШ №25 м. Луцька Матвійчук Роман  Качество питьевой воды
Качество питьевой воды Основные законы химии
Основные законы химии Рецепторы анионов
Рецепторы анионов Мұнай, құрамыөңдеу әдістері
Мұнай, құрамыөңдеу әдістері Фосфор, строение, свойства
Фосфор, строение, свойства