Содержание
- 2. Электролиты и неэлектролиты Соли Кислоты Щелочи Простые вещества-неметаллы Органические водорастворимые вещества (кроме кислот, аминов, солей)
- 3. Две теории растворов «Растворы – химические соединения, определяе-мые силами, действующи-ми между растворителем и растворенным веществом» Д.И.Менделеев
- 4. Две теории растворов С.Аррениус «Электролиты в растворах состоят частично из диссоциированных молекул, число которых растет при
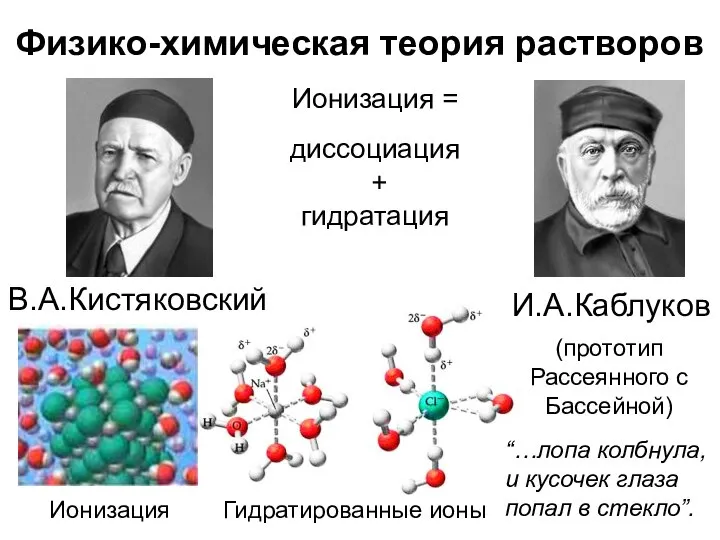
- 5. Физико-химическая теория растворов И.А.Каблуков Ионизация = диссоциация + гидратация Гидратированные ионы (прототип Рассеянного с Бассейной) В.А.Кистяковский
- 6. Энергетика диссоциации Na+(газ) + OH–(газ) + + H2O (частично неупорядоч.) NaOH(тв.) + H2O(ж.) Na+(р-р) + OH–(р-р)
- 7. Кислоты, основания, соли Кислота: катионы при диссоциации – только H+ Основание: анионы при диссоциации – только
- 8. Амфотерные гидроксиды X(OH)n [X(OH)n-1]+ +OH– [XO(OH)n-1]– +H+ Диссоциация по основному типу Диссоциация по кислотному типу От
- 9. Сильные электролиты Диссоциируют полностью или почти полностью
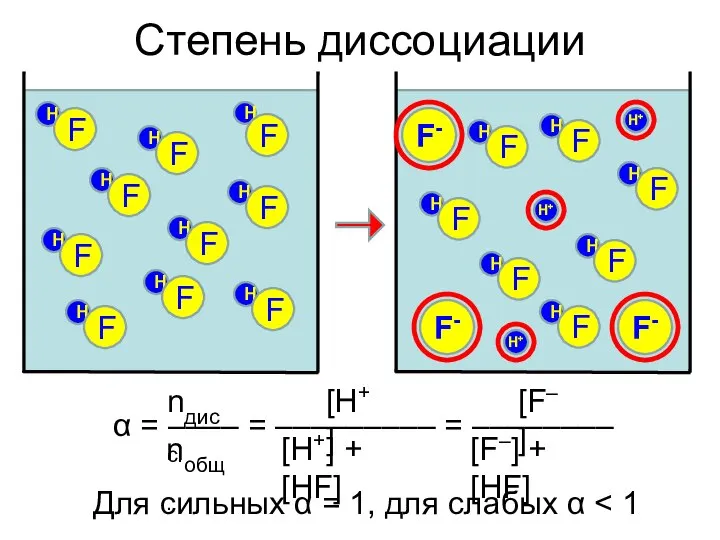
- 10. Степень диссоциации H+ F- H F H F H F H F H F H F
- 11. От чего зависит α? Природа растворителя (полярность и др.) – Н2О > C2H5OH > (C2H5)O >
- 12. Закон разбавления Оствальда К.В.Оствальд Только для очень разбавленных растворов слабых электролитов! α ~ 1/√CKtAn С →
- 13. Константа диссоциации HAn ⇄ H+ + An– – константа диссоциации Для многоосновных кислот – ступенчатая диссоциация
- 14. Вывод закона разбавления HAn ⇄ H+ + An– С0 СHAn 0 0 ΔC –x x x
- 16. Скачать презентацию





![Амфотерные гидроксиды X(OH)n [X(OH)n-1]+ +OH– [XO(OH)n-1]– +H+ Диссоциация по основному типу](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1407030/slide-7.jpg)





 Топливо и его свойства
Топливо и его свойства Квалификация химических реактивов, принятая в РФ
Квалификация химических реактивов, принятая в РФ Термокаталитические процессы. Каталитический крекинг. Классификация и основные факторы процесса
Термокаталитические процессы. Каталитический крекинг. Классификация и основные факторы процесса Комплексные соединения. Лекция № 3
Комплексные соединения. Лекция № 3 Ферменти мікробіологічного синтезу
Ферменти мікробіологічного синтезу Анілін. Фізичні властивості
Анілін. Фізичні властивості Биохимия нервной и мышечной ткани
Биохимия нервной и мышечной ткани Реакции горения и материальный баланс котла
Реакции горения и материальный баланс котла Устойчивость и коагуляция коллоидных растворов
Устойчивость и коагуляция коллоидных растворов Молекулярная адсорбция. (Лекция 2)
Молекулярная адсорбция. (Лекция 2) Железо Железо не только основа всего мира, самый главный металл окружающей нас природы, оно – основа культуры и промышленности,
Железо Железо не только основа всего мира, самый главный металл окружающей нас природы, оно – основа культуры и промышленности,  Симметрия, структура и свойства твердых тел – кристаллография и кристаллофизика
Симметрия, структура и свойства твердых тел – кристаллография и кристаллофизика ГИА. А1: Строение атомов первых 20 химических элементов ПСХЭ
ГИА. А1: Строение атомов первых 20 химических элементов ПСХЭ Стартап. Производство минерального удобрения
Стартап. Производство минерального удобрения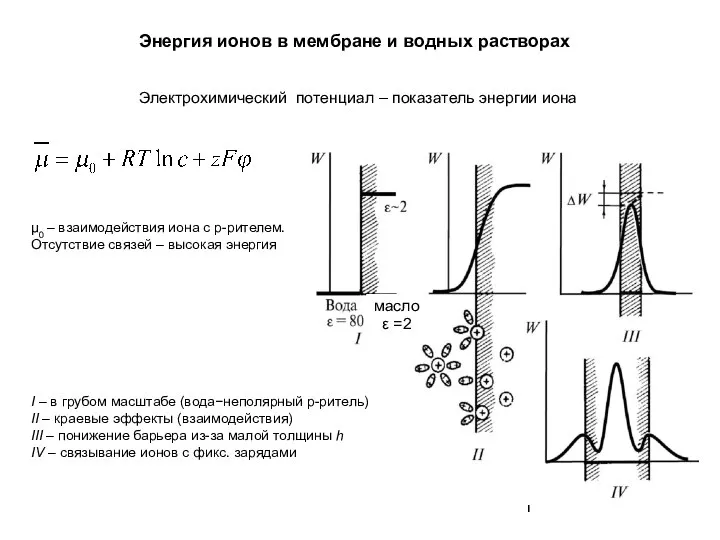 Энергия ионов в мембране и водных растворах
Энергия ионов в мембране и водных растворах Правила техники безопасности. Приемы обращения с лабораторным оборудованием
Правила техники безопасности. Приемы обращения с лабораторным оборудованием Карбонові кислоти. Насичені карбонові кислоти
Карбонові кислоти. Насичені карбонові кислоти Регуляция и патология липидного обмена
Регуляция и патология липидного обмена Количество вещества
Количество вещества Окислительно - восстановительные реакции
Окислительно - восстановительные реакции Химиялық реакцияның жылдамдығы. Катализ
Химиялық реакцияның жылдамдығы. Катализ Автоматизована мікропроцесорна система контролю концентрації речовин в розчинах
Автоматизована мікропроцесорна система контролю концентрації речовин в розчинах “ КОРОЗІЯ МЕТАЛІВ. ЗАХИСТ ВІД КОРОЗІЇ ” Підготував: Учень 10-А класу ЗОШ №25 м. Луцька Матвійчук Роман
“ КОРОЗІЯ МЕТАЛІВ. ЗАХИСТ ВІД КОРОЗІЇ ” Підготував: Учень 10-А класу ЗОШ №25 м. Луцька Матвійчук Роман  Качество питьевой воды
Качество питьевой воды Основные законы химии
Основные законы химии Рецепторы анионов
Рецепторы анионов Мұнай, құрамыөңдеу әдістері
Мұнай, құрамыөңдеу әдістері Фосфор, строение, свойства
Фосфор, строение, свойства