Содержание
- 2. Термодинамика система - открытая - закрытая - изолированная
- 3. Тепловая энергия Q, [Дж] Параметры состояния: P, T, V, состав системы
- 4. Функции состояния: Внутренняя энергия U, Энтальпия H, Энтропия S, Энергия Гиббса (изобарно-изотермический потенциал) G.
- 5. Первый закон термодинамики Q = ΔU + A ΔU = U2 – U1, U2 и U1
- 6. Изохорный процесс: V=const, ΔV = 0, А = 0, тогда QV = ΔU Изобарный процесс: Р=const
- 7. H = U + рV, Отсюда: Qp = Н2 – Н1 = ΔН ΔH > 0
- 8. H2(г) + 1/2О2(г) → H2O(ж); ΔrH = –285,84 кДж при 25°С и 101 кПа ΔH°обр или
- 9. ΔfH°298(O2) = 0, ΔfH°298(C(графит)) = 0, Однако: ΔfH°298(O3) = 142,3 кДж/моль, ΔfH°298(C(алмаз)) = 1,828 кДж/моль
- 10. Закон Лавуазье-Лапласа 1/2H2 (г) + 1/2Сl2(г) → HCl(г); ΔrH°298(HCl) = –92 кДж HCl(г) → 1/2H2 (г)
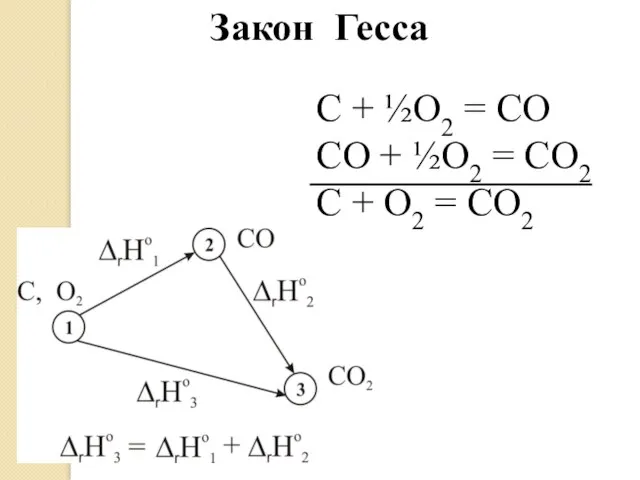
- 11. C + ½O2 = CO CO + ½O2 = CO2 C + O2 = CO2 Закон
- 12. Следствие из закона Гесса: ΔH = Для реакции в общем виде: аА + bB → cC
- 13. Пример: Вычислить тепловой эффект реакции горения бензола по стандартным энтальпиям образования С6Н6(ж) + 7/2О2(г) = 6СО2(г)
- 14. Энтропия, S [Дж/(моль⋅К)] Процессы, для которых ΔS > 0: 1) расширение газов; 2) Sтв SН2О(пар) =
- 15. Процессы, для которых ΔS 1) сжатие газов; 2) конденсация и кристаллизация веществ. S = Рассчитывается по
- 16. NH4NO2(к) = N2О(г) + 2H2О(г) V1 V2 V1 △S > 0 2H2S(г) + 3O2(г)= 2H2О(к) +
- 17. Энергия Гиббса, ΔG, [кДж/моль] ΔG = ΔН – ТΔS
- 18. ΔG ΔG > 0 – процесс термодинамически невозможен (реакция не идет); ΔG = 0 – система
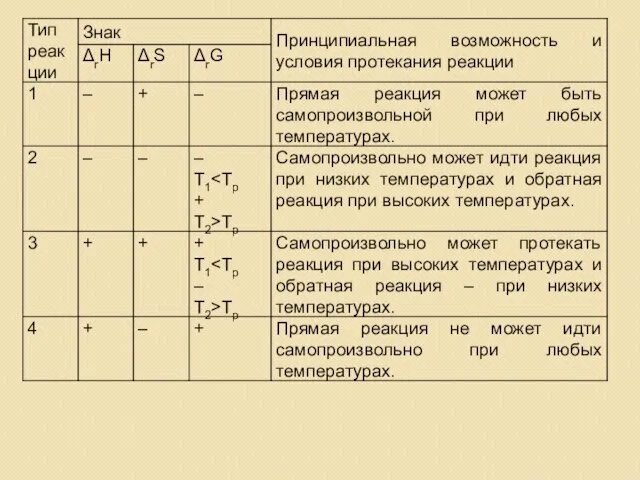
- 19. Возможность протекания реакции Реакция экзотермическая ΔН 0, ΔН ΔG = ΔН – ТΔS то всегда ΔG
- 20. Реакция эндотермическая ΔН > 0, ΔS ΔН > 0, ΔS > 0, ΔG = ΔН –
- 22. NH3(г) + HCl(г) = NH4Сl(к) при 298 К Выписываем из справочных данных: ΔrН° = ? ΔrS°
- 23. Из з-на Гесса энтальпия реакции: ΔrН° = ΔН°(NH4Сl(к)) – ΔН°(NH3(г)) – ΔН°(HCl(г)) = –315,39 – (–46,19
- 25. Скачать презентацию

![Тепловая энергия Q, [Дж] Параметры состояния: P, T, V, состав системы](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/530933/slide-2.jpg)









![Энтропия, S [Дж/(моль⋅К)] Процессы, для которых ΔS > 0: 1) расширение](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/530933/slide-13.jpg)

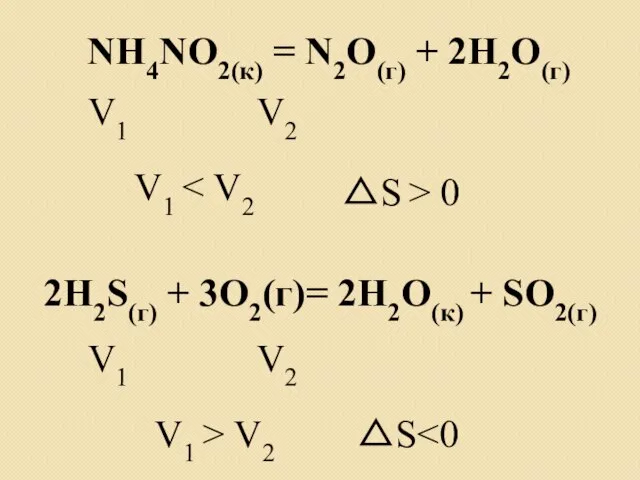
![Энергия Гиббса, ΔG, [кДж/моль] ΔG = ΔН – ТΔS](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/530933/slide-16.jpg)





 Природа активності та кислотності цеолітних каталізаторів
Природа активності та кислотності цеолітних каталізаторів Кристаллические решетки
Кристаллические решетки Электронное строение атома
Электронное строение атома Нуклеиновые кислоты
Нуклеиновые кислоты Электронное строение атома. Лекция № 2
Электронное строение атома. Лекция № 2 Марганец и его свойства
Марганец и его свойства Обратимость химических реакций. Химическое равновесие
Обратимость химических реакций. Химическое равновесие Практическая работа № 3. Получение, собирание и распознавание газов
Практическая работа № 3. Получение, собирание и распознавание газов Алкины. Гомологический ряд
Алкины. Гомологический ряд Презентация по Химии "Бензини" - скачать смотреть бесплатно
Презентация по Химии "Бензини" - скачать смотреть бесплатно Алкены – непредельные углеводороды
Алкены – непредельные углеводороды Контроль качества неорганических лекарственных средств элементов VII группы периодической системы Д. И. Менделеева
Контроль качества неорганических лекарственных средств элементов VII группы периодической системы Д. И. Менделеева Каталітичні процеси нафтопереробки
Каталітичні процеси нафтопереробки МОУ СОШ №5 ст.Бриньковская УРОК ПО ТЕМЕ: «ЧИСТАЯ ВОДА» подготовила учитель химии Беба Е.А.
МОУ СОШ №5 ст.Бриньковская УРОК ПО ТЕМЕ: «ЧИСТАЯ ВОДА» подготовила учитель химии Беба Е.А.  Алкени
Алкени Күрделі липидтер.Сабынданбайтын липидтер (стериндер, стероидтар) және олардың биологиялық маңызы. Терпендер
Күрделі липидтер.Сабынданбайтын липидтер (стериндер, стероидтар) және олардың биологиялық маңызы. Терпендер Карбоновые кислоты и их функциональные производные
Карбоновые кислоты и их функциональные производные Цепная сополимеризация
Цепная сополимеризация Неметаллы
Неметаллы Классификация веществ, вызывающих отравление. (Тема 4)
Классификация веществ, вызывающих отравление. (Тема 4) Углеводы
Углеводы Экоаналитический контроль воздуха
Экоаналитический контроль воздуха Реакция Бэйлиса Хиллмана-Мориты
Реакция Бэйлиса Хиллмана-Мориты Термодинамика фазовых превращений
Термодинамика фазовых превращений ДОСЛІДЖЕННЯ ДОСЛІДЖЕННЯ НАЙМАСОВІШИХ КУПАННЯ смт
ДОСЛІДЖЕННЯ ДОСЛІДЖЕННЯ НАЙМАСОВІШИХ КУПАННЯ смт XXI ғасыр көшбасшысы
XXI ғасыр көшбасшысы Рівняння характеристики крупності
Рівняння характеристики крупності IV,III группа периодической системы Д..И. Менделеева. Кислота борная, натрия гидрокарбонат
IV,III группа периодической системы Д..И. Менделеева. Кислота борная, натрия гидрокарбонат