Содержание
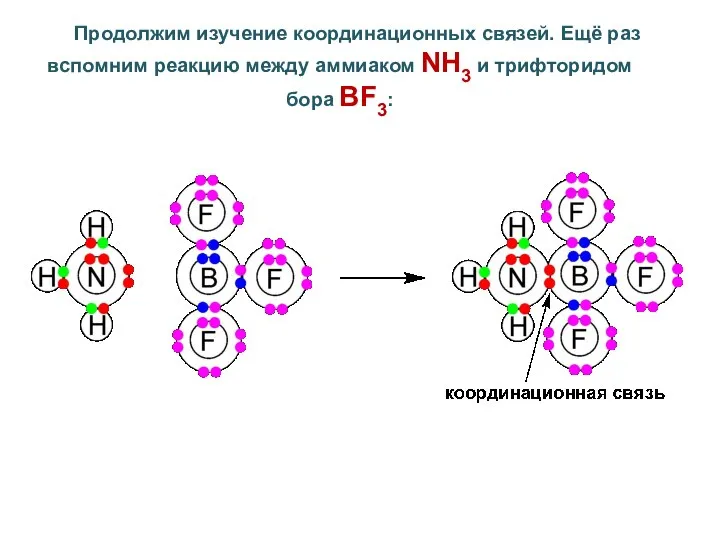
- 2. Продолжим изучение координационных связей. Ещё раз вспомним реакцию между аммиаком NH3 и трифторидом бора BF3:
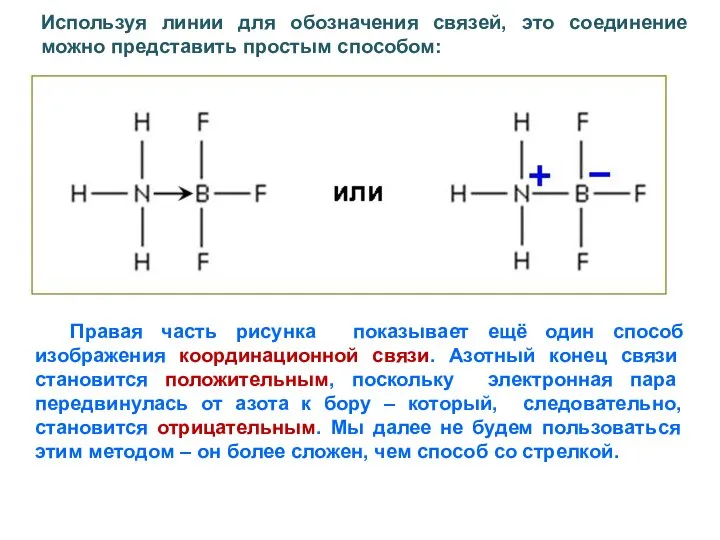
- 3. Используя линии для обозначения связей, это соединение можно представить простым способом: Правая часть рисунка показывает ещё
- 4. Если из аммиака в водном растворе соляной кислоты (HCl) образуется всем известный ион аммония, NH4+, то
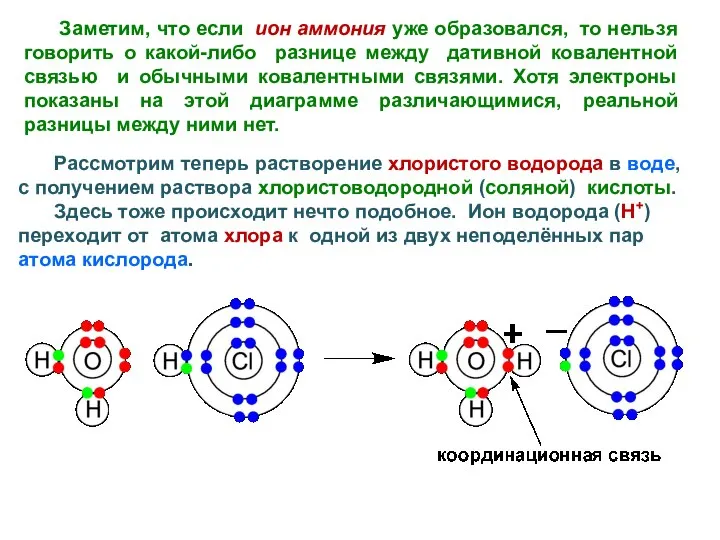
- 5. Заметим, что если ион аммония уже образовался, то нельзя говорить о какой-либо разнице между дативной ковалентной
- 6. Или в обычном виде: Ион H3O+ называют ионом гидроксония, но иногда ионом гидрония или ионом оксония.
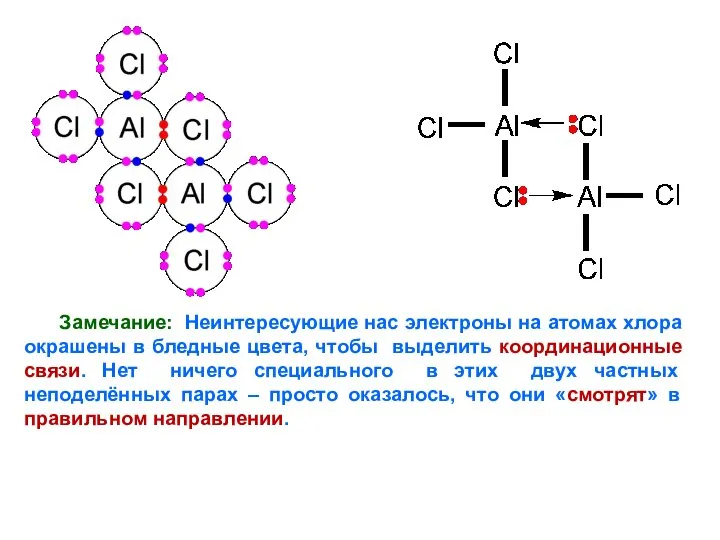
- 7. Рассмотрим более сложный пример димеризации солей: структура хлорида алюминия Хлорид алюминия сублимируется (превращается прямо из твёрдой
- 8. AlCl3, подобно BF3, является электронно-дефицитным. В самом деле, этого подобия следует ожидать, поскольку Al и B
- 9. Замечание: Неинтересующие нас электроны на атомах хлора окрашены в бледные цвета, чтобы выделить координационные связи. Нет
- 10. Связь в гидратированных металлических ионах Водные молекулы сильно притягиваются к ионам в растворе – молекулы воды
- 11. Связь в нём (и подобных комплексных ионах, образованных огромным большинством других металлов) является координационной (дативной ковалентной)
- 12. Это означает, что все орбитали 3-уровня теперь пусты. Алюминий перестраивает (гибридизует) шесть этих орбиталей (одну 3s,
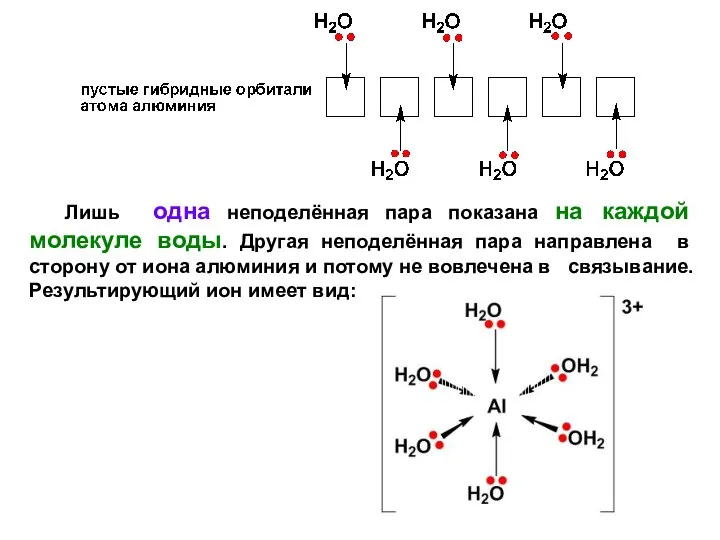
- 13. Лишь одна неподелённая пара показана на каждой молекуле воды. Другая неподелённая пара направлена в сторону от
- 14. Из-за движения электронов к центру иона, заряд 3+ теперь не расположен полностью на алюминии, но распределён
- 15. Al3+ + 6H2O → [Al(H2O)6]3+ + H2O → [Al(H2O)5(OH)]2+ + H3O+ Очевидно, что и [Al(H2O)6]3+ и
- 16. Помимо реакций между ионами и нейтральными полярными молекулами, связывание катионов с группами анионов также приводит к
- 17. Существование координационных комплексных соединений основано на образовании координационной химической связи, для которой требуется наличие акцептора электронной
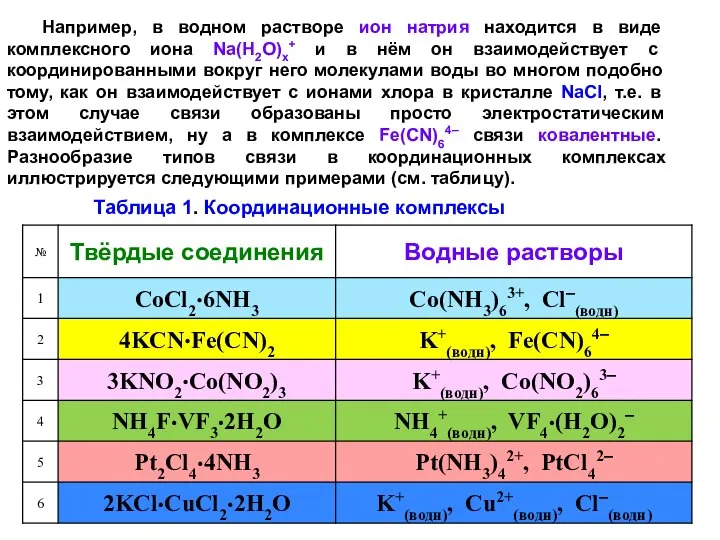
- 18. Например, в водном растворе ион натрия находится в виде комплексного иона Na(H2O)x+ и в нём он
- 19. Первые четыре соединения можно рассматривать, как соли с комплексным катионом или анионом, что особенно хорошо видно
- 20. Пятое соединение Pt2Cl4·4NH3 и в твёрдом кристаллическом состоянии , и в водном растворе содержит одновременно и
- 21. Ni(H2O)62+ + 6 NH3 → Ni(NH3)62+ + 6H2O зелёный синий 2. Ni(H2O)62+ + en → Ni(en)(H2O)42+
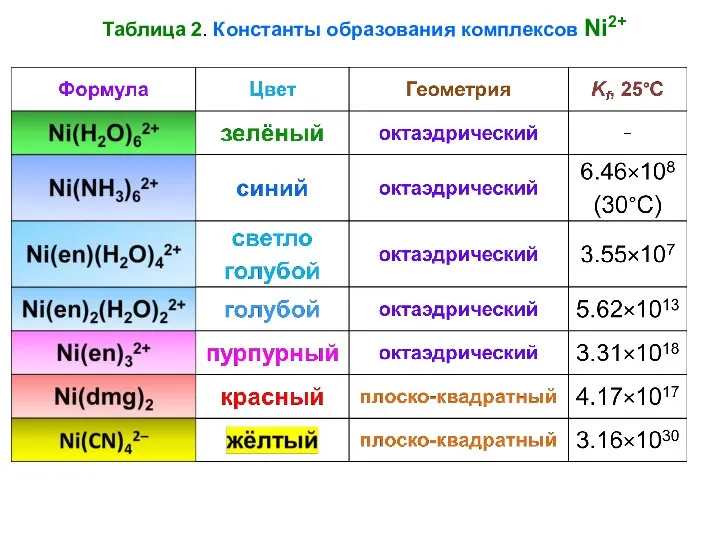
- 22. Таблица 2. Константы образования комплексов Ni2+
- 23. Геометрические структуры комплексов 1. Ион гексааквоникеля (II): Ni(H2O)62+ 2. Ион гексаамминникеля (II): Ni(NH3)62+
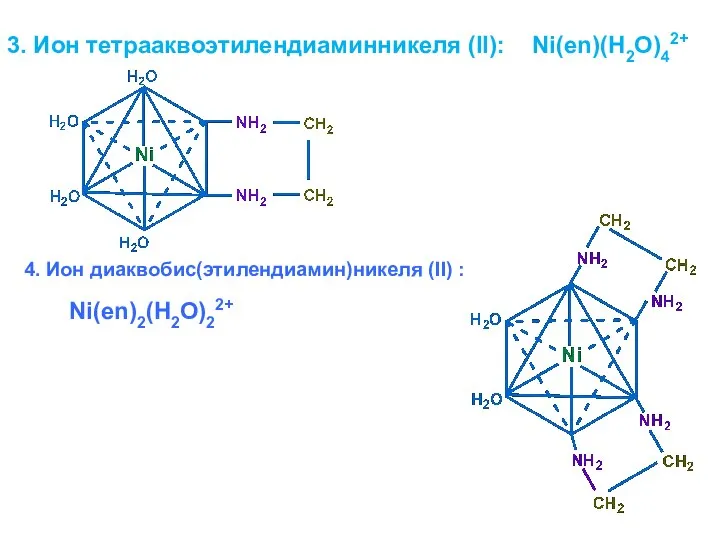
- 24. 3. Ион тетрааквоэтилендиаминникеля (II): Ni(en)(H2O)42+ 4. Ион диаквобис(этилендиамин)никеля (II) : Ni(en)2(H2O)22+
- 25. 5. Ион трисэтилендиаминникеля (II): Ni(en)32+
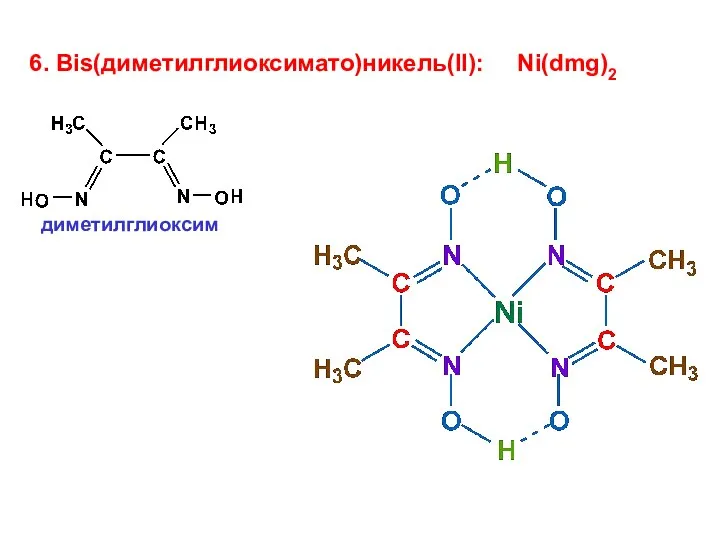
- 26. 6. Bis(диметилглиоксимато)никель(II): Ni(dmg)2 диметилглиоксим
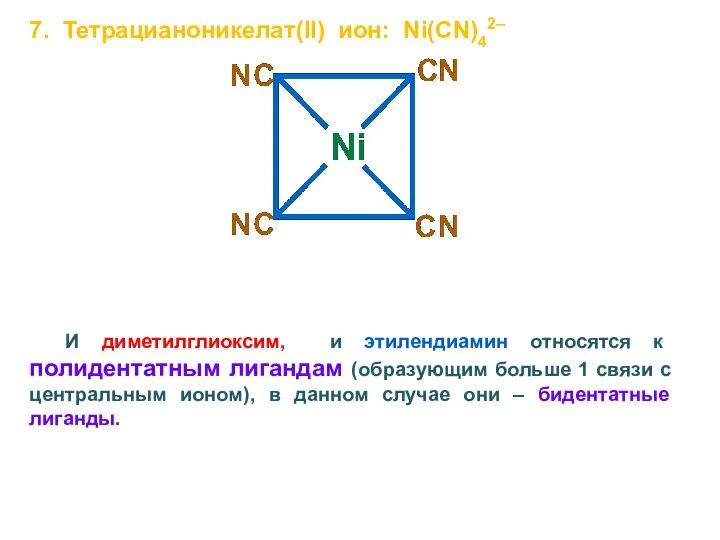
- 27. 7. Тетрацианоникелат(II) ион: Ni(CN)42– И диметилглиоксим, и этилендиамин относятся к полидентатным лигандам (образующим больше 1 связи
- 28. Пример практического использования комплексов. В обоих пигментах имеется эта группировка так что по сути Турнбуллева синь
- 29. Применяется: При производстве вина, когда избыток железа в вине удаляют контролирующими добавками K4Fe(CN)6. Главное применение –
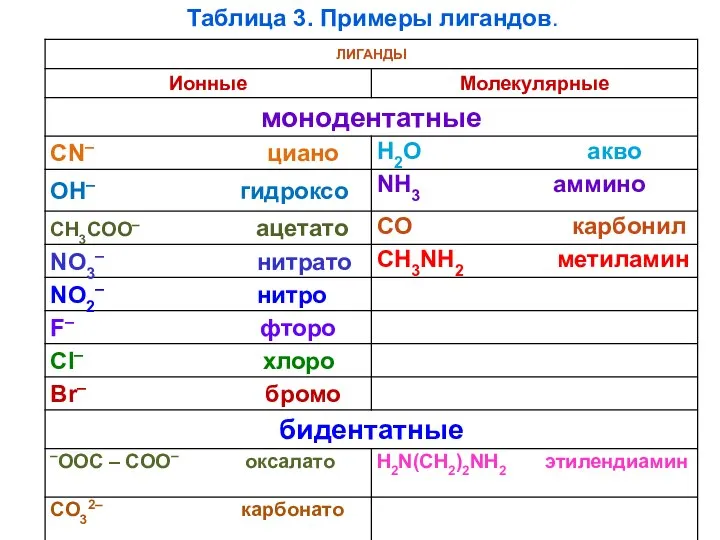
- 30. Таблица 3. Примеры лигандов.
- 31. Координационное число и геометрическое строение комплексов Вернёмся к реакции образования комплекса из центрального атома и нескольких
- 32. Таблица 4. Зависимость геометрического строения комплексов от координационного числа центрального иона.
- 34. Интересно выяснить, каково предельное число лигандов, которое может координироваться вокруг центрального иона. В некоторых комплексах координационное
- 35. В некоторых случаях имеет значение то, что лиганд оказывается значительно больше катиона по размерам: Экспериментальные наблюдения
- 36. Однако, если это отношение радиусов очень мало, более важным фактором является не геометрические соотношения, а баланс
- 37. ПРИРОДА ХИМИЧЕСКОЙ СВЯЗИ В КООРДИНАЦИОННЫХ КОМПЛЕКСАХ Как уже говорилось, во многих отношениях связи в комплексных соединениях
- 38. У всех элементов с порядковыми номерами больше 10 имеется по крайней мере 9 валентных орбиталей: одна
- 39. Таблица 5. Гибридные орбитали, участвующие в образовании связей в координационных комплексах.
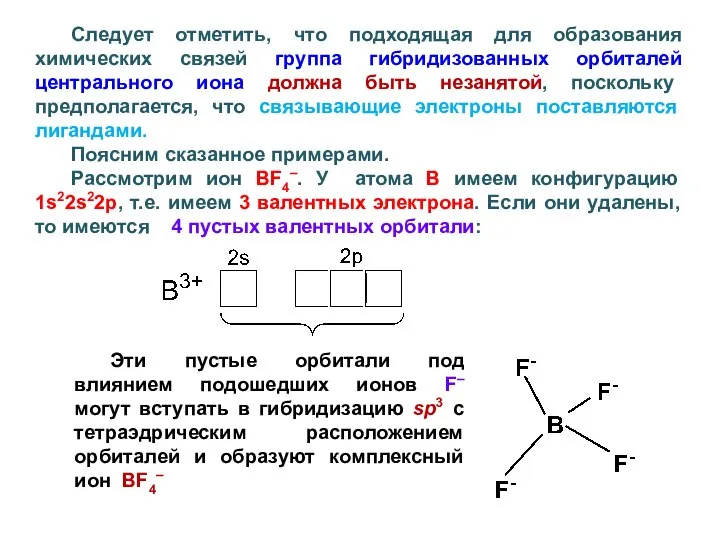
- 40. Следует отметить, что подходящая для образования химических связей группа гибридизованных орбиталей центрального иона должна быть незанятой,
- 41. Рассмотрим образование комплекса Zn(NH3)42+. У атома Zn к валентным относятся 4s, 4p и 3d орбитали. Однако,
- 42. Оставшиеся пустыми валентные орбитали вступают в гибридизацию, образуя плоскоквадратную структуру. Или пример образования комплексного иона AlF63–
- 43. Устойчивость комплексов Чаще всего представляет интерес степень диссоциации комплекса на катион и лиганды в равновесных условиях.
- 44. Это уравнение представляет собой сумму уравнений отдельных стадий диссоциации, каждой из которых соответствует своя константа равновесия,
- 45. Суммарному уравнению соответствует константа равновесия, которую принято называть константой нестойкости, она, как легко показать, представляет собой
- 46. При прочих равных условиях лиганды, которые являются хорошими донорами электронов, дают наиболее устойчивые комплексы. Применение координационных
- 47. Факторы, определяющие устойчивость комплексов в зависимости от типа лигандов. Основность (способность отдавать электронную пару, быть донором)
- 48. Стабильность комплексов возрастает по мере повышения заряда центрального катиона, а в случае одинаковых зарядов катионов –
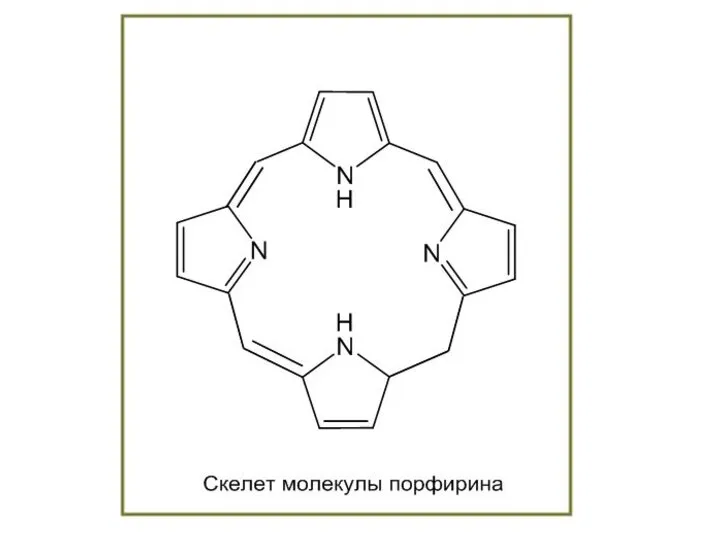
- 49. Протеин, переносящий кислород в крови: гемоглобин Один из наиболее важных способов связывания металлических ионов – образование
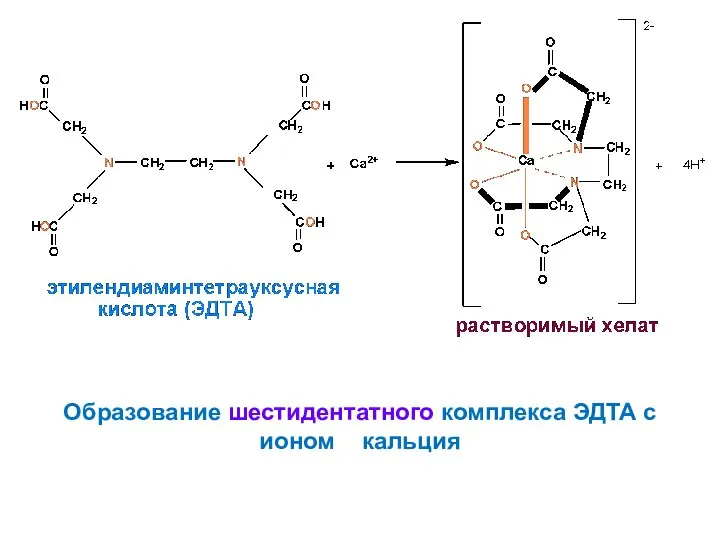
- 51. Образование шестидентатного комплекса ЭДТА с ионом кальция
- 55. Скачать презентацию








![Al3+ + 6H2O → [Al(H2O)6]3+ + H2O → [Al(H2O)5(OH)]2+ + H3O+](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/606958/slide-14.jpg)





























 11 хб
11 хб  Химия. Вопросы. Практическая работа
Химия. Вопросы. Практическая работа Серная кислота H2SO4
Серная кислота H2SO4 EPR of phosphorus in diamond crystals. An influence of nitrogen impurity, HTHP treatment and high phosphorus concentration
EPR of phosphorus in diamond crystals. An influence of nitrogen impurity, HTHP treatment and high phosphorus concentration Дека́н (н-декан) — органическое соединение класса алканов
Дека́н (н-декан) — органическое соединение класса алканов Катализдің түрлері жене маңызы
Катализдің түрлері жене маңызы Химические Недотроги
Химические Недотроги  Названы именем Д.И.Менделеева. Презентацию подготовили: Баранов С.-ученик 9 класса Мошковской СОШ Воронцова О.Е. – учитель химии М
Названы именем Д.И.Менделеева. Презентацию подготовили: Баранов С.-ученик 9 класса Мошковской СОШ Воронцова О.Е. – учитель химии М Сопротивление материалов. Металлический тип химической связи и основные свойства металлов
Сопротивление материалов. Металлический тип химической связи и основные свойства металлов Растворы электролитов
Растворы электролитов Синтез реакционноспособных олигомеров и полимеров на их основе
Синтез реакционноспособных олигомеров и полимеров на их основе Поверхностные явлении и дисперсные системы (коллоидная химия)
Поверхностные явлении и дисперсные системы (коллоидная химия) Решение задач на растворы и смеси
Решение задач на растворы и смеси Презентация по Химии "Закон збереження маси" - скачать смотреть
Презентация по Химии "Закон збереження маси" - скачать смотреть  F элементы
F элементы Жёсткость воды и способы её устранения
Жёсткость воды и способы её устранения Аминокислоты. Номенклатура аминокислот
Аминокислоты. Номенклатура аминокислот Все о витамине С и его определение в лекарственных растениях и продуктах питания
Все о витамине С и его определение в лекарственных растениях и продуктах питания История микроскопа
История микроскопа  Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Оборудование кабинета химии. Смотрите внимательно и запоминайте!!!
Оборудование кабинета химии. Смотрите внимательно и запоминайте!!! Презентация по Химии "Белки" - скачать смотреть бесплатно_
Презентация по Химии "Белки" - скачать смотреть бесплатно_ Презентация по Химии "История развития химии" - скачать смотреть
Презентация по Химии "История развития химии" - скачать смотреть  Анализ смеси катионов первойтретьей аналитических групп по систематическому анализу. Химическое равновесие
Анализ смеси катионов первойтретьей аналитических групп по систематическому анализу. Химическое равновесие Көмірдің оптикалық қасиеттері
Көмірдің оптикалық қасиеттері Простые и сложные вещества Моцепуро Иван Класс 10 «а» Учитель: Макарова Е. И.
Простые и сложные вещества Моцепуро Иван Класс 10 «а» Учитель: Макарова Е. И. Ферменттер – тіршілік негізі
Ферменттер – тіршілік негізі Синергизм и синергические системы
Синергизм и синергические системы