Содержание
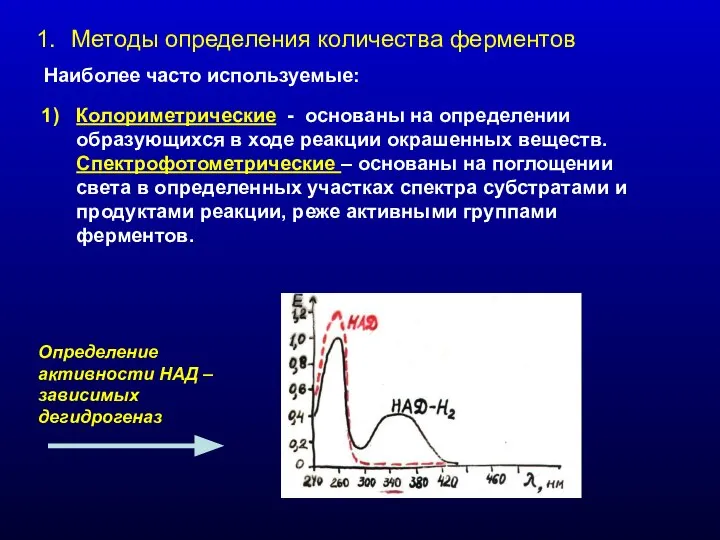
- 2. Методы определения количества ферментов Наиболее часто используемые: Колориметрические - основаны на определении образующихся в ходе реакции
- 3. 2. Способы выражения активности ферментов. Используются 2 основные единицы: КАТАЛ – такое количество фермента, которое может
- 4. 3. Кинетика ферментативных реакций Ферментативная кинетика занимается исследованием закономерностей влияния химической природы реагирующих веществ (ферментов, субстратов)
- 5. Зависимость скорости от вида субстрата. Ферменты обладают избирательностью действия - специфичность действия: 1 – Абсолютная специфичность.
- 6. 2 – Относительная специфичность ( объясняется тем, что, активный центр ферментов, обладаю-щих относительной специфичностью не жесткая
- 7. 2) Влияние [S] на скорость реакции. Теоретический график зависимости скорости ферментативной реакции от концентрации субстрата при
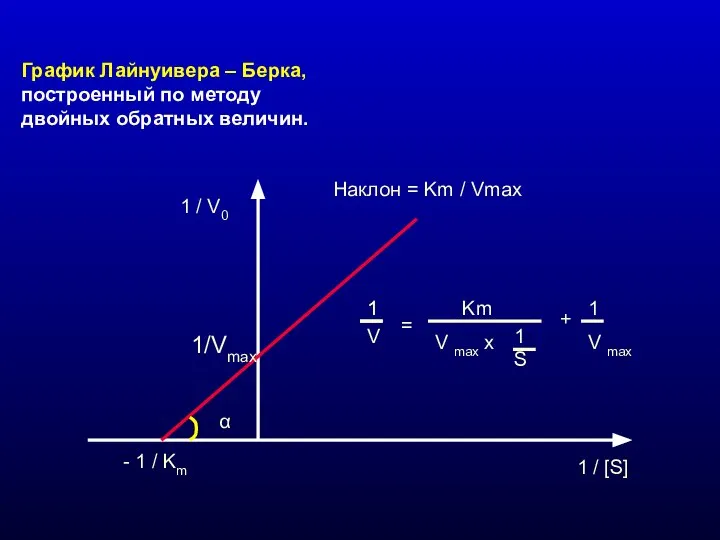
- 8. График Лайнуивера – Берка, построенный по методу двойных обратных величин. 1 / V0 1 / [S]
- 9. 3) Зависимость скорости реакции от концентрации фермента. 4) Зависимость скорости реакции от температуры. 4Х 3Х 2Х
- 10. 4) Зависимость скорости реакции от рН среды. В норме рН цитозоля =7,2 1 2 3 4
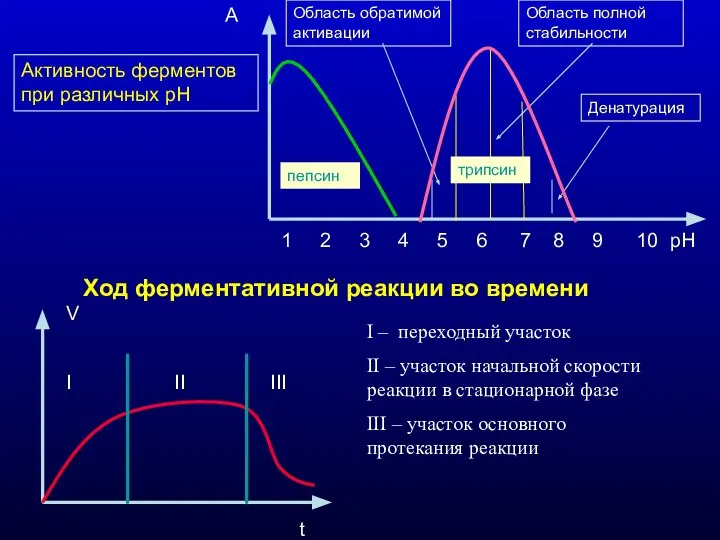
- 11. Активность ферментов при различных рН 1 2 3 4 5 6 7 8 9 10 рН
- 12. Влияние различных веществ на активность ферментов АКТИВАТОРЫ ФЕРМЕНТОВ 1.1. Активация ферментов ионами металлов Ионы Mg+2, Mn+2,
- 13. Механизм активации ферментов металлами 1. В состав активного центра: Н2О + СО2 Н2СО3 Е + Ме
- 14. Активность амилазы в присутствии различных ионов Cl Br 1 2 3 4 5 6 7 8
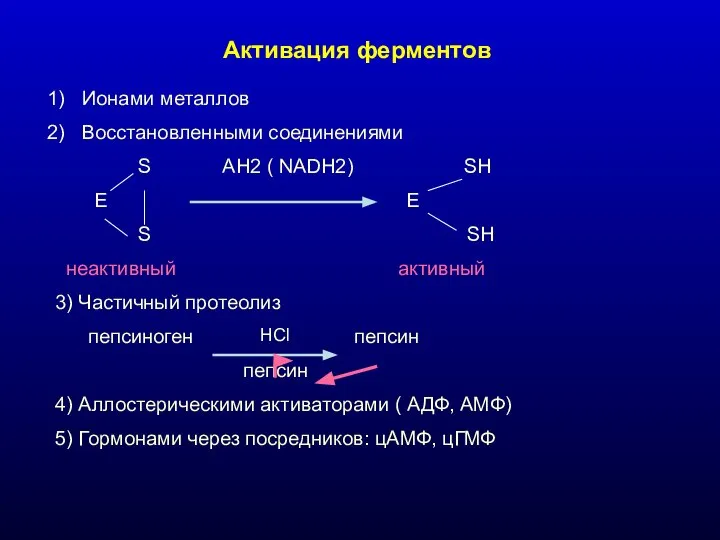
- 15. Активация ферментов Ионами металлов Восстановленными соединениями S AH2 ( NADH2) SH E E S SH неактивный
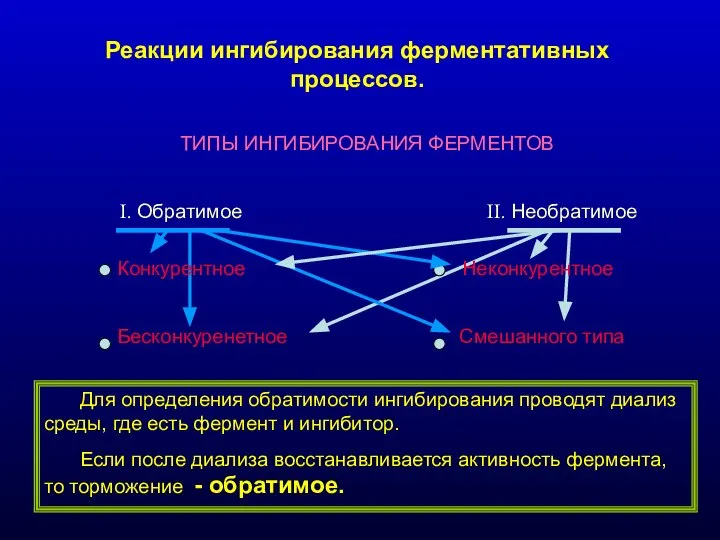
- 16. Реакции ингибирования ферментативных процессов. ТИПЫ ИНГИБИРОВАНИЯ ФЕРМЕНТОВ I. Обратимое II. Необратимое Конкурентное Неконкурентное Бесконкуренетное Смешанного типа
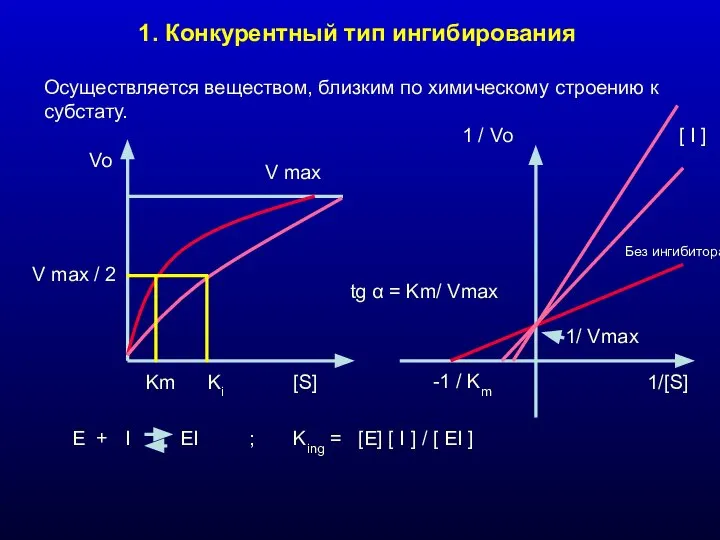
- 17. 1. Конкурентный тип ингибирования Осуществляется веществом, близким по химическому строению к субстату. V max Vo [S]
- 18. 2. Неконкурентное торможение Ингибитор реагирует с ферментом иным образом , чем субстрат, и поэтому повышение концентрации
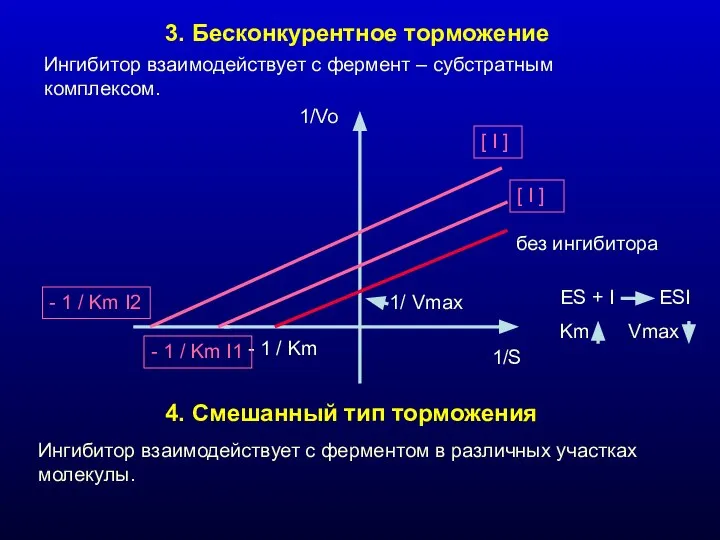
- 19. 3. Бесконкурентное торможение Ингибитор взаимодействует с фермент – субстратным комплексом. 4. Смешанный тип торможения Ингибитор взаимодействует
- 20. Ингибиторы взаимодействуют с ферментами различными путями, они могут: Блокировать активный центр фермента Менять четвертичную структуру фермента
- 21. Классификация ингибиторов ИНГИБИТОРЫ 1) специфические 2) неспецифические 3) Необратимого действия конкурентные неконкурентные 4) Обратимого действия 5)
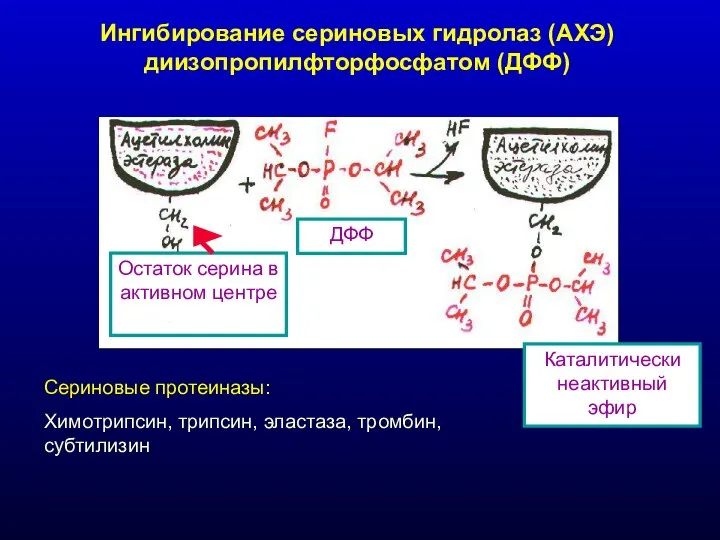
- 22. Ингибирование сериновых гидролаз (АХЭ) диизопропилфторфосфатом (ДФФ) Остаток серина в активном центре ДФФ Каталитически неактивный эфир Сериновые
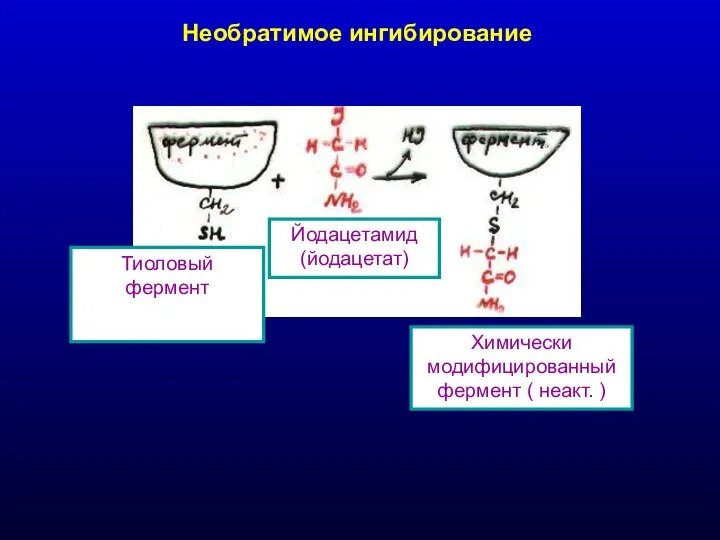
- 23. Необратимое ингибирование Химически модифицированный фермент ( неакт. ) Йодацетамид (йодацетат) Тиоловый фермент
- 24. Необратимое ингибирование Трансацилаза –один из ферментов, участвующих в биосинтезе клеточной стенки бактерий. - CH2OH + Трансацилаза
- 25. Необратимое ингибирование тиоловых ферментов Химически модифицированный фермент ( неакт. ) ТОКСИЧЕСКОЕ ДЕЙСТВИЕ Hg++ Pb++ , соединений
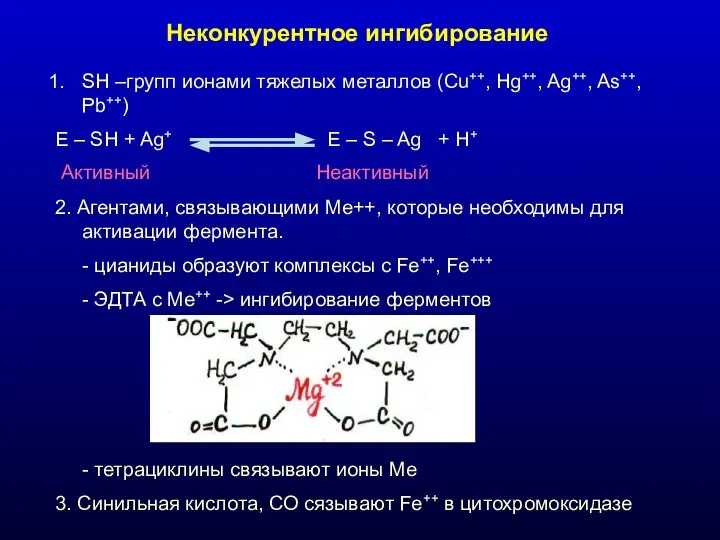
- 26. Неконкурентное ингибирование SH –групп ионами тяжелых металлов (Cu++, Hg++, Ag++, As++, Pb++) E – SH +
- 27. Неконкурентное ингибирование монотиоловых ферментов - SH - SH Активный Е + Cl As – CH =
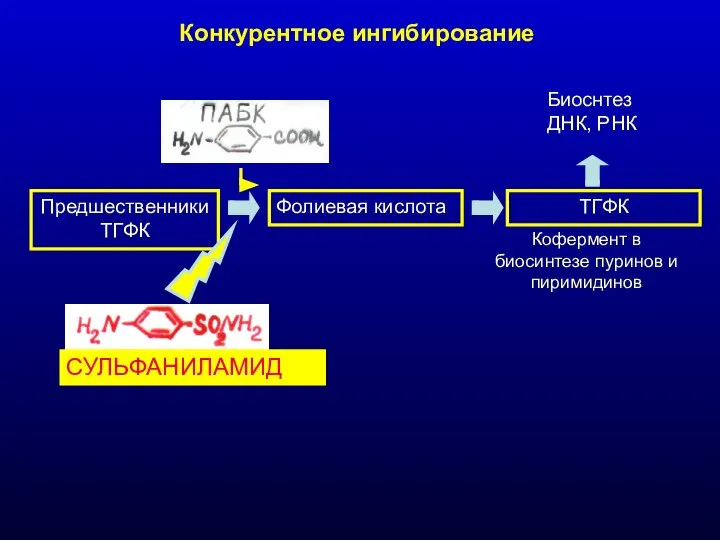
- 28. Конкурентное ингибирование ПредшественникиТГФК Фолиевая кислота ТГФК Биоснтез ДНК, РНК Кофермент в биосинтезе пуринов и пиримидинов СУЛЬФАНИЛАМИД
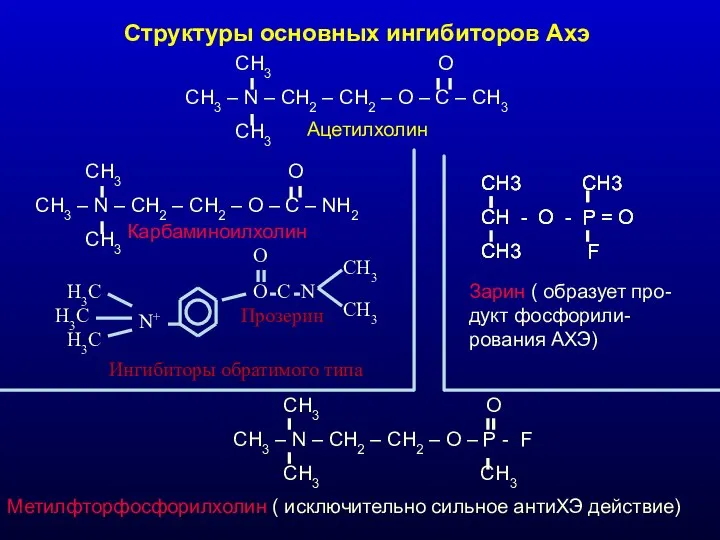
- 29. Структуры основных ингибиторов Ахэ CH3 O CH3 – N – CH2 – CH2 – O –
- 30. Инактивация АХЭ
- 31. Реактивация АХЭ -I Пиридин-альдоксин-метил-йодид
- 32. Аллостерическое ингибирование Е I EI - комплекс + Аллостерический центр (НАДН2, АТФ) V max Vo [S]
- 33. Фосфатная модификация ферментов Е - ОН Е – О – РО3Н2 АТФ АДФ гликогенсинтаза Неактивный фермент
- 34. Ингибирование фермента путем ацетатной модификации PES - NH2 + Н3С-С-О || O COO- Простагландин-эндопироксид-синтаза (ее циклоге-назный
- 36. Скачать презентацию




![2) Влияние [S] на скорость реакции. Теоретический график зависимости скорости ферментативной](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1408507/slide-6.jpg)
















 Күрделі липидтер.Сабынданбайтын липидтер (стериндер, стероидтар) және олардың биологиялық маңызы. Терпендер
Күрделі липидтер.Сабынданбайтын липидтер (стериндер, стероидтар) және олардың биологиялық маңызы. Терпендер Урок № 11 Углекислый газ Цель урока: Систематизировать знания о физических свойствах углекислого газа. Повторить понятия «
Урок № 11 Углекислый газ Цель урока: Систематизировать знания о физических свойствах углекислого газа. Повторить понятия « Презентация по Химии "Полиэтилен" - скачать смотреть
Презентация по Химии "Полиэтилен" - скачать смотреть  Базовое нефтехимическое сырье. Технология каткрекинга
Базовое нефтехимическое сырье. Технология каткрекинга Презентация по Химии "Роль металлов в искусстве" - скачать смотреть
Презентация по Химии "Роль металлов в искусстве" - скачать смотреть  Диаграммы состояния двухкомпонентных систем типа твердое тело – жидкость
Диаграммы состояния двухкомпонентных систем типа твердое тело – жидкость Презентация на тему: Кислотные дожди
Презентация на тему: Кислотные дожди Органическая химия. Лекция. Стероиды
Органическая химия. Лекция. Стероиды Глауберова соль
Глауберова соль Металлы ГОУ СОШ № 661 УЧИТЕЛЬ ХИМИИ Ефремова С.А.
Металлы ГОУ СОШ № 661 УЧИТЕЛЬ ХИМИИ Ефремова С.А.  Свойства кислот Сульфура H2SO4, H2SO3, H2S
Свойства кислот Сульфура H2SO4, H2SO3, H2S Аміни. Метиламін
Аміни. Метиламін Экскурсия по химическому факультету
Экскурсия по химическому факультету Предельные углеводороды
Предельные углеводороды Презентация по Химии "Техника безопасности в кабинете химии" - скачать смотреть
Презентация по Химии "Техника безопасности в кабинете химии" - скачать смотреть  Азот. Физические и химические свойства азота
Азот. Физические и химические свойства азота Гетерофункционалды органикалық қосылыстар
Гетерофункционалды органикалық қосылыстар Производство метанола и этанола
Производство метанола и этанола Слайд-шоу. Коррозия металлов и сплавов
Слайд-шоу. Коррозия металлов и сплавов Алюминий и его свойства
Алюминий и его свойства Коррозия металлов
Коррозия металлов Адиабатическое приближение
Адиабатическое приближение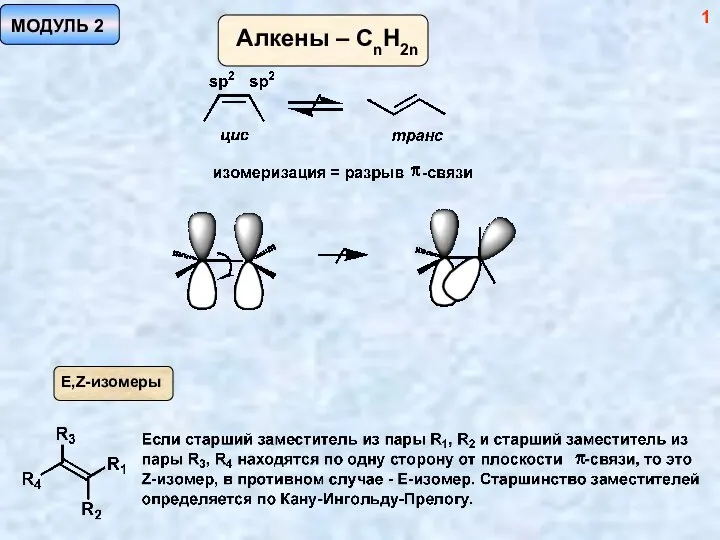 Методы синтеза алкенов. (Модуль 2)
Методы синтеза алкенов. (Модуль 2) Количественные методы анализа риска
Количественные методы анализа риска Исследование зависимости интенсивности люминесценции пленок оксида цинка от уровня фотовозбуждения
Исследование зависимости интенсивности люминесценции пленок оксида цинка от уровня фотовозбуждения Silicates
Silicates Оксиды
Оксиды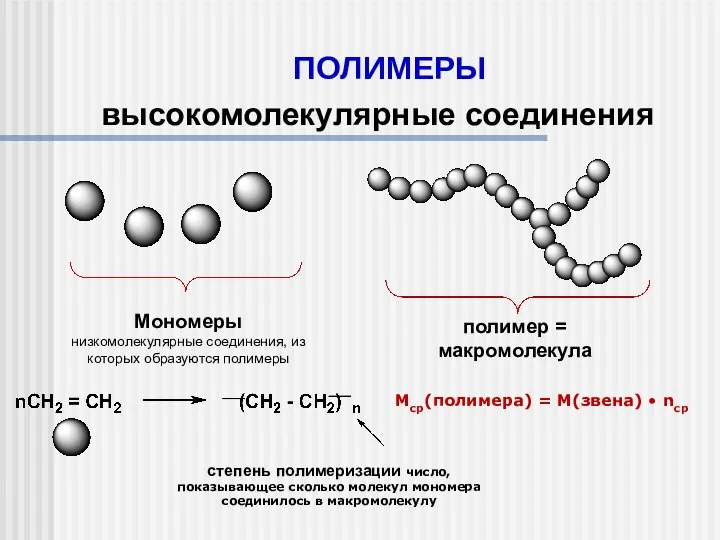 Полимеры. Высокомолекулярные соединения
Полимеры. Высокомолекулярные соединения