Содержание
- 2. Химическая кинетика – учение о скоростях химических реакций и влиянии различных факторов на скорость. Задачи химической
- 3. Химическая кинетика изучает протекание процессов во времени, т.е. в неравновесном состоянии системы. Основная кинетическая характеристика –
- 13. ПРИЧИНЫ НЕСОВПАДЕНИЯ МОЛЕКУЛЯРНОСТИ И ПОРЯДКА
- 15. Основной постулат формальной кинетики объединяет два подхода к описанию скорости реакции : КИНЕТИКА НЕОБРАТИМЫХ РЕАКЦИЙ ЦЕЛОГО
- 16. КИНЕТИЧЕСКОЕ УРАВНЕНИЕ РЕАКЦИИ ПЕРВОГО ПОРЯДКА
- 20. КИНЕТИЧЕСКОЕ УРАВНЕНИЕ РЕАКЦИИ ВТОРОГО ПОРЯДКА
- 23. КИНЕТИЧЕСКОЕ УРАВНЕНИЕ РЕАКЦИИ ТРЕТЬЕГО ПОРЯДКА
- 25. Порядок реакции является эмпирической величиной и не может быть рассчитан теоретически, если не известен механизм реакции.
- 27. метод подстановки (аналитический и графический) метод времени полупревращения метод Оствальда-Нойеса (аналитический) ИНТЕГРАЛЬНЫЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ ПОРЯДКА РЕАКЦИИ
- 28. 1) МЕТОД ПОДСТАНОВКИ
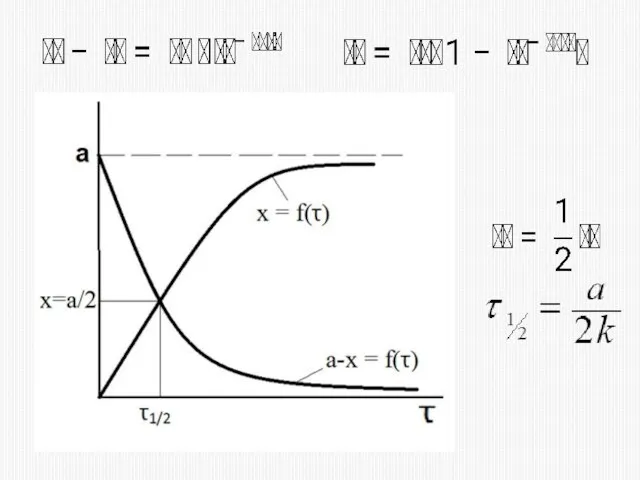
- 33. 2) МЕТОД ВРЕМЕНИ ПОЛУПРЕВРАЩЕНИЯ
- 39. 3) МЕТОД ОСТВАЛЬДА-НОЙЕСА
- 40. метод избытка или изоляции (графический метод Оствальда-Нойеса) метод Вант-Гоффа ДИФФЕРЕНЦИАЛЬНЫЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ ПОРЯДКА РЕАКЦИИ
- 41. 1) МЕТОД ИЗБЫТКА (ИЗОЛЯЦИИ)
- 44. Скачать презентацию





















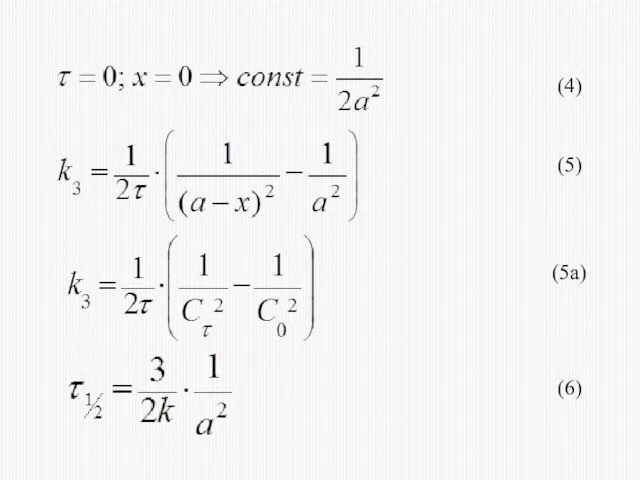


















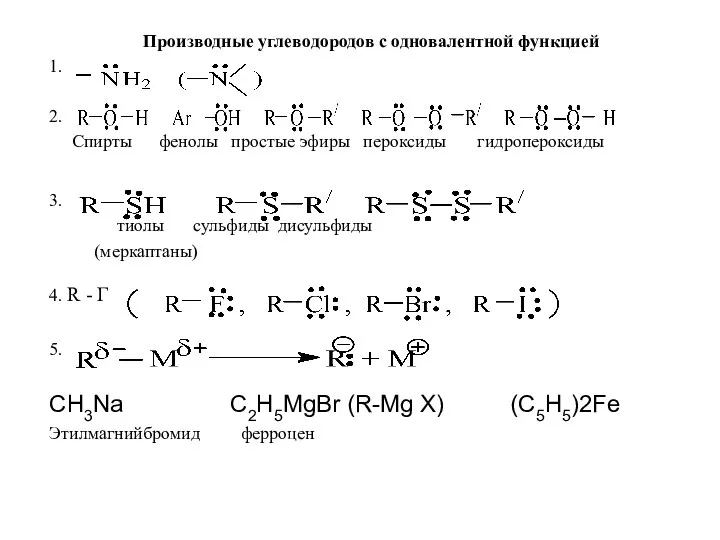 Производные углеводородов с одновалентной функцией
Производные углеводородов с одновалентной функцией Introduction to Periodic Table
Introduction to Periodic Table Нафта
Нафта  Физико-химические методы анализа
Физико-химические методы анализа Термохимия. Расчетные задачи. (Лекция 4.2)
Термохимия. Расчетные задачи. (Лекция 4.2) Старение полимеров. Процессы, протекающие при старении полимеров
Старение полимеров. Процессы, протекающие при старении полимеров Поверхностное натяжение. Поверхности раздела фаз
Поверхностное натяжение. Поверхности раздела фаз Твердые растворы Zn1,92-2хMg0,08Mn2xSiO4 и Zn1,76-2хMg0,24Mn2xSiO4: синтез и спектроскопические свойства
Твердые растворы Zn1,92-2хMg0,08Mn2xSiO4 и Zn1,76-2хMg0,24Mn2xSiO4: синтез и спектроскопические свойства Мұнайдың құрамындағы тұз мөлшерін анықтау
Мұнайдың құрамындағы тұз мөлшерін анықтау Синтетические лекарственные препараты
Синтетические лекарственные препараты Курс химии для основных академических направлений подготовки специалистов НИЯУ МИФИ
Курс химии для основных академических направлений подготовки специалистов НИЯУ МИФИ Рекомендации по подготовке учащихся к выполнению заданий различного уровня сложности ЕГЭ по химии
Рекомендации по подготовке учащихся к выполнению заданий различного уровня сложности ЕГЭ по химии СИБИРСКИЙ ФЕДЕРАЛЬНЫЙ УНИВЕРСИТЕТ Институт Нефти и Газа
СИБИРСКИЙ ФЕДЕРАЛЬНЫЙ УНИВЕРСИТЕТ Институт Нефти и Газа  Многоатомные спирты
Многоатомные спирты Презентация по Химии "Уран" - скачать смотреть
Презентация по Химии "Уран" - скачать смотреть  Горно-химическое сырье
Горно-химическое сырье Презентация по Химии "Волокнистые материалы вокруг нас" - скачать смотреть
Презентация по Химии "Волокнистые материалы вокруг нас" - скачать смотреть  Отношение масс элементов в веществе. Массовые доли элементов в веществе
Отношение масс элементов в веществе. Массовые доли элементов в веществе Химический состав клетки
Химический состав клетки Адам ағзасындағы химиялық элементтер
Адам ағзасындағы химиялық элементтер МОЛЕКУЛЯРНО - КИНЕТИЧЕСКАЯ ТЕОРИЯ идеального газа ОСНОВНЫЕ ПОЛОЖЕНИЯ МКТ. ИДЕАЛЬНЫЙ ГАЗ, ЕГО ПАРАМЕТРЫ. ОСНОВНОЕ УРАВНЕНИЕ МКТ.
МОЛЕКУЛЯРНО - КИНЕТИЧЕСКАЯ ТЕОРИЯ идеального газа ОСНОВНЫЕ ПОЛОЖЕНИЯ МКТ. ИДЕАЛЬНЫЙ ГАЗ, ЕГО ПАРАМЕТРЫ. ОСНОВНОЕ УРАВНЕНИЕ МКТ.  Органикалық қосылыстар
Органикалық қосылыстар Задачи Спирты. Альдегиды
Задачи Спирты. Альдегиды Калитина Тамара Михайловна учитель экологии, биологии МОУ СОШ №3 и учитель химии МОУ СОШ №2 с.Александров-Гай Саратовской области
Калитина Тамара Михайловна учитель экологии, биологии МОУ СОШ №3 и учитель химии МОУ СОШ №2 с.Александров-Гай Саратовской области  Автометаморфизм
Автометаморфизм Повышение эффективности разработки низкопродуктивных коллекторов самотлорского месторождения
Повышение эффективности разработки низкопродуктивных коллекторов самотлорского месторождения Диссоциация кислот, оснований и солей
Диссоциация кислот, оснований и солей Природные полимеры и продукты их химических превращений
Природные полимеры и продукты их химических превращений