Содержание
- 2. Опыт. В стеклянном стакане смешивают равные объемы растворов нитрата свинца (II) и йодида калия. Сразу же
- 3. Комплексные соединения - устойчивые химические соединения сложного состава, в которых обязательно имеется хотя бы одна связь,
- 5. Положения координационной теории Вернера в центре комплексного соединения находится центральный ион – комплексообразователь. Комплексообразователь (центральный атом)
- 7. Вокруг центрального иона-комплексообразователя находятся противоположно заряженные ионы или нейтральные молекулы, которые называются лигандами (от латинского "ligare"
- 8. Комплексные соединения - это соединения, которые содержат катионный, анионный или нейтральный комплекс, состоящий из центрального атома
- 9. Заряд комплексного иона равен алгебраической сумме зарядов иона-комплексообразователя и лигандов. 2+ 0 2+ 2- [Cu(NH3)4] SO4
- 10. ЦЕНТРАЛЬНЫЙ АТОМ (ион-комплексообразователь) Ионами –коплексообразователями являются катионы металлов, а также некоторые неметаллы, например В, Р, Si.
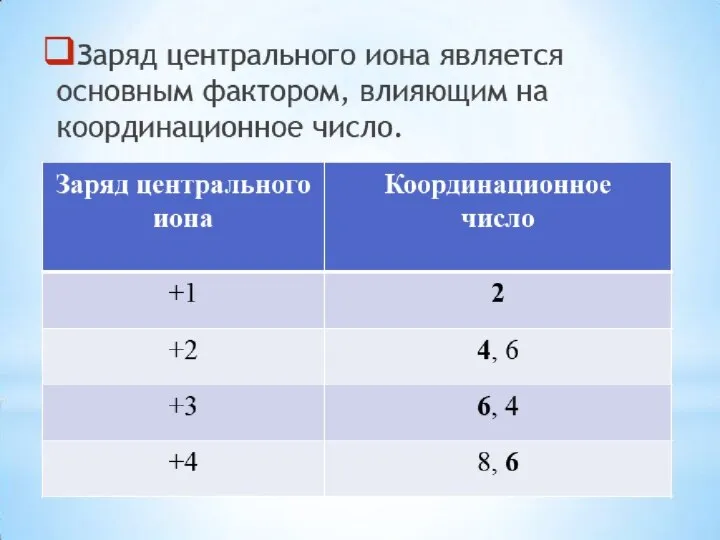
- 12. Координационное число не является неизменной величиной. Даже для одних и тех же комплексообразователей и лигандов координационное
- 13. ЛИГАНДЫ - молекулы или ионы, которые являются донорами электронных пар и непосредственно связаны с комплексообразователем. Лигандами
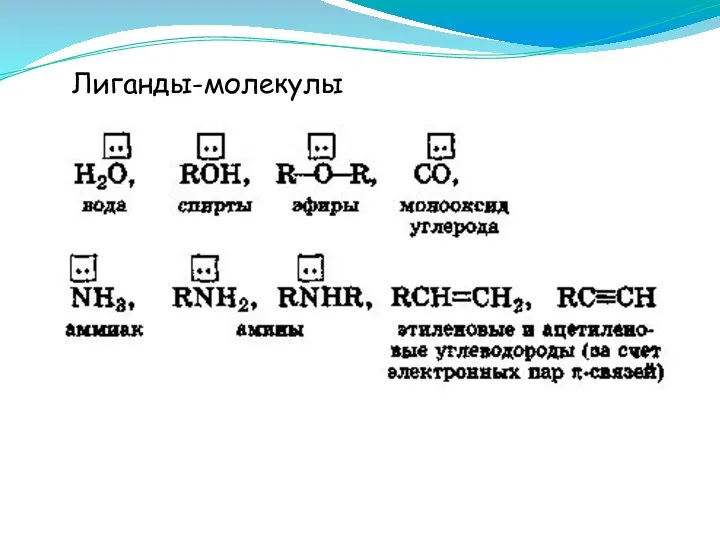
- 14. Лиганды-молекулы
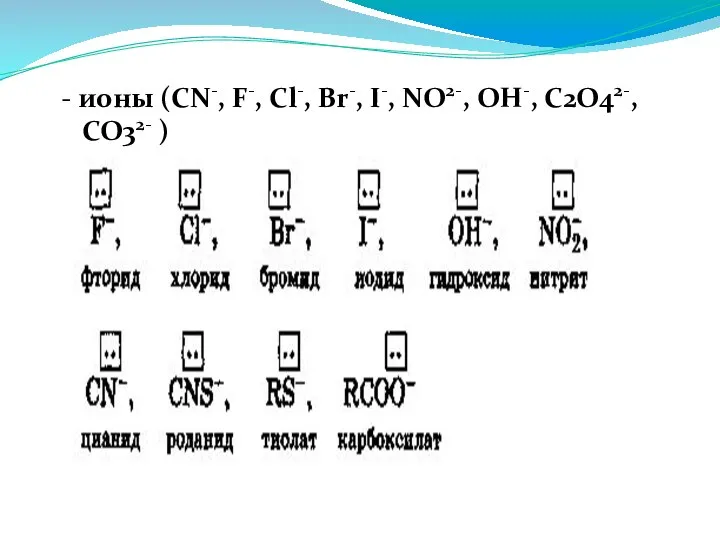
- 15. - ионы (CN-, F-, Cl-, Br-, I-, NO2-, OH-, C2O42-, CO32- )
- 16. Дентатность лиганда определяется числом координационных мест, занимаемых лигандом в координационной сфере комплексообразователя. Различают монодентатные лиганды, занимающие
- 20. Природа химической связи в комплексных соединениях Во внутренней сфере между комплексообразователем и лигандами существуют ковалентные связи,
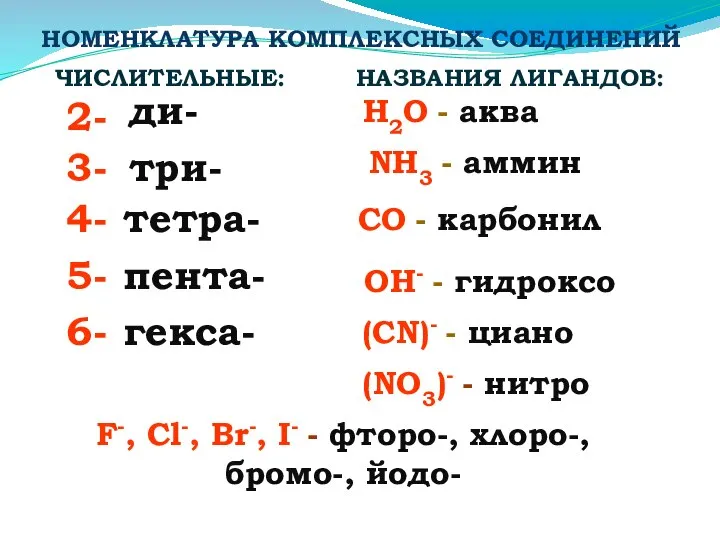
- 23. НОМЕНКЛАТУРА КОМПЛЕКСНЫХ СОЕДИНЕНИЙ 2- 4- 3- 5- 6- ди- три- тетра- пента- гекса- ЧИСЛИТЕЛЬНЫЕ: НАЗВАНИЯ ЛИГАНДОВ:
- 24. НОМЕНКЛАТУРА КОМПЛЕКСНЫХ СОЕДИНЕНИЙ НАЗВАНИЯ комплексообразователей (лат.): Fe - феррат Cu - купрат Ag - аргентат Au
- 25. Соль содержит комплексный катион [Cо(NH3)4Cl2]Cl -называют анион соли (хлорид); -называют входящие во внутреннюю сферу лиганды-анионы с
- 26. Соль содержит комплексный анион K4[Fe(CN)6] -называют лиганды-анионы с окончанием на «о» с указанием их количества (гексациано);
- 27. Нейтральный комплекс [Co2(CO)8] -названия комплексов без внешней сферы состоят из одного слова; -указывается число и названия
- 28. тетра гидроксо цинкат НОМЕНКЛАТУРА КОМПЛЕКСНЫХ СОЕДИНЕНИЙ Na+2 4] (OH)- [Zn+2 натрия [Cr+3 (H2O)0 6] Cl-3 хлорид
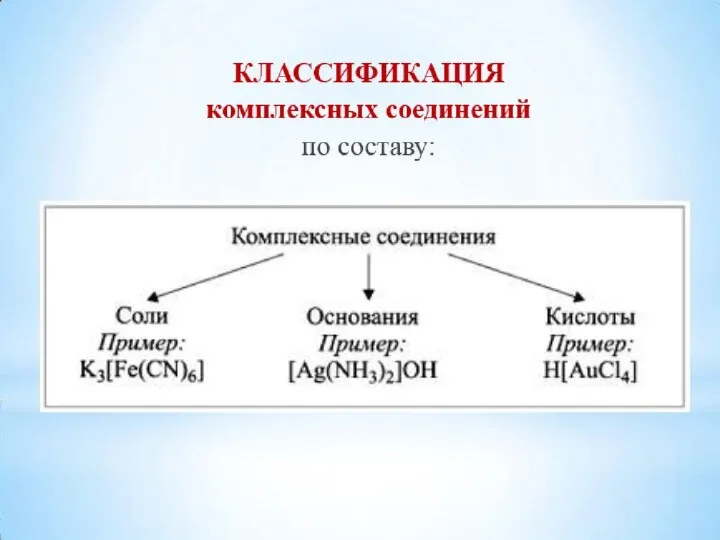
- 29. Классификация комплексных соединений по разным признакам 1. По знаку электрического заряда комплекса 2. Принадлежности к определённому
- 30. 2. По принадлежности к определённому классу соединений комплексные диамминсеребро(I) гидрооксид кислоты основания соли H[AuCl4] [Ag(NH3)2]OH K2[HgI4]
- 31. По природе лиганда 1) Аммиакаты — комплексы, в которых лигандами служат молекулы аммиака, например: [Cu(NH3)4]SO4, [Co(NH3)6]Cl3,
- 32. 4) Ацидокомплексы — комплексы, в которых лигандами являются кислотные остатки. K2[PtCl4], H2[CoCl4], H2[SiF6]. 5) Гидроксокомплексы —
- 38. Чем меньше константа диссоциации, тем устойчивее комплекс. Чем больше константа устойчивости, тем устойчивее комплекс. На прочность
- 41. В живых организмах в полидентных лигандах донорные атомы связаны в единое кольцо-цикл. - порфирины [железо в
- 42. Порфирин
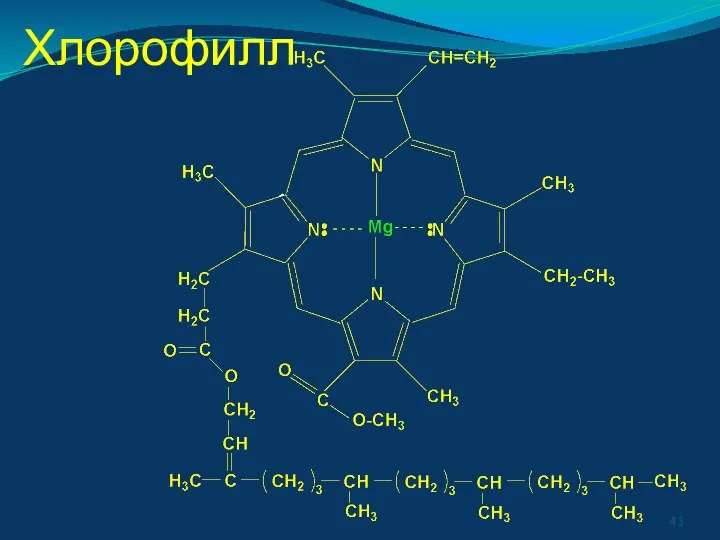
- 43. Хлорофилл
- 44. Гемоглобин
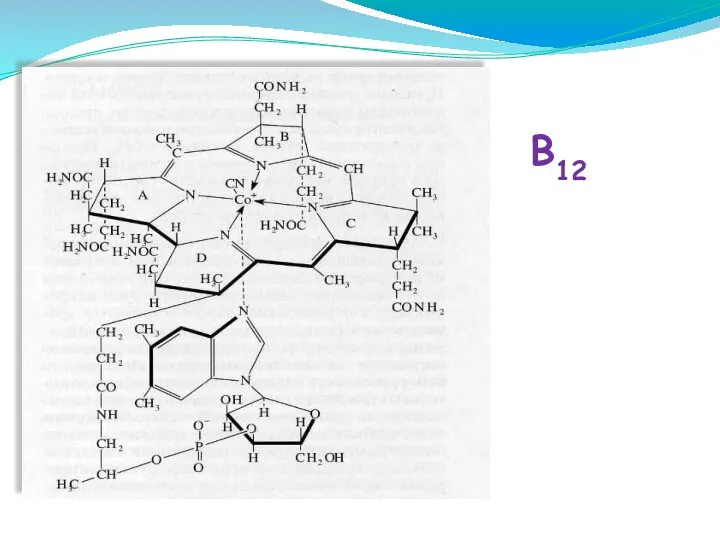
- 45. B12
- 46. Полидентные лиганды связываются с ионами металла гораздо сильнее, чем монодентные с теми же донорными атомами [прочность
- 47. ……. Изомерия комплексных соединений. 1. Сольватная [гидратная]: различие в распределении воды во внутренней и внешней сфере:
- 48. Комплексообразователи и лиганды нашего организма. Ca 2+ - [Na+ и К+] присутствуют в основном в свободном
- 49. Общие понятия об активном центре металлоферментов. ферменты представляют собой комплексные соединения с металлами, ионы которых определяют
- 50. Значение комплексов в медицине. Биохимик Дж.Вуд писал:. Биохимия — это координационная химия живых систем». В медицине
- 52. Скачать презентацию



















![Соль содержит комплексный катион [Cо(NH3)4Cl2]Cl -называют анион соли (хлорид); -называют входящие](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1366721/slide-24.jpg)
![Соль содержит комплексный анион K4[Fe(CN)6] -называют лиганды-анионы с окончанием на «о»](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1366721/slide-25.jpg)
![Нейтральный комплекс [Co2(CO)8] -названия комплексов без внешней сферы состоят из одного](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1366721/slide-26.jpg)
![тетра гидроксо цинкат НОМЕНКЛАТУРА КОМПЛЕКСНЫХ СОЕДИНЕНИЙ Na+2 4] (OH)- [Zn+2 натрия](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1366721/slide-27.jpg)


![4) Ацидокомплексы — комплексы, в которых лигандами являются кислотные остатки. K2[PtCl4],](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1366721/slide-31.jpg)












![……. Изомерия комплексных соединений. 1. Сольватная [гидратная]: различие в распределении воды](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1366721/slide-46.jpg)
![Комплексообразователи и лиганды нашего организма. Ca 2+ - [Na+ и К+]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1366721/slide-47.jpg)


 Природа активності та кислотності цеолітних каталізаторів
Природа активності та кислотності цеолітних каталізаторів Кристаллические решетки
Кристаллические решетки Электронное строение атома
Электронное строение атома Нуклеиновые кислоты
Нуклеиновые кислоты Электронное строение атома. Лекция № 2
Электронное строение атома. Лекция № 2 Марганец и его свойства
Марганец и его свойства Обратимость химических реакций. Химическое равновесие
Обратимость химических реакций. Химическое равновесие Практическая работа № 3. Получение, собирание и распознавание газов
Практическая работа № 3. Получение, собирание и распознавание газов Алкины. Гомологический ряд
Алкины. Гомологический ряд Презентация по Химии "Бензини" - скачать смотреть бесплатно
Презентация по Химии "Бензини" - скачать смотреть бесплатно Алкены – непредельные углеводороды
Алкены – непредельные углеводороды Контроль качества неорганических лекарственных средств элементов VII группы периодической системы Д. И. Менделеева
Контроль качества неорганических лекарственных средств элементов VII группы периодической системы Д. И. Менделеева Каталітичні процеси нафтопереробки
Каталітичні процеси нафтопереробки МОУ СОШ №5 ст.Бриньковская УРОК ПО ТЕМЕ: «ЧИСТАЯ ВОДА» подготовила учитель химии Беба Е.А.
МОУ СОШ №5 ст.Бриньковская УРОК ПО ТЕМЕ: «ЧИСТАЯ ВОДА» подготовила учитель химии Беба Е.А.  Алкени
Алкени Күрделі липидтер.Сабынданбайтын липидтер (стериндер, стероидтар) және олардың биологиялық маңызы. Терпендер
Күрделі липидтер.Сабынданбайтын липидтер (стериндер, стероидтар) және олардың биологиялық маңызы. Терпендер Карбоновые кислоты и их функциональные производные
Карбоновые кислоты и их функциональные производные Цепная сополимеризация
Цепная сополимеризация Неметаллы
Неметаллы Классификация веществ, вызывающих отравление. (Тема 4)
Классификация веществ, вызывающих отравление. (Тема 4) Углеводы
Углеводы Экоаналитический контроль воздуха
Экоаналитический контроль воздуха Реакция Бэйлиса Хиллмана-Мориты
Реакция Бэйлиса Хиллмана-Мориты Термодинамика фазовых превращений
Термодинамика фазовых превращений ДОСЛІДЖЕННЯ ДОСЛІДЖЕННЯ НАЙМАСОВІШИХ КУПАННЯ смт
ДОСЛІДЖЕННЯ ДОСЛІДЖЕННЯ НАЙМАСОВІШИХ КУПАННЯ смт XXI ғасыр көшбасшысы
XXI ғасыр көшбасшысы Рівняння характеристики крупності
Рівняння характеристики крупності IV,III группа периодической системы Д..И. Менделеева. Кислота борная, натрия гидрокарбонат
IV,III группа периодической системы Д..И. Менделеева. Кислота борная, натрия гидрокарбонат