Содержание
- 3. Провал электронов Cr, Cu, Nb, Mo, Ru, Rh, Ag, Pt, Au
- 4. d-Элементы
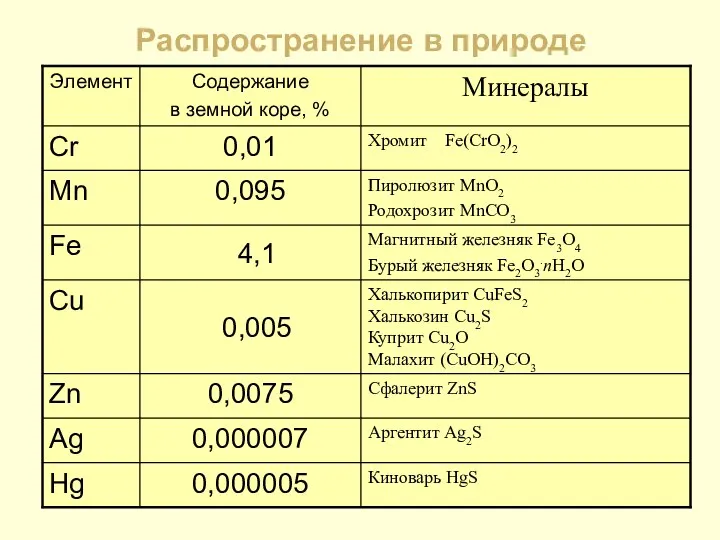
- 5. Распространение в природе
- 6. М и н е р а л ы Лимонит Fe2O3∙nH2O Магнетит Fe3O4 Сфалерит ZnS Смитсонит ZnCO3
- 7. Минералы Малахит (CuOH)2CO3 Крокоит PbCrO4 Хромит (Fe,Cr2)O4
- 8. Минералы Киноварь HgS Пиролюзит MnO2 Серебро Ag
- 9. Параметры d-элементов
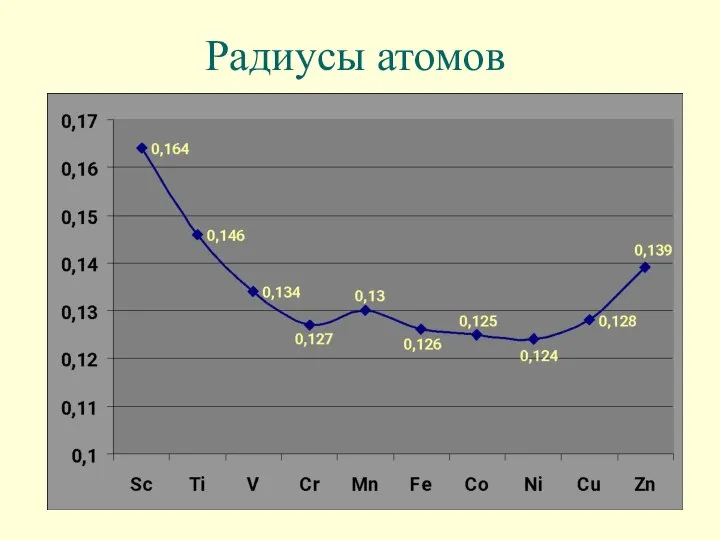
- 10. Радиусы атомов
- 11. Радиусы атомов, нм Лантаноидное f-сжатие
- 12. Орбитальные радиусы атомов, пм
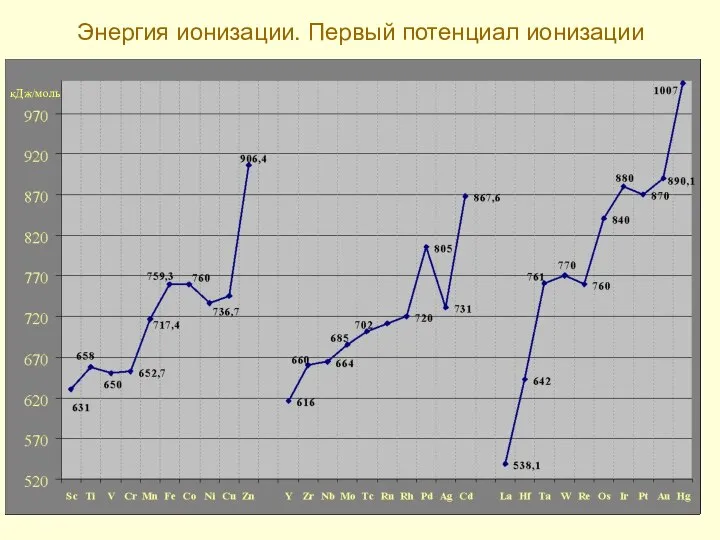
- 13. Энергия ионизации. Первый потенциал ионизации кДж/моль
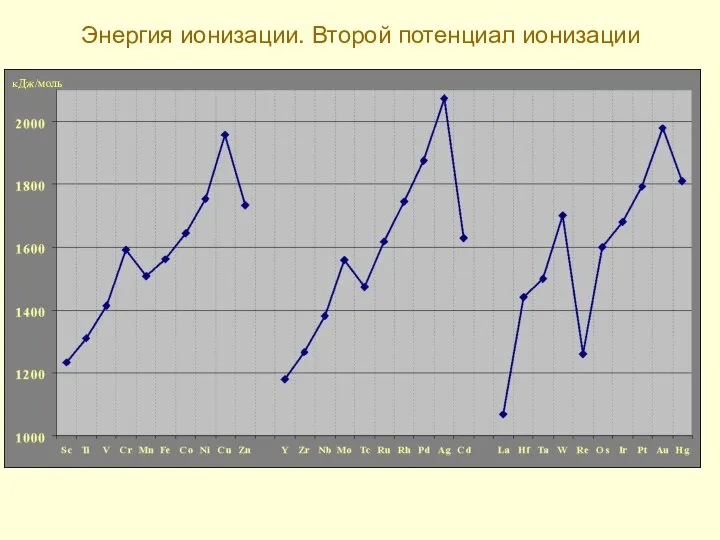
- 14. Энергия ионизации. Второй потенциал ионизации кДж/моль
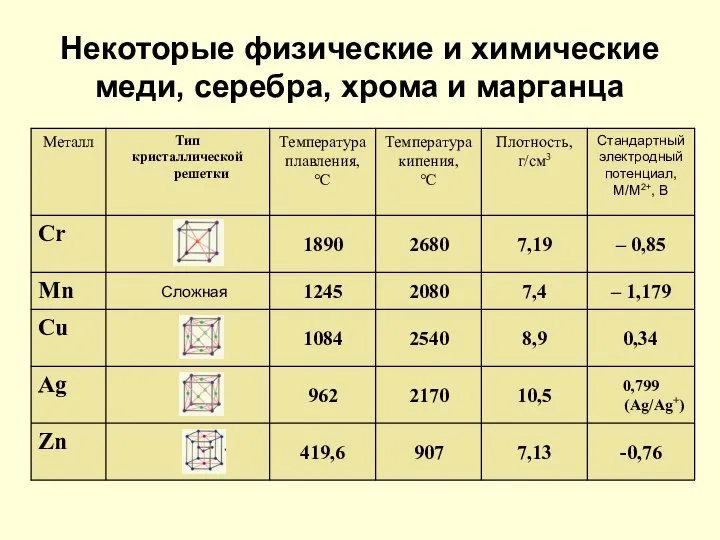
- 16. Некоторые физические и химические меди, серебра, хрома и марганца
- 17. Температуры плавления 3d °С
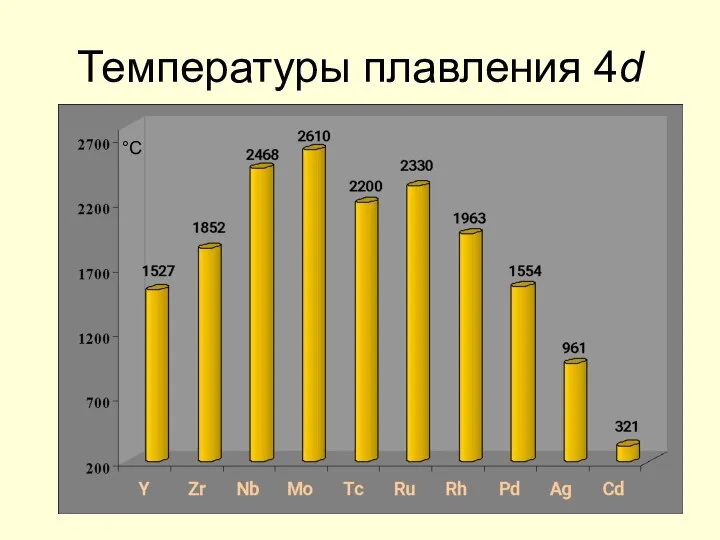
- 18. Температуры плавления 4d °С
- 19. Температуры плавления 5d °С
- 20. Плотность 3d
- 21. Плотность 4d
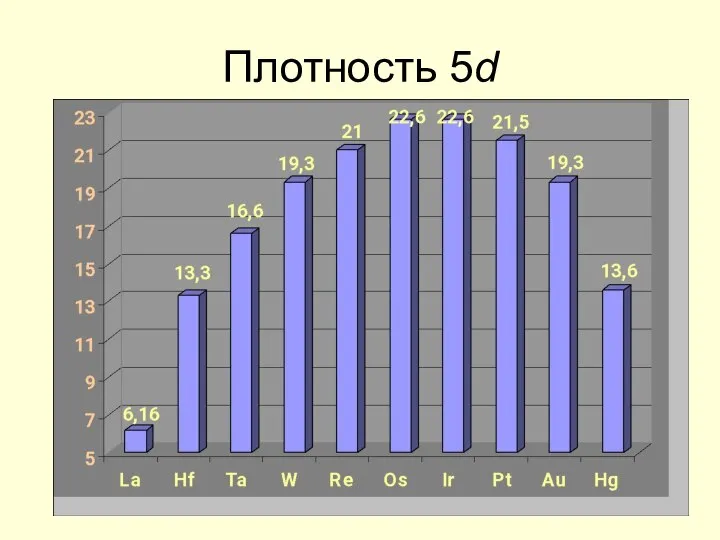
- 22. Плотность 5d
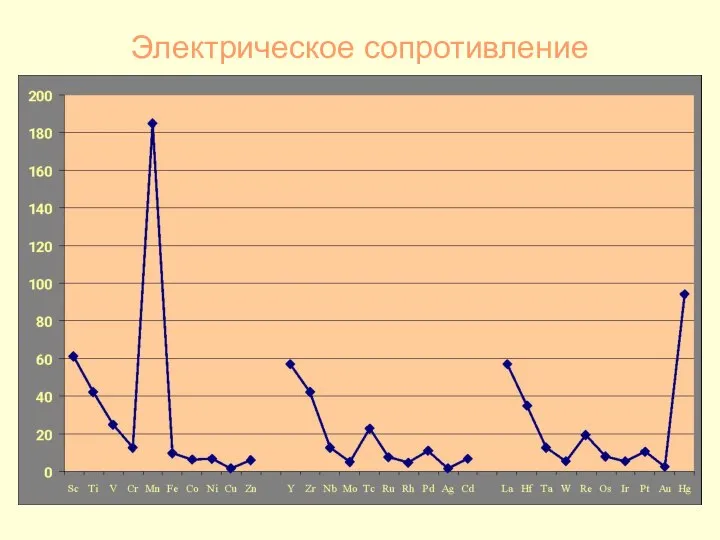
- 23. Электрическое сопротивление
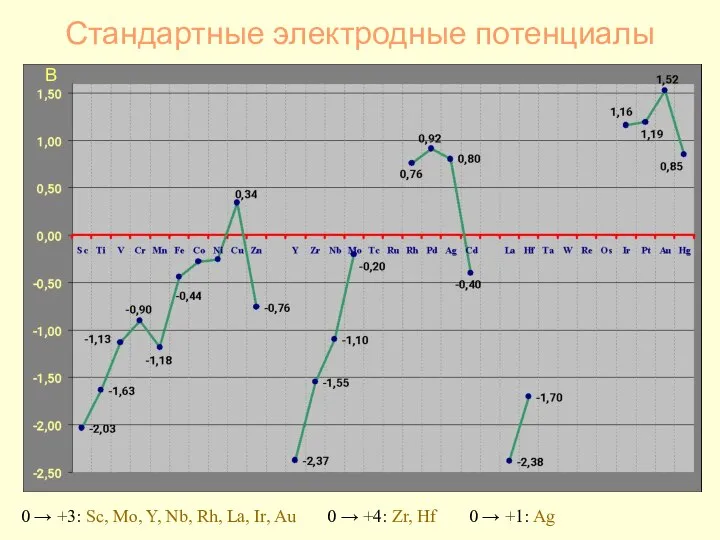
- 24. Стандартные электродные потенциалы В 0 → +3: Sc, Mo, Y, Nb, Rh, La, Ir, Au 0
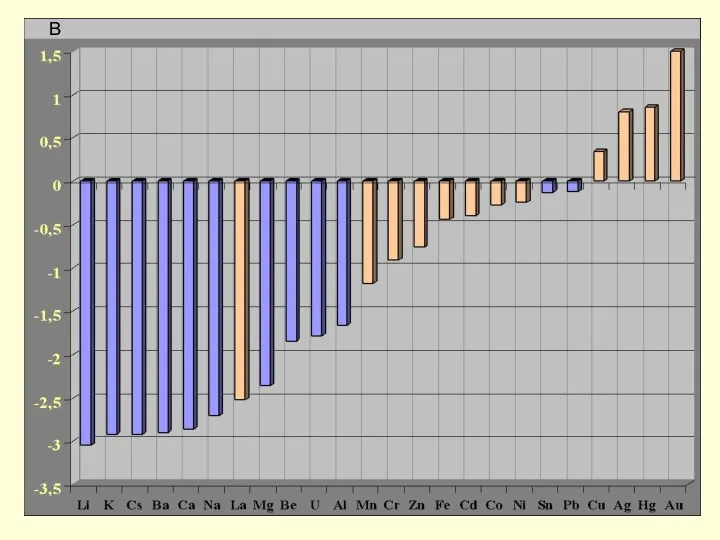
- 25. В
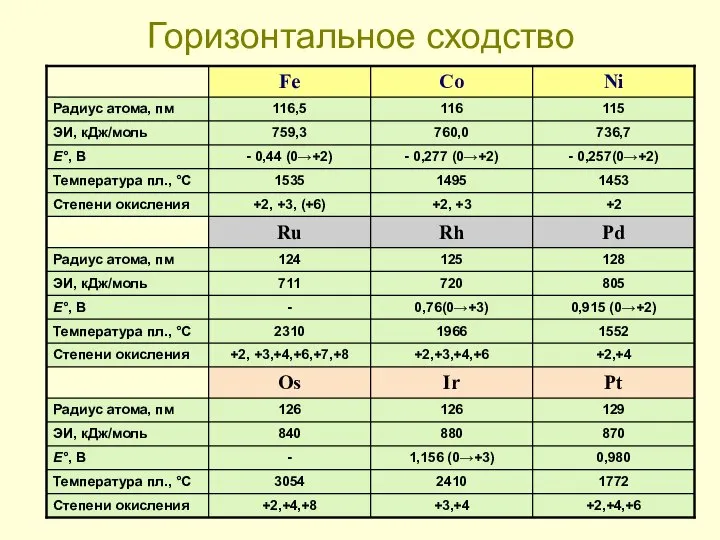
- 26. Горизонтальное сходство
- 27. Устойчивость высшей степени окисления 4Cr(порошок) + 3O2 = 2Cr2O3 (медленно) 2Mo + 3O2 = 2MoO3 (600-700
- 28. Химические свойства меди 2Cu + O2 = 2CuO Cu + Cl2 = CuCl2 2Cu + S
- 29. Химические свойства серебра 2Ag + Cl2 = 2AgCl 2Ag + S = Ag2S 2Ag + 2H2SO4
- 30. Химические свойства цинка Zn + H2O (пар) = ZnO + H2 Zn + 2HCl = ZnCl2
- 31. Химические свойства ртути 2Hg + 2H2SO4 = Hg2SO4 + SO2 + 2H2O Hg + 2H2SO4 =
- 32. Химические свойства хрома Cr + H2SO4 (разб.) = CrSO4 + H2↑ 4Cr (порошок) + 3O2 =
- 33. Химические свойства марганца Mn + Cl2 = MnCl2 Mn + O2 = MnO2 Mn + S
- 34. Символы металлов, которые не реагируют с конц. азотной кислотой, выделены жирным шрифтом
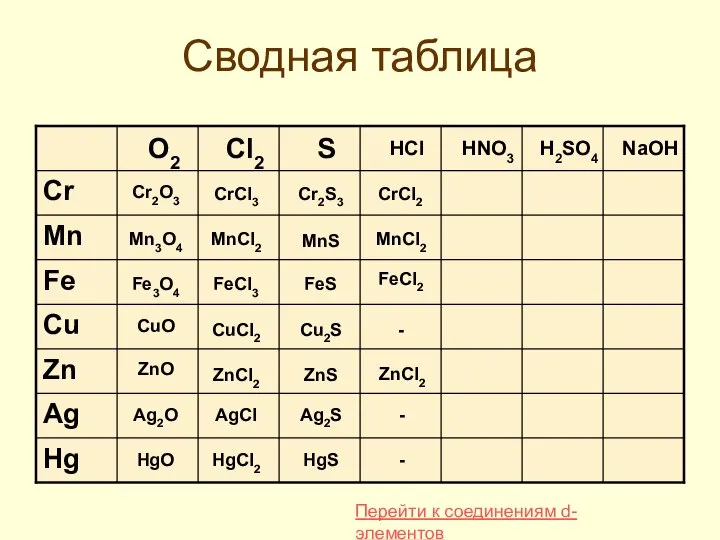
- 35. Сводная таблица Cr2O3 Mn3O4 Fe3O4 CuO ZnO Ag2O HgO CrCl3 MnCl2 FeCl3 CuCl2 ZnCl2 AgCl HgCl2
- 36. Окраска высших оксидов d-элементов
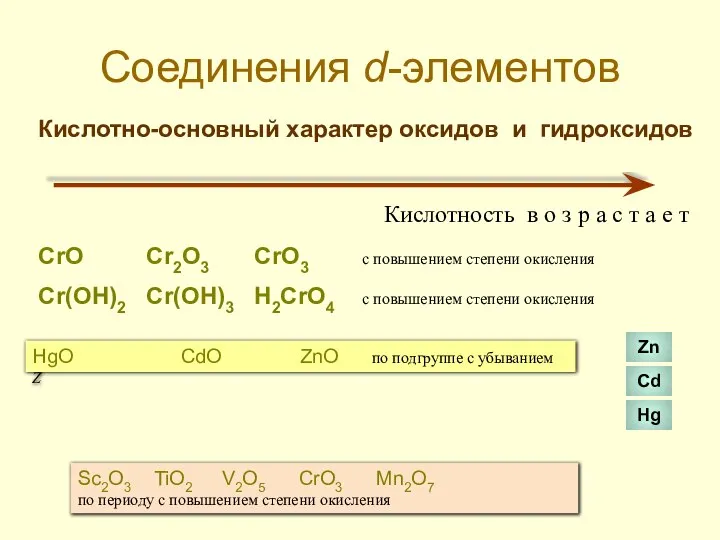
- 37. Соединения d-элементов Кислотно-основный характер оксидов и гидроксидов Кислотность в о з р а с т а
- 38. Соединения меди Cu(OH)2 + 2H+ = Cu2+ + 2H2O Cu(OH)2 + 2OH– = [Cu(OH)4]2– Сульфат меди(II)
- 39. Полезная информация к практикуму 2Cu2+ + [Fe(CN)6]4- = Cu2[Fe(CN)6]↓ Cu2+ + S2- = CuS↓ CuS +
- 40. Соединения серебра Степени окисления серебра +1, +2, +3 Ag2O 2AgNO3 + 2NaOH = Ag2O↓ +2NaNO3 +
- 41. Соединения хрома Хром был открыт в минерале крокоите PbCrO4 Луи Вокленом в 1797 г.
- 42. Соединения хрома Cr(OH)2 + 2H+ = Cr2+ + 2H2O 4CrCl2 + 4HCl + O2 = 4CrCl3
- 43. Соединения марганца MnCO3 = MnO + CO2↑ MnO2 + H2 = MnO + H2O MnO +
- 44. Окислительные свойства перманганата 2KMnO4 + 5K2SO3 + 3H2SO4 = 2MnSO4 + 6K2SO4 + 3H2O 2KMnO4 +
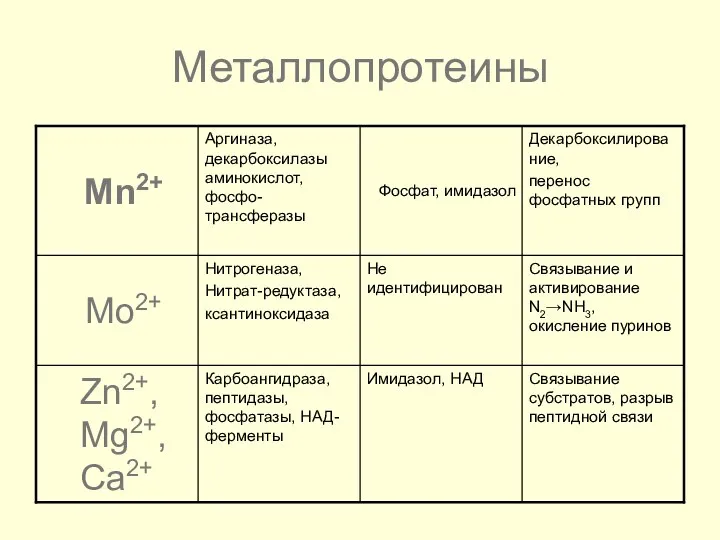
- 45. Металлопротеины
- 46. Металлопротеины
- 47. Применение
- 49. Скачать презентацию
























![Полезная информация к практикуму 2Cu2+ + [Fe(CN)6]4- = Cu2[Fe(CN)6]↓ Cu2+ +](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1400681/slide-38.jpg)







 Биологическое окисление
Биологическое окисление Симметрия кристаллических решеток
Симметрия кристаллических решеток Нітрати в продуктах харчування
Нітрати в продуктах харчування  Аллотропные модификации
Аллотропные модификации Проектная деятельность школьников в процессе обучения химии
Проектная деятельность школьников в процессе обучения химии Мінеральні добрива Хімія, 10 клас Розробила вчитель сзш №213 Деснянського р-ну м. Києва Мартиненко О.А.
Мінеральні добрива Хімія, 10 клас Розробила вчитель сзш №213 Деснянського р-ну м. Києва Мартиненко О.А.  Уран. Применение. Ядерное топливо
Уран. Применение. Ядерное топливо Презентация к уроку химии по теме «Спирты» 10 класс. УМК Габриеляна О.С. Базовый уровень
Презентация к уроку химии по теме «Спирты» 10 класс. УМК Габриеляна О.С. Базовый уровень Соли. Классификация сложных неорганических веществ
Соли. Классификация сложных неорганических веществ Epoxy-Based Fibre Reinforced Nanocomposites
Epoxy-Based Fibre Reinforced Nanocomposites Сера, сероводород, сульфиды
Сера, сероводород, сульфиды Химия элементов. Лекция 6 Комплексные соединения: типы и классификация. Методы получения и разрушения. Решение задач.
Химия элементов. Лекция 6 Комплексные соединения: типы и классификация. Методы получения и разрушения. Решение задач.  Радиофармацевтическая химия
Радиофармацевтическая химия Век медный, бронзовый, железный. Химические элементы металлы
Век медный, бронзовый, железный. Химические элементы металлы Характеристика химического элемента
Характеристика химического элемента Мыло. Мылящие вещества в природе
Мыло. Мылящие вещества в природе Ферменты. Размеры ферментов и их строение
Ферменты. Размеры ферментов и их строение Vodík
Vodík Скло, його різновиди та застосування Робота Учениці 10-А класу Баранюк Надії
Скло, його різновиди та застосування Робота Учениці 10-А класу Баранюк Надії  Проектная работа. Косметика своими руками
Проектная работа. Косметика своими руками Серная кислота и её свойства
Серная кислота и её свойства Презентация по Химии "Полімери" - скачать смотреть бесплатно
Презентация по Химии "Полімери" - скачать смотреть бесплатно Хімічні зв’язки Алмакаева 8-Б
Хімічні зв’язки Алмакаева 8-Б  Золото и серебро
Золото и серебро Химические волокна. Полиэфирные волокна. Лавсан
Химические волокна. Полиэфирные волокна. Лавсан Химические методы получения наночастиц
Химические методы получения наночастиц Выполнил: Лизунов Иван, 9Т
Выполнил: Лизунов Иван, 9Т Окислительно – восстановительные реакции. Раева Анна Семеновна Учитель химии МОБУ СОШ № 24 имени С. И. Климакова, г. Якутск
Окислительно – восстановительные реакции. Раева Анна Семеновна Учитель химии МОБУ СОШ № 24 имени С. И. Климакова, г. Якутск