Содержание
- 2. Метали (від лат. metallum - шахта, рудник): група елементів, що має характерні металеві властивості, такі як
- 3. Розташування металів в періодичній системі Якщо в періодичній системі елементів Д. І. Менделєєва провести діагональ від
- 4. З 118 хімічних елементів, відкритих на даний момент (з них не все офіційно визнані), до металам
- 5. Атоми металів легко віддають електрони зовнішнього електронного шару, перетворюючись в позитивні іони. Будова атомів металів Метали
- 6. Кристалічна структура металів Всі метали мають кристалічну будову. Розташовані тим або іншим способом атоми утворюють елементарну
- 7. Кристалічна структура металів + + + + + + + + + + + + -
- 8. Вміст металів у земній корі Металами є прості речовини більшості хімічних елементів (приблизно 80 % елементів
- 9. Платина Метеоритне залізо Золото Ртуть Срібло Осмій Мідь Паладій Метали у природі:
- 10. Червоний залізняк Залізний колчедан Сульфідна руда Боксити Хлорид натрію Халькопірит Хромна руда Нікелева руда Руди металів
- 11. Металургія - наука про методи і процеси виробництва металів із їх руд. Таку ж назву має
- 12. Cпособи добування металів
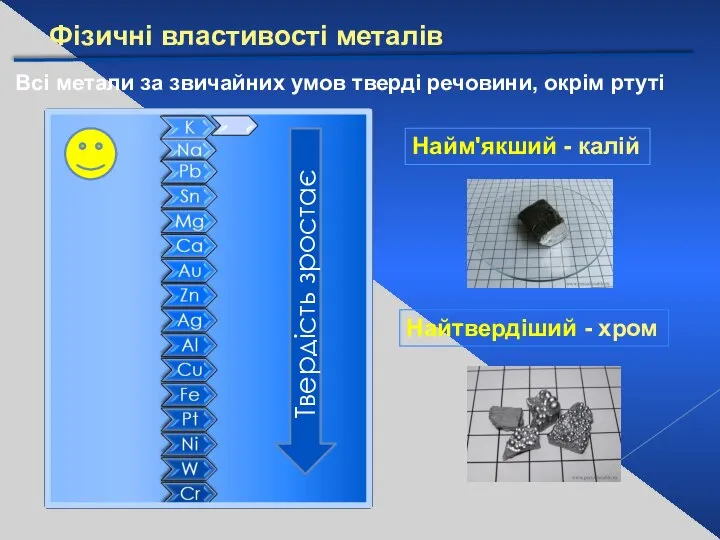
- 13. Фізичні властивості металів Всі метали за звичайних умов тверді речовини, окрім ртуті Найм'якший - калій Найтвердіший
- 14. Фізичні властивості металів Для всіх металів характерний металічний блиск обумовлюється їх здатністю сильно відбивати промені світла
- 15. Характерною властивістю металів є також пластичність Фізичні властивості металів Властивість під дією зовнішнього навантаження деформуватися, не
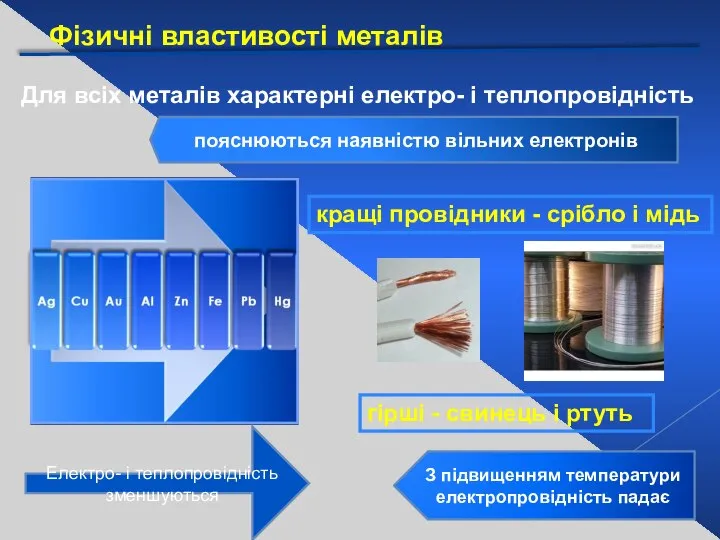
- 16. Фізичні властивості металів Для всіх металів характерні електро- і теплопровідність пояснюються наявністю вільних електронів Електро- і
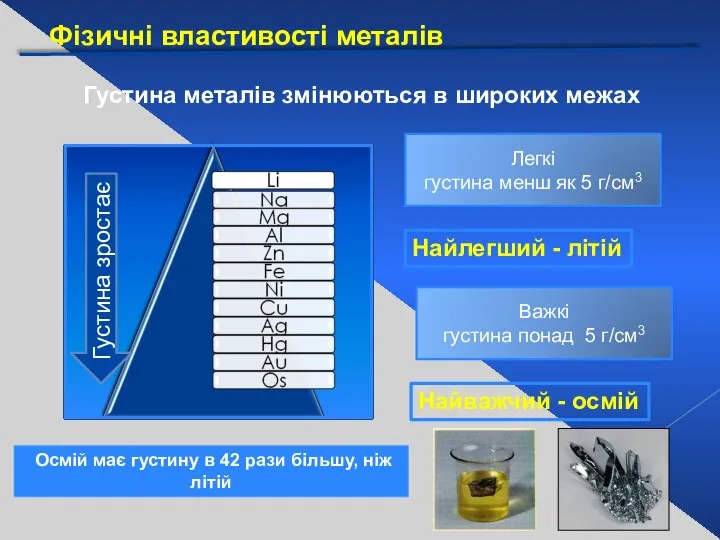
- 17. Фізичні властивості металів Густина металів змінюються в широких межах Густина зростає Легкі густина менш як 5
- 18. Фізичні властивості металів У великих інтервалах змінюються температури плавлення металів Найменша — у ртуті (—38,9 °С)
- 19. Хімічні властивості металів
- 20. Хімічні властивості металів Взаємодія металів з киснем: 2Na + О2 = Na2О2 2Сu+ О2 = 2СuО
- 21. Хімічні властивості металів Взаємодія металів з водою: 2Na + 2Н2О = 2NaОН + Н2 Na0 -1е
- 22. Хімічні властивості металів Взаємодія з кислотами: Взаємодія з солями: Zn + 2HCl → ZnCl2 + H2
- 23. КОРОЗІЯ – самочинне руйнування металів і сплавів внаслідок взаємодії їх з навколишнім середовищем Це окисно-відновна реакція,
- 24. За характером руйнівної дії Суцільна (загальна) корозія Місцева (локальна) корозія Охоплює всю поверхню металу Охоплює окремі
- 25. Залежно від механізму процесу ЕЛЕКТРО- ХІМІЧНА ХІМІЧНА руйнування металу внаслідок окиснення його окисниками, що містяться в
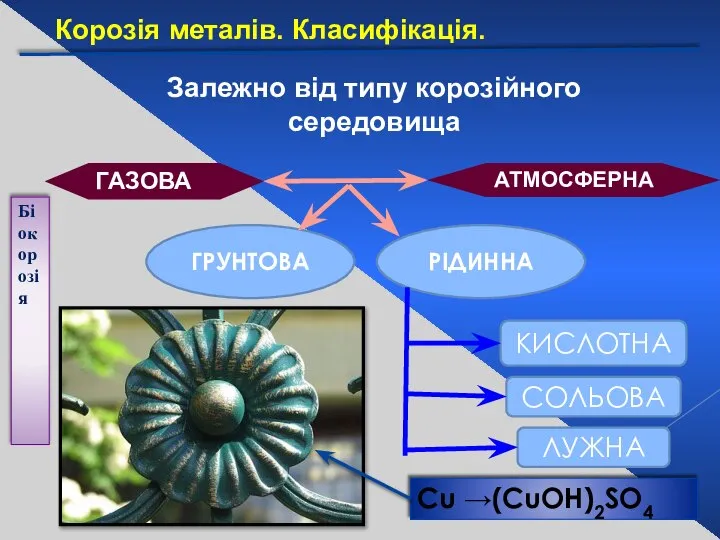
- 26. Залежно від типу корозійного середовища АТМОСФЕРНА ГАЗОВА ГРУНТОВА РІДИННА КИСЛОТНА СОЛЬОВА ЛУЖНА Біокорозія Сu →(CuOH)2SO4 Корозія
- 27. Механізм електрохімічної корозії ПОВІТРЯ
- 28. повітря Крапля води ІРЖА ЗАЛІЗО (анод) Механізм електрохімічної корозії ОЛОВО (катод)
- 29. Електрохімічна реакція Анод Катод Мінеральні поверхні Механізм електрохімічної корозії ЕЛЕКТРОЛІТ ПОВІТРЯ
- 30. Внаслідок корозії виходять з ладу обладнання, машини, механізми, руйнуються металеві конструкції Корозія металів завдає великої економічної
- 31. Методи захисту металів і сплавів від корозії Металічні (Zn,Sn,Cr,Pb,Ni) Неметалічні (лаки, фарби, емалі) Zn Ni Cr
- 32. Протекторний захист і електрозахист деталь Ел. струм Анод - протектор Створення сплавів з антикорозійними властивостями Методи
- 33. Галузі застосування металів Застосування металів Літако – машино- будування Металургія Атомна та ядерна енергетика Металеві захисні
- 34. СПЛАВИ - це матеріали з характерними властивостями, які складаються з двох або більше компонентів, з яких
- 35. Однорідними – при сплавленні утворюється розчин одного металу у іншому Неоднорідними – це механічна суміш металів
- 36. В металургії залізо и всі його сплави об’єднують в одну групу під назвою ЧОРНІ МЕТАЛИ інші
- 37. Сталь - сплав на основі заліза, який має менш 2% вуглецю. По хімічному складу сталі поділяють
- 38. Нержавіюча сталь використовується для виготовлення столових приборів, містить близько 12% хрому і до 10% нікелю. Нержавіючі
- 39. ДЮРАЛЮМІНІЙ – сплав на основі алюмінію, який містить Cu, Mg, Mn, Ni. Має добрі механічні властивості,
- 40. Щоб зберегти залізо від іржавіння, його деталі вкривають тонким шаром олова (лудіння). Занурюючи листове залізо у
- 41. Фізичні та хімічні властивості алюмінію зумовили його широке застосування в техніці. Значним споживачем алюмінію, є авіаційна
- 43. Скачать презентацию




































 Природа активності та кислотності цеолітних каталізаторів
Природа активності та кислотності цеолітних каталізаторів Кристаллические решетки
Кристаллические решетки Электронное строение атома
Электронное строение атома Нуклеиновые кислоты
Нуклеиновые кислоты Электронное строение атома. Лекция № 2
Электронное строение атома. Лекция № 2 Марганец и его свойства
Марганец и его свойства Обратимость химических реакций. Химическое равновесие
Обратимость химических реакций. Химическое равновесие Практическая работа № 3. Получение, собирание и распознавание газов
Практическая работа № 3. Получение, собирание и распознавание газов Алкины. Гомологический ряд
Алкины. Гомологический ряд Презентация по Химии "Бензини" - скачать смотреть бесплатно
Презентация по Химии "Бензини" - скачать смотреть бесплатно Алкены – непредельные углеводороды
Алкены – непредельные углеводороды Контроль качества неорганических лекарственных средств элементов VII группы периодической системы Д. И. Менделеева
Контроль качества неорганических лекарственных средств элементов VII группы периодической системы Д. И. Менделеева Каталітичні процеси нафтопереробки
Каталітичні процеси нафтопереробки МОУ СОШ №5 ст.Бриньковская УРОК ПО ТЕМЕ: «ЧИСТАЯ ВОДА» подготовила учитель химии Беба Е.А.
МОУ СОШ №5 ст.Бриньковская УРОК ПО ТЕМЕ: «ЧИСТАЯ ВОДА» подготовила учитель химии Беба Е.А.  Алкени
Алкени Күрделі липидтер.Сабынданбайтын липидтер (стериндер, стероидтар) және олардың биологиялық маңызы. Терпендер
Күрделі липидтер.Сабынданбайтын липидтер (стериндер, стероидтар) және олардың биологиялық маңызы. Терпендер Карбоновые кислоты и их функциональные производные
Карбоновые кислоты и их функциональные производные Цепная сополимеризация
Цепная сополимеризация Неметаллы
Неметаллы Классификация веществ, вызывающих отравление. (Тема 4)
Классификация веществ, вызывающих отравление. (Тема 4) Углеводы
Углеводы Экоаналитический контроль воздуха
Экоаналитический контроль воздуха Реакция Бэйлиса Хиллмана-Мориты
Реакция Бэйлиса Хиллмана-Мориты Термодинамика фазовых превращений
Термодинамика фазовых превращений ДОСЛІДЖЕННЯ ДОСЛІДЖЕННЯ НАЙМАСОВІШИХ КУПАННЯ смт
ДОСЛІДЖЕННЯ ДОСЛІДЖЕННЯ НАЙМАСОВІШИХ КУПАННЯ смт XXI ғасыр көшбасшысы
XXI ғасыр көшбасшысы Рівняння характеристики крупності
Рівняння характеристики крупності IV,III группа периодической системы Д..И. Менделеева. Кислота борная, натрия гидрокарбонат
IV,III группа периодической системы Д..И. Менделеева. Кислота борная, натрия гидрокарбонат