Содержание
- 2. Цели лекции: Обучающая - Сформировать знания о строении пептидов и белков и их биологической роли. Развивающая
- 3. План 1. Классификация пептидов и белков. Основные функции белков. 2. Пространственное строение пептидов и белков. 3.
- 4. 1. Классификация пептидов и белков
- 5. Белки и пептиды- полимерные азотсодержащие органические вещества состоящие из остатков аминокислот, соединенные пептидными связями, имеющие сложную
- 6. Классификация белков I. В зависимости от формы молекул белки подразделяются на фибриллярные и глобулярные. Молекулы фибриллярных
- 7. Классификация пептидов и белков. Глобулярные белки сложены в компактные глобулы. Водородные связи являются в основном внутримолекулярными,
- 8. Классификация пептидов и белков Строение белков определяет те функции, которые они выполняют в живых организмах. Фибриллярные
- 9. II. II. По составу белки делят на простые (неконъюгированные) и сложные (конъюгированные). По ряду характерных свойств
- 10. Простые белки: 1) Альбумины – растворимы в воде, не растворимы в конц. растворах солей. pl= 4,6-4,7.
- 11. коллагены - фибрилярные белки соединительной ткани. При длительном кипячении они растворяются в воде и при застудневании
- 12. Сложные белки : 1) Нуклеопротеины - содержат нуклеиновые кислоты. Наиболее изученными являются рибосомы, состоящие из нескольких
- 13. Гемопротеины - небелковый компонент этих протеидов - гем, построен из четырех пиррольных колец, с ними связан
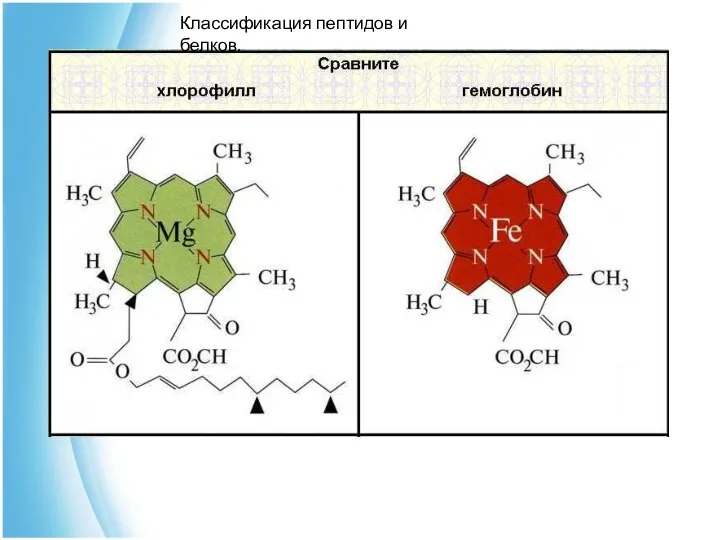
- 14. 3) Металлопротеины - в состав простетической группы входят металлы. Хлорофилл - содержит гем, но вместо железа
- 15. Классификация пептидов и белков.
- 16. Функции белков Ферментативная функция Структурная функция. Питательная функция. Защитная функция. Транспортная функция. Регуляторная функция. Запасающая функция.
- 17. 2. Пространственное строение пептидов и белков
- 18. Среди большого числа гипотез о строении молекулы белка лишь одна выдержала испытание временем: полипептидная теория строения
- 19. Уровни структурной организации белка первичная структура – аминокислотная последовательность вторичная структура – локальные высокоупорядоченные конформации белковой
- 20. Пространственное строение пептидов и белков
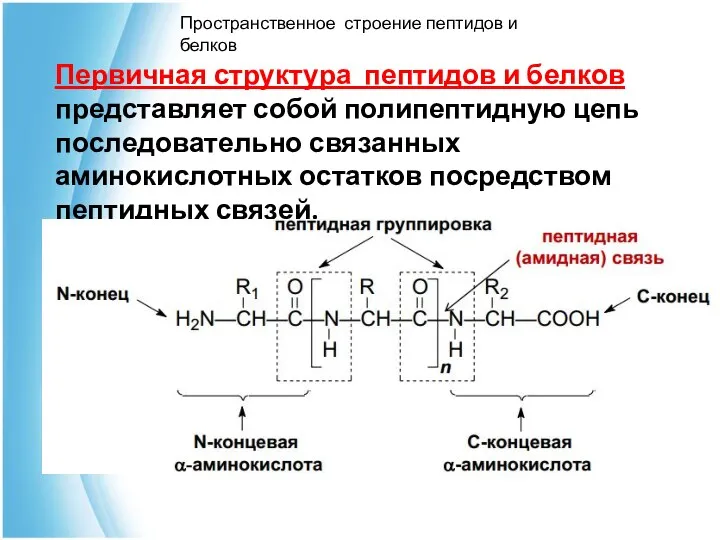
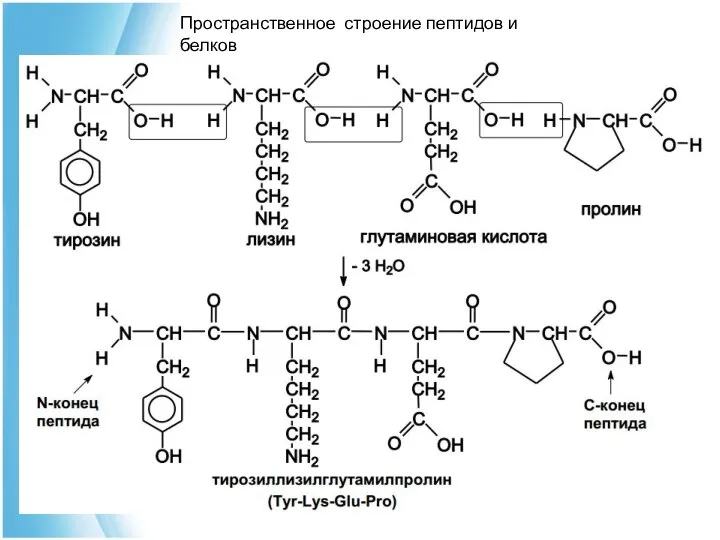
- 21. Пространственное строение пептидов и белков Первичная структура пептидов и белков представляет собой полипептидную цепь последовательно связанных
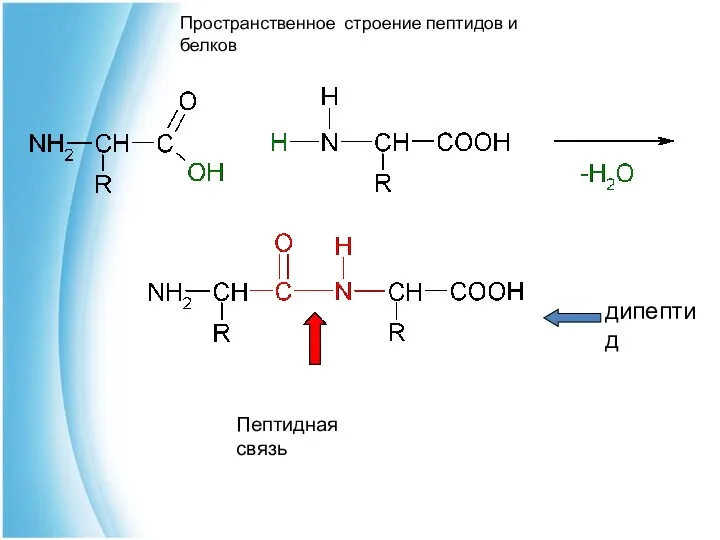
- 22. Пептидная связь дипептид Пространственное строение пептидов и белков
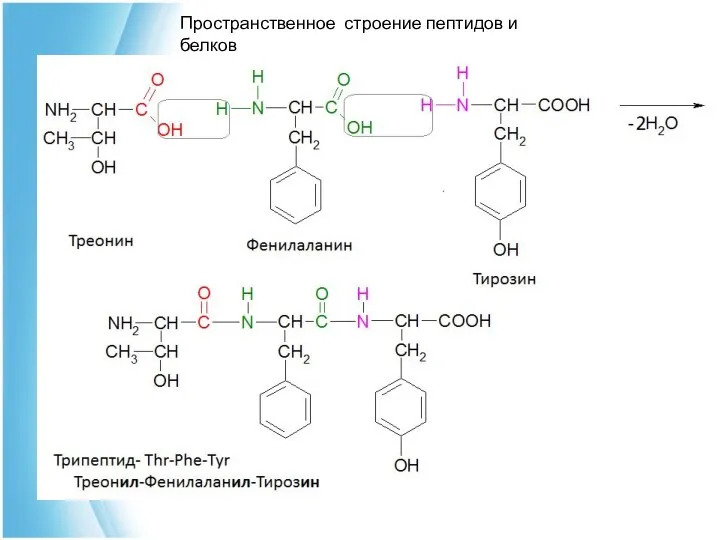
- 23. Пространственное строение пептидов и белков
- 24. Пространственное строение пептидов и белков
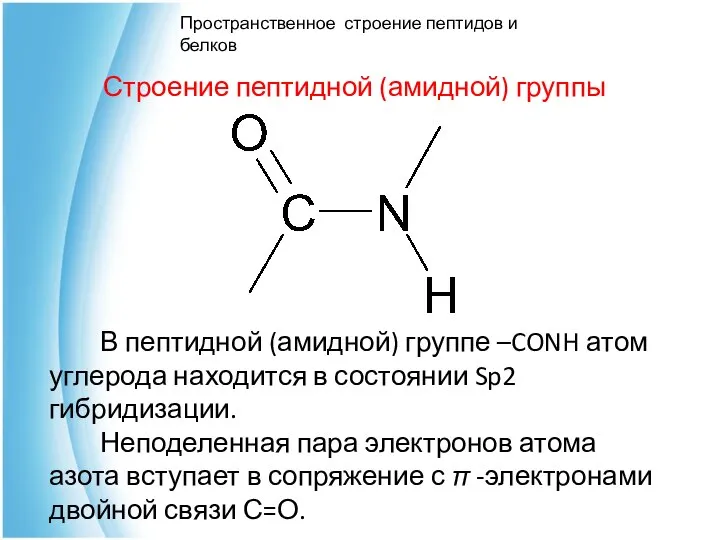
- 25. Строение пептидной (амидной) группы Пространственное строение пептидов и белков В пептидной (амидной) группе –CONH атом углерода
- 26. С позиций электронного строения пептидная группа представляет собой трехцентровую, р,π -сопряженную систему, электронная плотность в которой
- 27. Наличие плоской сопряженной системы в пептидной группе является причиной затруднения вращения вокруг связи C-N, а углеродные
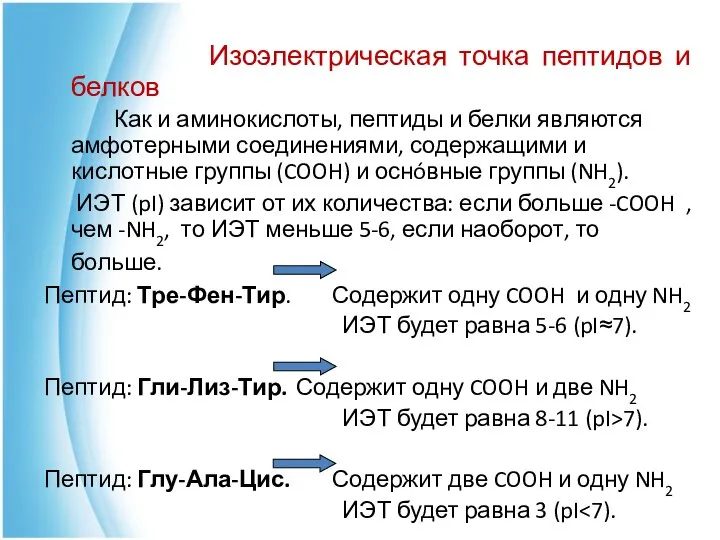
- 29. Изоэлектрическая точка пептидов и белков Как и аминокислоты, пептиды и белки являются амфотерными соединениями, содержащими и
- 30. Аминокислотная последовательность белков Первые исследования по выяснению аминокислотной последовательной белков были выполнены в Кембрижском университете Ф.Сенгером,
- 31. 20 аминокислот могут дать примерно 100000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000 белков, состоящих из 150 остатков аминокислот. Это астрономическое число –
- 32. Секвенирование биополимеров (белков и нуклеиновых кислот — ДНК и РНК) — определение их аминокислотной или нуклеотидной
- 33. Секвенирование ДНК Первичная структура любой белковой молекулы напрямую зависит от структуры ДНК-генома. Поэтому сначала выделяют ген,
- 34. Анализ первичной структуры пептидов Метод Эдмана Используя фенилизотиоцианат (Ph-NCS) последовательно отщепляют АК с N-конца и определяют
- 35. Фенилтиогидантоиновое производное N-концевой АК Пептид укороченный на 1 АК Пространственное строение пептидов и белков
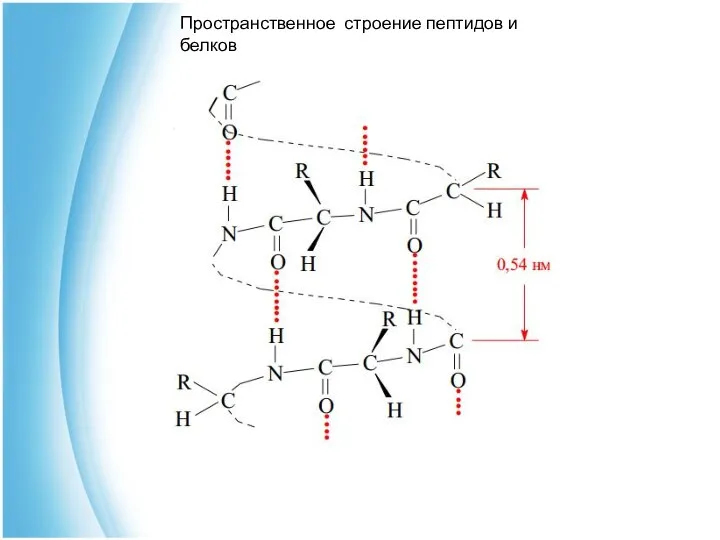
- 36. Вторичная структура белка возникает за счет водородных связей между пептидными связями, что приводит к упорядоченному расположению
- 37. α-спираль Представляет собой полипептидную цепь расположенную в виде правозакрученной спирали. Внешне она похожа на слегка растянутую
- 38. Пространственное строение пептидов и белков
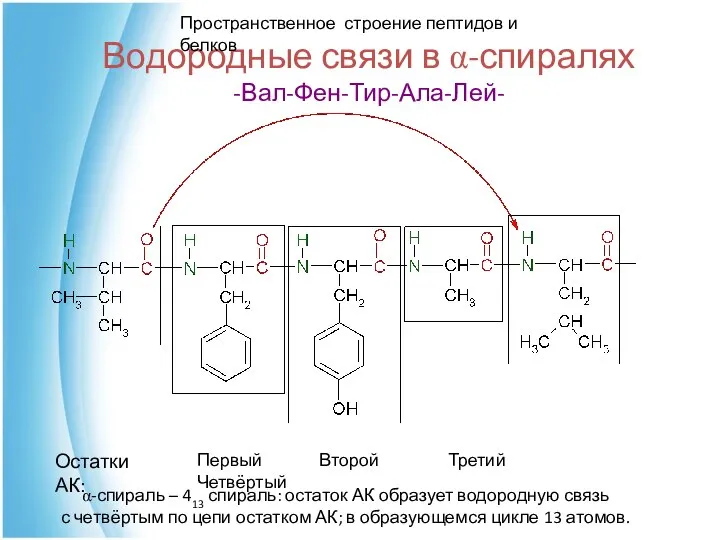
- 39. Водородные связи в α-спиралях -Вал-Фен-Тир-Ала-Лей- Первый Второй Третий Четвёртый Остатки АК: α-спираль – 413 спираль: остаток
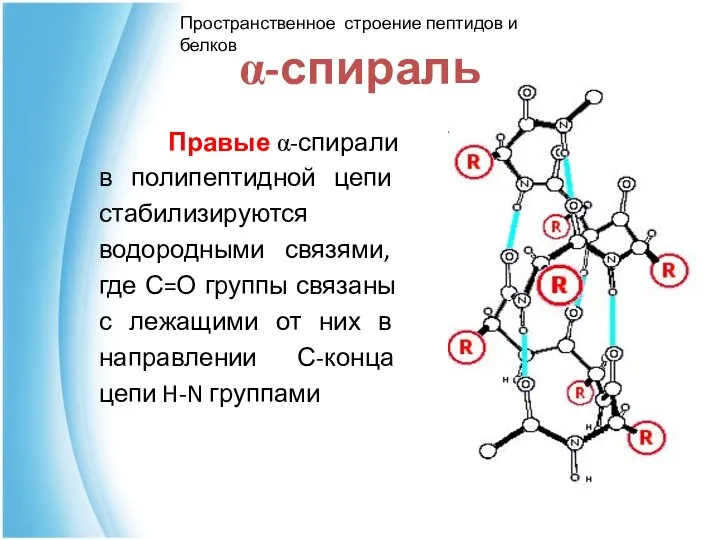
- 40. α-спираль Правые α-спирали в полипептидной цепи стабилизируются водородными связями, где С=О группы связаны с лежащими от
- 41. β-слой Пространственное строение пептидов и белков
- 42. Пространственное строение пептидов и белков
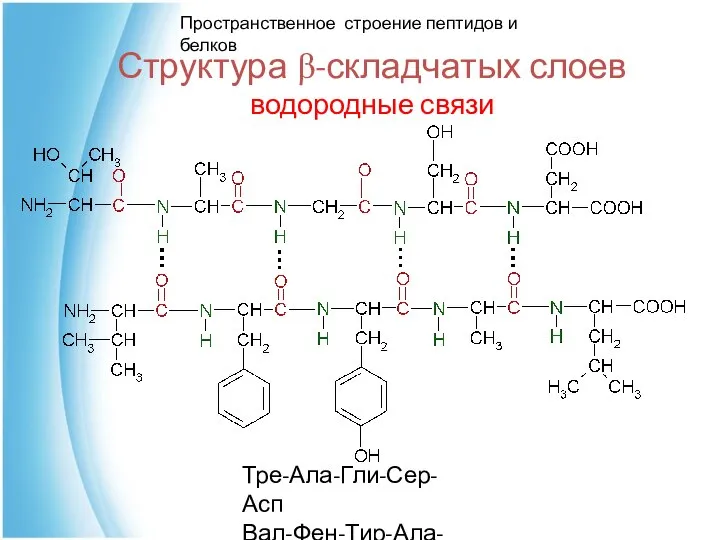
- 43. Структура β-складчатых слоев водородные связи Тре-Ала-Гли-Сер-Асп Вал-Фен-Тир-Ала-Лей Пространственное строение пептидов и белков
- 44. Третичная структура белка возникает в результате взаимодействия между радикалами аминокислотных остатков полипептидных цепей. К таким взаимодействиям
- 45. Выделяют два общих типа третичной структуры: 1) В Фибриллярных белках (например, коллаген, эластин) молекулы которых имеют
- 46. Укладка α-спиралей и β-структуры с образованием глобулы Пространственное строение пептидов и белков
- 47. Взаимодействия остатков АК в третичной структуре АК в белковой глобуле взаимодействуют за счёт: Ковалентных связей (дисульфидные
- 48. Дисульфидные связи в цистине Пространственное строение пептидов и белков
- 49. Ионные связи Асп Лиз Пространственное строение пептидов и белков
- 50. Третичная структура ацилтрансфераза пиктатлиаза С Пространственное строение пептидов и белков
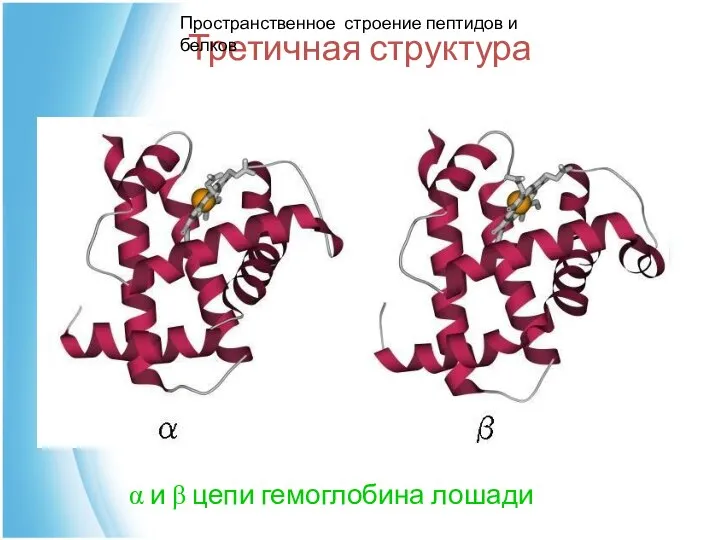
- 51. Третичная структура α и β цепи гемоглобина лошади Пространственное строение пептидов и белков
- 52. Домены Домены – глобулярные области в пределах одной белковой молекулы Домены соединены шарнирным участком Доменная структура
- 53. Четвертичная структура Четвертичная структура - способ укладки в пространстве отдельных полипептидных цепей, обладающих одинаковой первичной, вторичной,
- 54. Пространственное строение пептидов и белков 2130 одинаковых молекул белка расположены вокруг РНК вируса
- 55. 3. Физико-химические свойства пептидов и белков
- 56. Образуют коллоидные растворы. Большинство белков гидрофильны. Однако белковые молекулы имеют очень большие размеры, поэтому белки не
- 57. Несмотря на большую величину, многие белковые молекулы не осаждаются в водных растворах. Осаждению белковых молекул препятствуют
- 58. ФАКТОРЫ СТАБИЛИЗАЦИИ БЕЛКА В РАСТВОРЕ ГИДРАТНАЯ ОБОЛОЧКА - это слой молекул воды, определенным образом ориентированных на
- 59. Осаждение нативных белков 1. ВЫСАЛИВАНИЕ - это осаждение белков высокими концентрациями нейтральных солей щелочных и щелочноземельных
- 60. Белки менее гидрофильные, которые плохо удерживают воду гидратной оболочки, теряют ее раньше. Более гидрофильные белки требуют
- 61. 2. ПРИМЕНЕНИЕ ВОДООТНИМАЮЩИХ СРЕДСТВ. Такими средствами являются растворители, которые смешиваются с водой в любых соотношениях. Чаще
- 62. ДЕНАТУРАЦИЯ - это лишение белка eгo природных, нативных свойств, сопровождающееся разрушением четвертичной (если она была), третичной,
- 63. ФАКТОРЫ, ВЫЗЫВАЮЩИЕ ДЕНАТУРАЦИЮ БЕЛКОВ Физико-химические свойства пептидов и белков
- 64. ДЕЙСТВИЕ СОЛЕЙ ТЯЖЕЛЫХ МЕТАЛЛОВ. Образуют соединения с SН-группами белков. Ядовиты для человека и животных. В медицинской
- 65. Обратимость денатурации В пробирке (in vitгo) чаще всего это - необратимый процесс. Если же денатурированный белок
- 66. 4. Пептидный синтез
- 67. Чтобы соединить две аминокислоты пептидной связью, например получить метионилглицин, необходимо: 1) закрыть (защитить) аминогруппу метионина и
- 68. Пептидный синтез
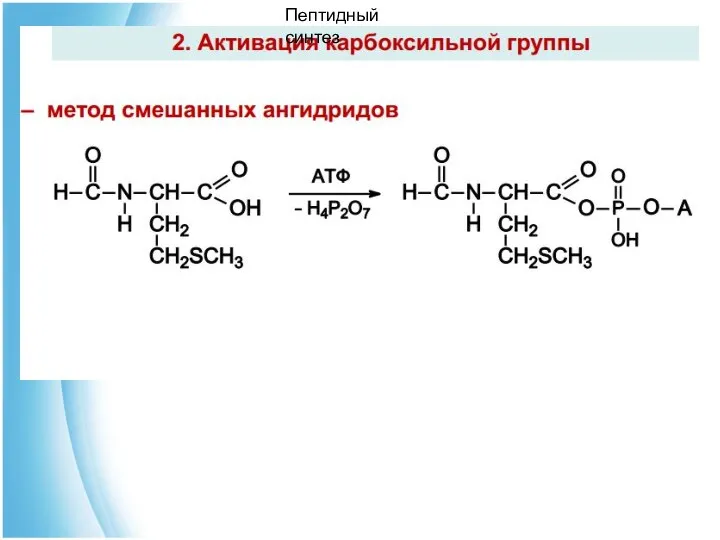
- 69. Пептидный синтез
- 70. Пептидный синтез
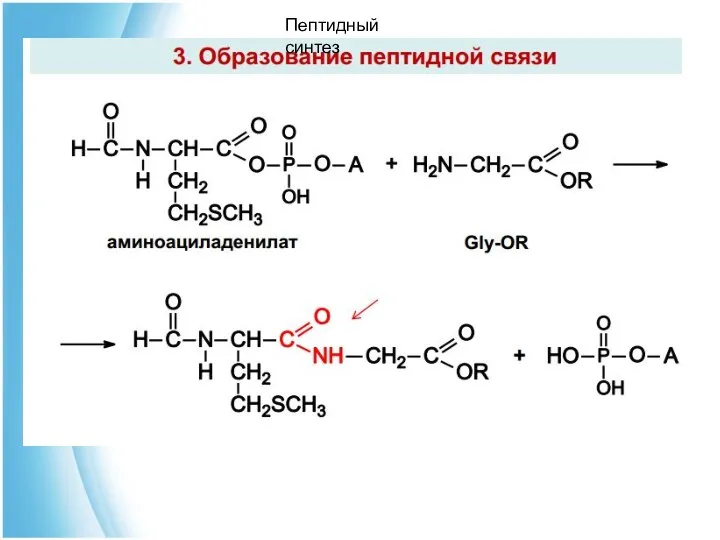
- 71. Пептидный синтез
- 72. Пептидный синтез
- 73. Очень перспективный метод синтеза пептидных связей предложил в 1960 г. Меррифильд (США) метод твердофазного синтеза пептидов.
- 74. Пептидный синтез
- 75. 5. Методы выделения и очистки белка
- 76. Диализ Диализ используют для отделения низкомолекулярных примесей или замены состава среды. Метод основан на том, что
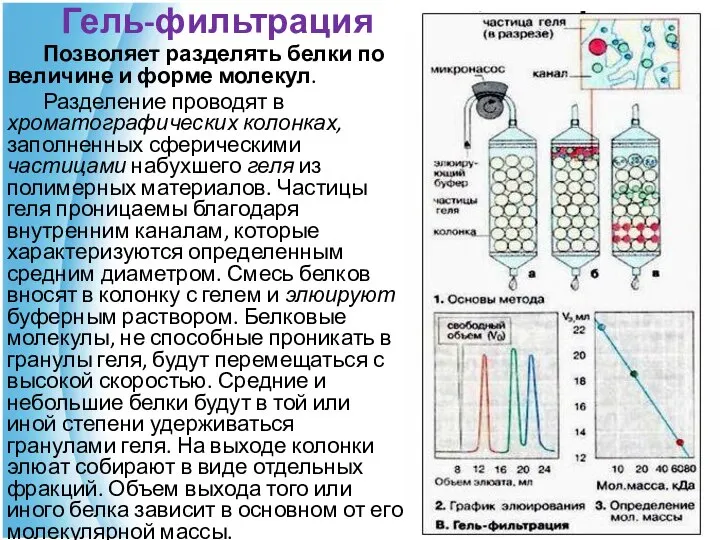
- 77. Гель-фильтрация Позволяет разделять белки по величине и форме молекул. Разделение проводят в хроматографических колонках, заполненных сферическими
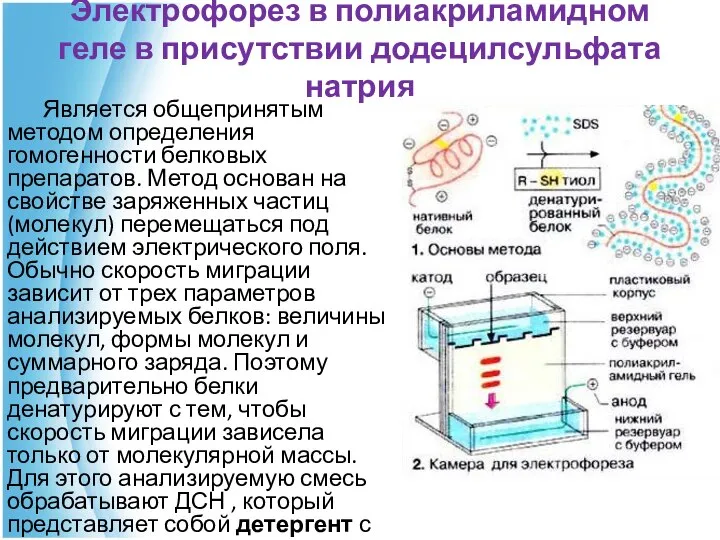
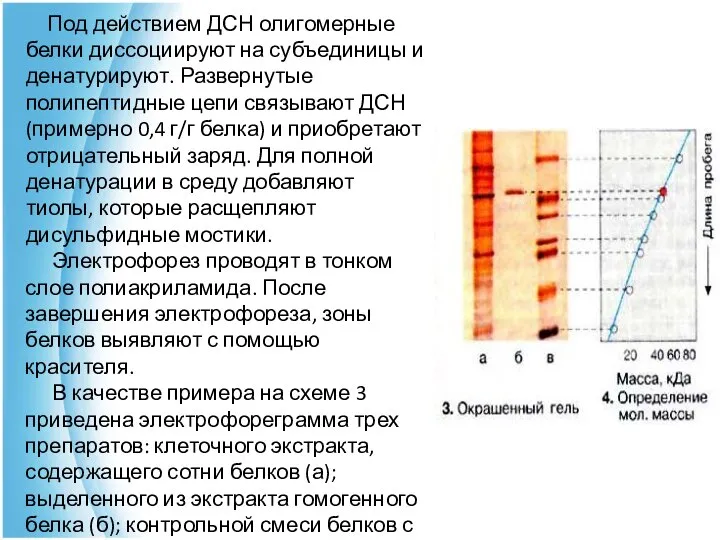
- 78. Электрофорез в полиакриламидном геле в присутствии додецилсульфата натрия Является общепринятым методом определения гомогенности белковых препаратов. Метод
- 79. Под действием ДСН олигомерные белки диссоциируют на субъединицы и денатурируют. Развернутые полипептидные цепи связывают ДСН (примерно
- 81. Скачать презентацию





























































 Природа активності та кислотності цеолітних каталізаторів
Природа активності та кислотності цеолітних каталізаторів Кристаллические решетки
Кристаллические решетки Электронное строение атома
Электронное строение атома Нуклеиновые кислоты
Нуклеиновые кислоты Электронное строение атома. Лекция № 2
Электронное строение атома. Лекция № 2 Марганец и его свойства
Марганец и его свойства Обратимость химических реакций. Химическое равновесие
Обратимость химических реакций. Химическое равновесие Практическая работа № 3. Получение, собирание и распознавание газов
Практическая работа № 3. Получение, собирание и распознавание газов Алкины. Гомологический ряд
Алкины. Гомологический ряд Презентация по Химии "Бензини" - скачать смотреть бесплатно
Презентация по Химии "Бензини" - скачать смотреть бесплатно Алкены – непредельные углеводороды
Алкены – непредельные углеводороды Контроль качества неорганических лекарственных средств элементов VII группы периодической системы Д. И. Менделеева
Контроль качества неорганических лекарственных средств элементов VII группы периодической системы Д. И. Менделеева Каталітичні процеси нафтопереробки
Каталітичні процеси нафтопереробки МОУ СОШ №5 ст.Бриньковская УРОК ПО ТЕМЕ: «ЧИСТАЯ ВОДА» подготовила учитель химии Беба Е.А.
МОУ СОШ №5 ст.Бриньковская УРОК ПО ТЕМЕ: «ЧИСТАЯ ВОДА» подготовила учитель химии Беба Е.А.  Алкени
Алкени Күрделі липидтер.Сабынданбайтын липидтер (стериндер, стероидтар) және олардың биологиялық маңызы. Терпендер
Күрделі липидтер.Сабынданбайтын липидтер (стериндер, стероидтар) және олардың биологиялық маңызы. Терпендер Карбоновые кислоты и их функциональные производные
Карбоновые кислоты и их функциональные производные Цепная сополимеризация
Цепная сополимеризация Неметаллы
Неметаллы Классификация веществ, вызывающих отравление. (Тема 4)
Классификация веществ, вызывающих отравление. (Тема 4) Углеводы
Углеводы Экоаналитический контроль воздуха
Экоаналитический контроль воздуха Реакция Бэйлиса Хиллмана-Мориты
Реакция Бэйлиса Хиллмана-Мориты Термодинамика фазовых превращений
Термодинамика фазовых превращений ДОСЛІДЖЕННЯ ДОСЛІДЖЕННЯ НАЙМАСОВІШИХ КУПАННЯ смт
ДОСЛІДЖЕННЯ ДОСЛІДЖЕННЯ НАЙМАСОВІШИХ КУПАННЯ смт XXI ғасыр көшбасшысы
XXI ғасыр көшбасшысы Рівняння характеристики крупності
Рівняння характеристики крупності IV,III группа периодической системы Д..И. Менделеева. Кислота борная, натрия гидрокарбонат
IV,III группа периодической системы Д..И. Менделеева. Кислота борная, натрия гидрокарбонат