Содержание
- 2. Растворы. Классификация растворов Растворитель – компонент, количество которого в системе преобладает либо не меняет своего агрегатного
- 3. Газообразные растворы (Смесь газов) Жидкие растворы По агрегатному состоянию: воздух – это раствор кислорода, паров воды,
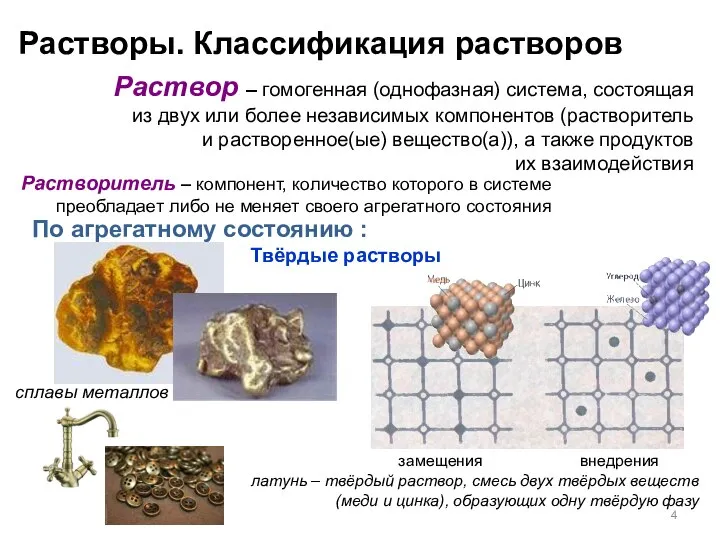
- 4. Твёрдые растворы сплавы металлов латунь – твёрдый раствор, смесь двух твёрдых веществ (меди и цинка), образующих
- 5. Растворы. Классификация растворов По относительным количествам растворенного вещества: Насыщенный раствор – это раствор, который находится в
- 6. Растворы. Классификация растворов Истинный раствор – однофазная система, образованная не менее чем двумя компонентами (т.е. компоненты
- 7. Физические и химические процессы при растворении Физическая теория растворов – идея индифферентности и подобия газовым системам
- 8. Физические и химические процессы при растворении Механическая смесь Раствор Химическое соединение переменность состава непрерывная, плавная зависимость
- 9. Физические и химические процессы при растворении Тепловой эффект, сопровождающий процесс растворения, относящийся к 1 молю растворенного
- 10. Способы выражения концентрации Концентрация – соотношение между количеством растворенного вещества и растворителя или количеством растворенного вещества
- 11. Растворимость веществ. Факторы, влияющие на растворимость коэффициент поглощения газа – наибольший объем газа, который может раствориться
- 12. Растворимость веществ. Факторы, влияющие на растворимость Растворимость веществ зависит: от природы реагирующих веществ от концентрации раствора
- 13. Растворимость твердых веществ в жидкостях от природы реагирующих веществ от температуры Для идеальных растворов справедливо уравнение
- 14. Растворимость жидкостей в жидкостях от природы реагирующих веществ от температуры от высокого давления Неограниченная растворимость –
- 15. Растворимость газов в жидкостях Растворимость газов в жидкостях при повышении температуры УМЕНЬШАЕТСЯ Закон Генри при постоянной
- 16. Закон распределения 1 2 c1 c2 c1 – концентрация вещества 3 в жидкости 1 c2 –
- 17. Законы Рауля Первый закон Рауля связывает давление насыщенного пара над раствором с его составом Для бинарного
- 18. Законы Рауля Относительное понижение парциального давления пара растворителя над раствором не зависит от природы растворённого вещества
- 19. Законы Рауля Понижение температуры замерзания раствора и повышение температуры его кипения прямо пропорционально моляльной концентрации раствора
- 20. Одинаковы при равновесии Осмотическое давление П – давление, которое надо приложить к раствору для прекращения переноса
- 21. Растворы электролитов Электролиты – вещества, которые в растворе или в расплаве состоят полностью или частично из
- 22. Растворы электролитов Степень диссоциации – доля растворенного электролита, которая распалась на ионы В растворах сильных электролитов
- 23. Растворы электролитов Сильные электролиты Слабые электролиты Электролиты средней силы Почти все соли, кроме CdCl2, HgCl2, Fe(CNS)3,
- 24. Состояние сильных электролитов в растворе + + + + + - - - - - Ионная
- 25. Водородный показатель Можно принять концентрацию недиссоциированных молекул воды постоянной Ионное произведение воды В чистой воде
- 26. Водородный показатель Ионное произведение воды моль/л - СРЕДА КИСЛАЯ моль/л - СРЕДА ОСНОВНАЯ - СРЕДА НЕЙТРАЛЬНАЯ
- 27. Водородный показатель
- 29. Скачать презентацию

























 11 хб
11 хб  Химия. Вопросы. Практическая работа
Химия. Вопросы. Практическая работа Серная кислота H2SO4
Серная кислота H2SO4 EPR of phosphorus in diamond crystals. An influence of nitrogen impurity, HTHP treatment and high phosphorus concentration
EPR of phosphorus in diamond crystals. An influence of nitrogen impurity, HTHP treatment and high phosphorus concentration Дека́н (н-декан) — органическое соединение класса алканов
Дека́н (н-декан) — органическое соединение класса алканов Катализдің түрлері жене маңызы
Катализдің түрлері жене маңызы Химические Недотроги
Химические Недотроги  Названы именем Д.И.Менделеева. Презентацию подготовили: Баранов С.-ученик 9 класса Мошковской СОШ Воронцова О.Е. – учитель химии М
Названы именем Д.И.Менделеева. Презентацию подготовили: Баранов С.-ученик 9 класса Мошковской СОШ Воронцова О.Е. – учитель химии М Сопротивление материалов. Металлический тип химической связи и основные свойства металлов
Сопротивление материалов. Металлический тип химической связи и основные свойства металлов Растворы электролитов
Растворы электролитов Синтез реакционноспособных олигомеров и полимеров на их основе
Синтез реакционноспособных олигомеров и полимеров на их основе Поверхностные явлении и дисперсные системы (коллоидная химия)
Поверхностные явлении и дисперсные системы (коллоидная химия) Решение задач на растворы и смеси
Решение задач на растворы и смеси Презентация по Химии "Закон збереження маси" - скачать смотреть
Презентация по Химии "Закон збереження маси" - скачать смотреть  F элементы
F элементы Жёсткость воды и способы её устранения
Жёсткость воды и способы её устранения Аминокислоты. Номенклатура аминокислот
Аминокислоты. Номенклатура аминокислот Все о витамине С и его определение в лекарственных растениях и продуктах питания
Все о витамине С и его определение в лекарственных растениях и продуктах питания История микроскопа
История микроскопа  Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Оборудование кабинета химии. Смотрите внимательно и запоминайте!!!
Оборудование кабинета химии. Смотрите внимательно и запоминайте!!! Презентация по Химии "Белки" - скачать смотреть бесплатно_
Презентация по Химии "Белки" - скачать смотреть бесплатно_ Презентация по Химии "История развития химии" - скачать смотреть
Презентация по Химии "История развития химии" - скачать смотреть  Анализ смеси катионов первойтретьей аналитических групп по систематическому анализу. Химическое равновесие
Анализ смеси катионов первойтретьей аналитических групп по систематическому анализу. Химическое равновесие Көмірдің оптикалық қасиеттері
Көмірдің оптикалық қасиеттері Простые и сложные вещества Моцепуро Иван Класс 10 «а» Учитель: Макарова Е. И.
Простые и сложные вещества Моцепуро Иван Класс 10 «а» Учитель: Макарова Е. И. Ферменттер – тіршілік негізі
Ферменттер – тіршілік негізі Синергизм и синергические системы
Синергизм и синергические системы