Содержание
- 2. #ОВРновый 3. Для выполнения задания используйте следующий перечень веществ: хлорид цинка, оксид фосфора(V), бромид кальция, медь,
- 3. Реакция: 2NO + 2Cu = 2CuO + N2 Баланс: 2N(+2) + 4е= N 2 1 Cu-2е=
- 4. #ОВРновый 5. Для выполнения задания используйте следующий перечень веществ: соляная кислота, нитрат серебра, сульфат аммония, оксид
- 5. Реакция: 4 HCl + MnO2 = MnCl2 + Cl2 + 2 H2O Баланс: 2Cl(-1) -2е= Cl2
- 6. #ОВРновый 6. Для выполнения задания используйте следующий перечень веществ: аммиак, сульфат меди (II), хлорид бария, йодид
- 7. Реакция: 2 CuSO4 + 4 KI = 2 CuI + 2 K2SO4 + I2 Баланс: Cu(+2)+1e=Cu(+1)
- 8. #ОВРновый 9. Для выполнения задания используйте следующий перечень веществ: диоксид кремния, сульфат натрия, фосфор, хлорид хрома
- 9. (Зажигаем спичку) Реакция: 6 P + 5 KClO3 = 3 P2O5 + 5 KCl Баланс: Р(0)-5е=Р(+5)
- 10. #ОВРновый 10. Для выполнения задания используйте следующий перечень веществ: карбонат калия, нитрат марганца, азот, оксид свинца(IV),
- 11. Реакция: 2Mn(NO3)2 + 5PbO2 + 6HNO3 = 5Pb(NO3)2 + 2HMnO4 + 2H2O Баланс: Mn(+2)-5е= Mn(+7) 2
- 12. #ОВРновый 11. Для выполнения задания используйте следующий перечень веществ: сульфид калия, нитрат цинка, ацетат калия, гипохлорит
- 13. 1 способ Реакция: Na2S2O3 + 4 NaClO + H2O = 4 NaCl + 2 NaHSO4 Баланс:
- 14. 2 способ. Метод полуреакций ClO(1-) +2Н(1+) +2е= Cl(-1) +Н2О 4 S2O3(2-) + 5Н2О -8е=2НSO4(1-)+8Н(1+) 1 Алгоритм:
- 15. Метод полуреакций. Продолжение Шаг 2. Уравнять по кислороду S2O3(2-) =2SO4(2-) Слева не хватает 5 атомов кислорода,
- 16. Метод полуреакций. Продолжение Шаг 3. Дописать электроны Считаем суммарный заряд для реагентов и для продуктов отдельно:
- 17. #ОВРновый 15. Для выполнения задания используйте следующий перечень веществ: сульфид натрия, хлорид натрия, хлорид железа(III), фосфат
- 18. Реакция: 2 FeCl3 + 3 Na2S = S + 2 FeS + 6 NaCl Баланс: Fe(+3)+1е=
- 19. #посчитай 16. При разбавлении 25 %-й соляной кислоты получили 150 г 10 %-й кислоты. Сколько граммов
- 20. Решение m1(HCI)=m2(HCI)=m2 p-pa(HCI)*w2(HCI)= =150 г *0,1=15 г m1 p-pa (HCl)=m1(HCl)/w1(HCl)=15 г/0,25=60 г Ответ: 60 ЗАМЕЧАНИЕ: обращайте
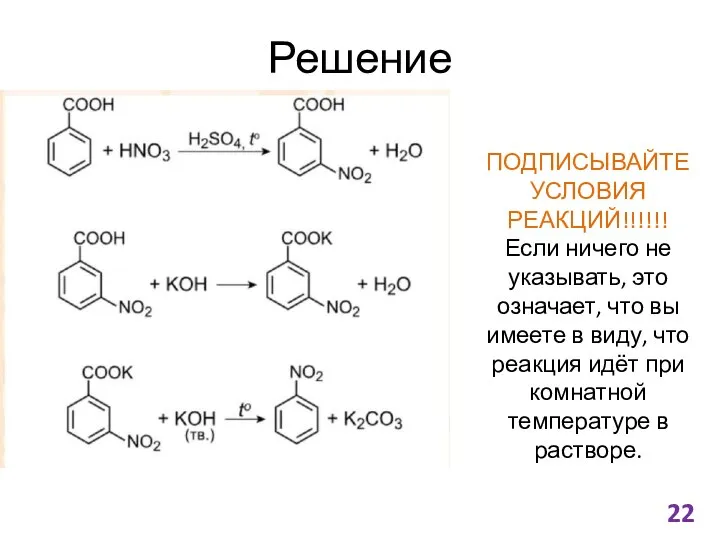
- 21. #соточка. 33 задание
- 22. Решение ПОДПИСЫВАЙТЕ УСЛОВИЯ РЕАКЦИЙ!!!!!! Если ничего не указывать, это означает, что вы имеете в виду, что
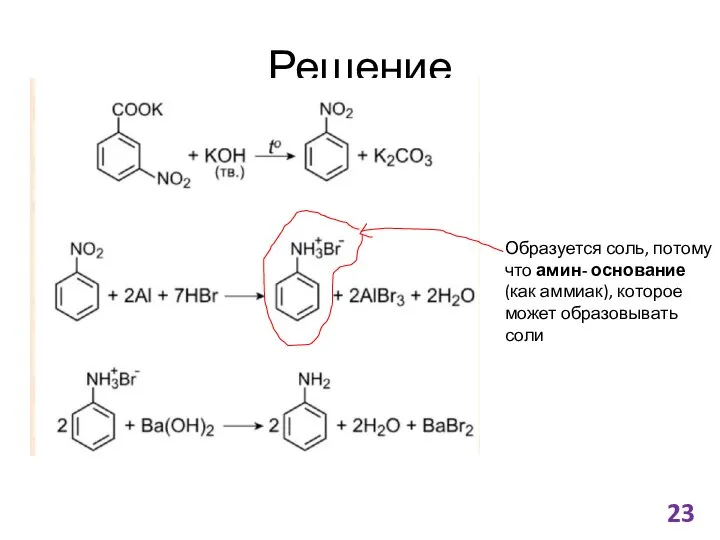
- 23. Решение Образуется соль, потому что амин- основание (как аммиак), которое может образовывать соли
- 24. #соточка 34. Технический нитрат алюминия, содержащий 3% примесей подвергли прокаливанию. Выделившийся при этом газ полностью поглотили
- 25. Решение (1 реакция) 4Al(NO3)3=2Al2O3+12NO2+3O2 (2 реакция)2NaOH+2NO2=NaNO3+NaNO2+H2O (3 реакция) H2SO4+2NaOH=Na2SO4+H2O 3% примесей => чистого Al(NO3)3 в навеске
- 26. Решение. Продолжение n3(NaOH)=2n(H2SO4)=2*0,184 моль=0,368 моль n2(NaOH)=n3(NaOH)=0,368 моль n(NO2)=n2(NaOH)= 0,368 моль- по коэффициентам 2 реакции n(NO2):n(Al(NO3)3)=12:4=3:1- по
- 27. Комментарии За 34 задание максимум – 4 первичных балла Правильно написаны все реакции=1 балл Необходимые вычисления
- 28. #соточка 35. При сжигании навески неизвестного вещества массой 3,5 г образовалось 4,48 л углекислого (н.у.) газа
- 29. Решение Реакция горения: СхНyОz+аО2=хСО2+(y/2)Н2О n(CO2) = V(CO2)/Vm(CO2) = 4,48/22,4 = 0,2 моль n(C) = n(CO2) =
- 30. Решение Теперь подумаем: альдегиды и кетоны (формула) СnН2nО (без двойных или тройных связей) Получили С4Н6О, не
- 31. Комментарии к ЕГЭ Подчеркивайте ключевые моменты (с чем реагирует/не реагирует, про количество вещества и тд) Чтобы
- 33. Скачать презентацию




























 Наличие 2 х сигналов в ЯМР 1Н (задача)
Наличие 2 х сигналов в ЯМР 1Н (задача) обобщение знаний
обобщение знаний Простой борный суперфосфат
Простой борный суперфосфат Ассортимент и качество изделий из пластмасс (урок 84)
Ассортимент и качество изделий из пластмасс (урок 84) Жесткость воды и способы ее устранения
Жесткость воды и способы ее устранения Практика по химии
Практика по химии Галогены
Галогены Жири. Жири в природі. Біологічна роль жирів. Жири. Жири в природі. Біологічна роль жирів.
Жири. Жири в природі. Біологічна роль жирів. Жири. Жири в природі. Біологічна роль жирів.  Химический состав клетки. Неорганические вещества клетки. Глава 1
Химический состав клетки. Неорганические вещества клетки. Глава 1 Физико-химические свойства белков. Электрофоретические и хроматографические методы
Физико-химические свойства белков. Электрофоретические и хроматографические методы Технология получения полиуретанов
Технология получения полиуретанов Природные (натуральные) полимеры. Композиционные материалы
Природные (натуральные) полимеры. Композиционные материалы Химические реактивы
Химические реактивы Презентация по Химии "Строение атома" - скачать смотреть бесплатно_
Презентация по Химии "Строение атома" - скачать смотреть бесплатно_ Металлы ГОУ СОШ № 661 УЧИТЕЛЬ ХИМИИ Ефремова С.А.
Металлы ГОУ СОШ № 661 УЧИТЕЛЬ ХИМИИ Ефремова С.А. Машиностроительные материалы
Машиностроительные материалы Углерод и кремний
Углерод и кремний Химическая кинетика. Лекция 2
Химическая кинетика. Лекция 2 Положение в ПСХЭ Д.И.Менделеева и строение атома
Положение в ПСХЭ Д.И.Менделеева и строение атома Рождающий воду
Рождающий воду Химические формулы. Относительные атомная и молекулярная массы. Расчетные задачи
Химические формулы. Относительные атомная и молекулярная массы. Расчетные задачи Особенности строения, реакционной способности и методы синтеза аренов
Особенности строения, реакционной способности и методы синтеза аренов Лекарственное растительное сырье, содержащее алкалоиды
Лекарственное растительное сырье, содержащее алкалоиды Хімія та обмін ліпідів
Хімія та обмін ліпідів Химические свойства металлов
Химические свойства металлов «Аспирин» Выполнила ученица 11 «Б»класса Панина Евгения
«Аспирин» Выполнила ученица 11 «Б»класса Панина Евгения  Органические галогениды. (Лекция 7)
Органические галогениды. (Лекция 7) Кристаллохимия. Тығыз шарлар теориясы
Кристаллохимия. Тығыз шарлар теориясы