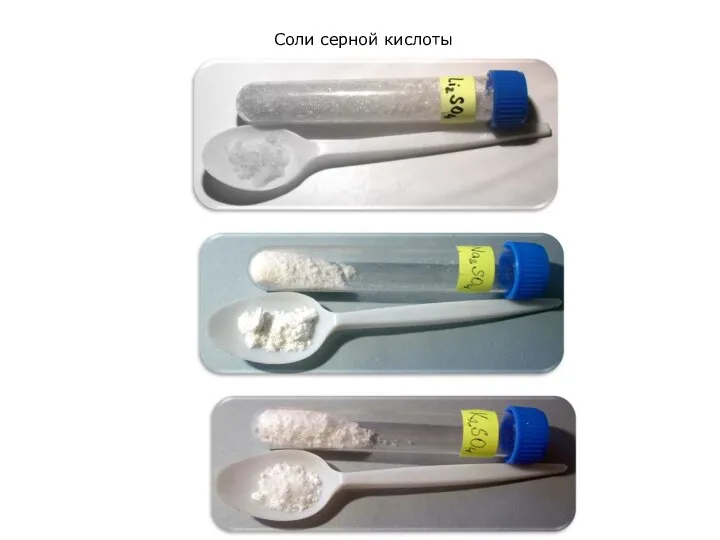
Соли серной кислоты
Сульфаты (от лат. sulphur, sulfur – сера), сернокислые соли, соли
серной кислоты H2SO4. Имеются два ряда сульфатов – средние (нормальные) общей формулы M2SO4 и кислые (гидросульфаты) – MHSO4, где М – одновалентный металл.
Сульфаты – кристаллические вещества, бесцветные (если катион бесцветен), в большинстве случаев хорошо растворимые в воде. Малорастворимые сульфаты встречаются в виде минералов: гипса CaSO4·2H2O, целестина SrSO4, англезита PbSO4 и др.
Практически нерастворимы барит BaSO4 и RaSO4.
Кислые сульфаты выделены в твёрдом состоянии лишь для наиболее активных металлов – Na, K и др. Они хорошо растворимы в воде, легко плавятся.
Нормальные сульфаты можно получить растворением металлов в H2SO4, действием H2SO4 на окиси, гидроокиси, карбонаты металлов и др.
Гидросульфаты получают нагреванием нормальных сульфатов с концентрированной H2SO4: K2SO4 + H2SO4 = 2KHSO4.
Кристаллогидраты сульфатов некоторых тяжёлых металлов называются купоросами.
Широкое применение во многих отраслях промышленности находят природные сульфаты.






![Соли серной кислоты CuSO4·5H2O CuSO4 [Cu(NH3)4SO4]·H2O](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1396676/slide-8.jpg)


 Гліцерин (Гліцерол)
Гліцерин (Гліцерол) ВМС и растворы ВМС
ВМС и растворы ВМС Непредельные углеводороды алкены
Непредельные углеводороды алкены Презентация по Химии "углерод" - скачать смотреть бесплатно
Презентация по Химии "углерод" - скачать смотреть бесплатно Металлы в нашей жизни
Металлы в нашей жизни Углеводы
Углеводы Катализаторы. Ферменты
Катализаторы. Ферменты Презентация Карбонаты
Презентация Карбонаты  Титриметрический анализ. Кривые титрования
Титриметрический анализ. Кривые титрования Оксиды углерода (II) и (IV). Качественная реакция на углекислый газ
Оксиды углерода (II) и (IV). Качественная реакция на углекислый газ Использование энергии солнца на земле
Использование энергии солнца на земле Дикарбоновые кислоты
Дикарбоновые кислоты Адиабатическое приближение
Адиабатическое приближение Минерал клинохлор. Месторождения
Минерал клинохлор. Месторождения Презентация по Химии "Таблица Периодическая система химических элементов Д.И. Менделеева" - скачать смотреть
Презентация по Химии "Таблица Периодическая система химических элементов Д.И. Менделеева" - скачать смотреть  Презентация Производство стекла
Презентация Производство стекла История получения алюминия и его применение
История получения алюминия и его применение Сarbonyl compounds. Carboxylic acids. Lipids
Сarbonyl compounds. Carboxylic acids. Lipids Классификация минералов + самородные элементы. Занятие 5
Классификация минералов + самородные элементы. Занятие 5 Сера. Строение и свойства атома серы
Сера. Строение и свойства атома серы ПРИРОДНИЙ ГАЗ
ПРИРОДНИЙ ГАЗ  Презентация по Химии "Тема: Цікаві факти з життя Д.І. Менделєєва" - скачать смотреть бесплатно
Презентация по Химии "Тема: Цікаві факти з життя Д.І. Менделєєва" - скачать смотреть бесплатно Химия и здоровье
Химия и здоровье Презентация по Химии "РАСТВОРЫ ЭЛЕКТРОЛИТОВ" - скачать смотреть
Презентация по Химии "РАСТВОРЫ ЭЛЕКТРОЛИТОВ" - скачать смотреть  Вольфрам және молибден
Вольфрам және молибден Лекарственные препараты
Лекарственные препараты  Методы снижения уровня учебного стресса у обучающихся 9-х классов на уроках химии
Методы снижения уровня учебного стресса у обучающихся 9-х классов на уроках химии Екстракція і йонний обмін
Екстракція і йонний обмін