Содержание
- 2. Жоспар. І. Кіріспе; ІІ. Негізгі бөлім: Спирттердің жіктелуі, қасиеттері,қолданылуы. Фенолдардың қасиеттері,алынуы,қолданылуы. ІІІ. Қорытынды; ІV. Пайдаланылған әдебиеттер.
- 3. Спирттер СnH2n+1OH Спирттер - малекулаларында көмірсутек радикалымен байланысқан (ОН) гидроксил тобы бар заттар.
- 4. Шарап спирті немесе этил спиртінің формуласы-С2Н5ОН Этил спиртін әртүрлі жолдармен алады. Соның бірі-глюкозадан ашытқы қатысында мына
- 6. Спирттердің жіктелуі Гидроксил тобымен байланысқан көмірсутек радикалына байланысты гидроксил тобының саңына байланысты гидроксил тобымен байланысқан көміртек
- 9. Спирттердің гомологтық қатары Спирттердің жалпы формуласы CnH2n+1OH Жүйелік номенклатура бойынша спирттерге «ол» деген жүрнақ қосылады
- 10. Спирттердің физикалық қасиеттері Қалыпты температурада С10- ға дейінгі спирттер сұйық заттар, С11-ден бастап қатты заттар. Алғашқы
- 11. Қайнау температурасы
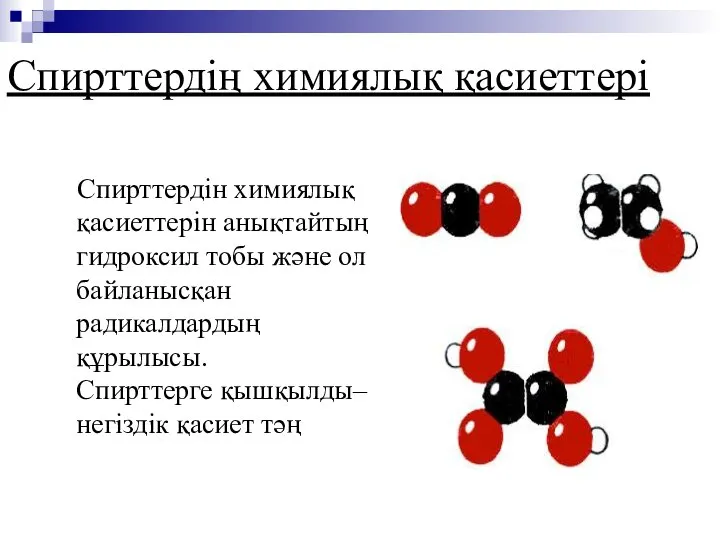
- 12. Спирттердің химиялық қасиеттері Спирттердін химиялық қасиеттерін анықтайтың гидроксил тобы және ол байланысқан радикалдардың құрылысы. Спирттерге қышқылды–
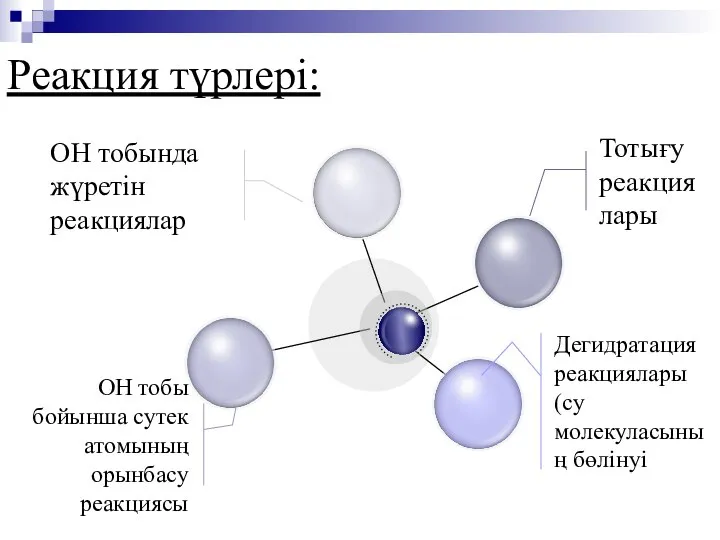
- 13. Реакция түрлері:
- 14. ОН тобы бойынша сутек атомының орынбасу реакциясы С2Н5ОН + Na → C2H5ONa + H2 C2H5ONa +
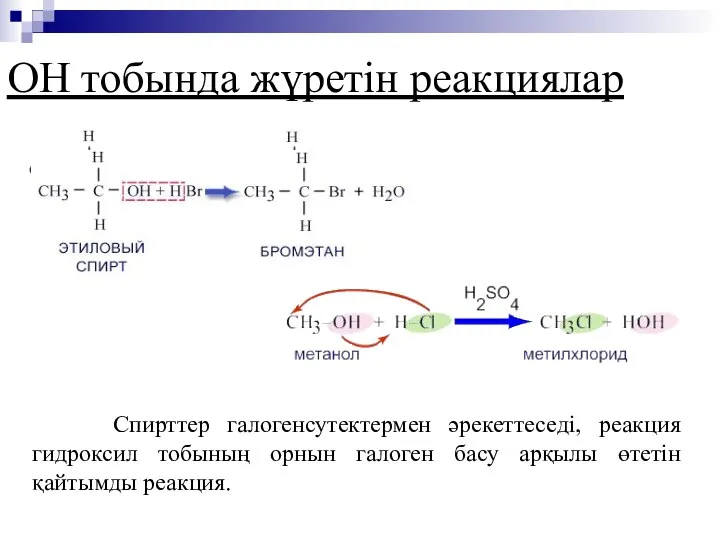
- 15. ОН тобында жүретін реакциялар Спирттер галогенсутектермен әрекеттеседі, реакция гидроксил тобының орнын галоген басу арқылы өтетін қайтымды
- 16. Дегидратация реакциялары Cпирттерге дегидратацияның екі түрі тәң: - молекула ішілік - молекула аралық Молекула ішілік -
- 17. Тотығу реакциялары Спирттердің тотығуы күшті тотықтырғыштар әсерінен тотығады. Түзілу өнімдері спирттердін орынбасу дәрежесіне сай, және пайдаланатын
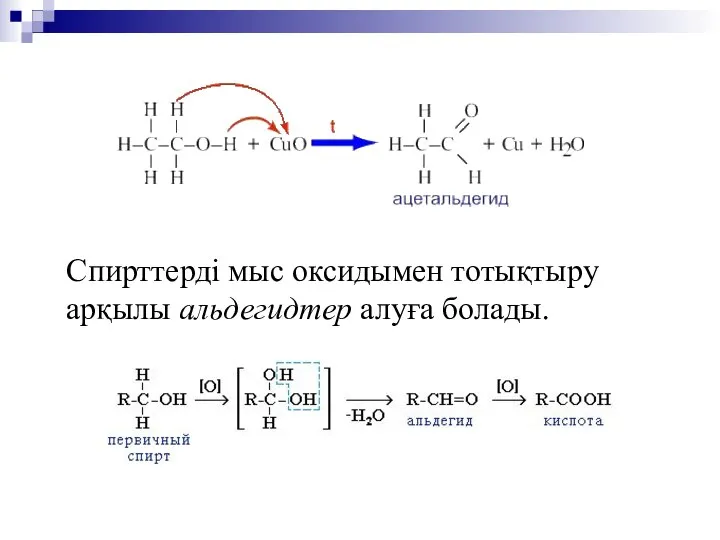
- 18. Спирттерді мыс оксидымен тотықтыру арқылы альдегидтер алуға болады.
- 19. Қолданылуы: Медициналық практикада этил спирті негізінен сүртінуге, компресстерге арналған сыртқы антисептикалық және тітіркендіргіш зат ретінде қолданылады.
- 20. Фенолдар — бензол сақинасындағы бір немесе бірнеше сутек атомдарының орнын гидроксотоп басқан ароматты көмірсутектердің туындылары. Ең
- 21. Фенолды көбіне тас көмір шайырын өңдеу арқылы алады. Сондай-ақ ароматты көмірсутектерінің галогентуындыларын сілтімен әрекеттестіріп те алады.
- 22. Физикалық қасиеттері. Фенол — түссіз кристалдық зат. 43°С-та балқиды. Ауада ашық қалғанда тотығатындықтан, қызғылт түсті болады.
- 23. Фенолдың 3—5%-тік ерітіндісін зиянды микробтарды жою үшін антисептик ретінде қолданады. Фенолдан түрлі дәрі-дәрмектік препараттарды, бояуларды, синтездік
- 24. Қорытынды: Сутектік байланыс –бір сутегі молекуласымен электртерістігі жоғары атомдар (О,F,N,Cl) арасында пайда болатын байланыс. Этерификация реакциясы
- 26. Скачать презентацию



















 ПРЕЗЕНТАЦІЯ З ХІМІЇ НА ТЕМУ: АЦЕТИЛЕН
ПРЕЗЕНТАЦІЯ З ХІМІЇ НА ТЕМУ: АЦЕТИЛЕН  Configuratia electronica. Sistemul periodic al elementelor. (Curs 3)
Configuratia electronica. Sistemul periodic al elementelor. (Curs 3) Устойчивость и резистентность вредных организмов к пестицидам и пути ее преодоления. (Лекция 4)
Устойчивость и резистентность вредных организмов к пестицидам и пути ее преодоления. (Лекция 4) Просто знать еще не все, знания необходимо еще использовать
Просто знать еще не все, знания необходимо еще использовать Программа дополнительного образования Химия, здоровье и окружающая среда
Программа дополнительного образования Химия, здоровье и окружающая среда Окислительно-восстановительные реакции
Окислительно-восстановительные реакции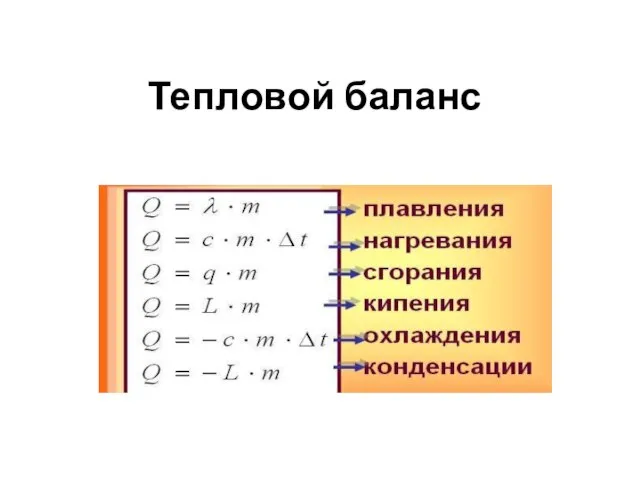 Тепловой баланс
Тепловой баланс Конструкция ферментатора
Конструкция ферментатора Хлорид калия KCI
Хлорид калия KCI Введение в химию органических соединений
Введение в химию органических соединений Вода. Твердість води
Вода. Твердість води  Презентация на тему: Кислотные дожди
Презентация на тему: Кислотные дожди Анализ процесса гальванического нанесения рения. Поиск альтернативных способов нанесения рения
Анализ процесса гальванического нанесения рения. Поиск альтернативных способов нанесения рения Біоорганічна хімія. Реакційна здатність біоорганічних сполук
Біоорганічна хімія. Реакційна здатність біоорганічних сполук Массовая доля элемента в соединении
Массовая доля элемента в соединении Алканы: метан, пропан, этан, бутан
Алканы: метан, пропан, этан, бутан Реакции ионного обмена
Реакции ионного обмена Пиролиз. Паровой крекинг углеводородов
Пиролиз. Паровой крекинг углеводородов Работу выполнила: Пьянкова Елена Руководитель: Баранова Алевтина Владимировна 2010
Работу выполнила: Пьянкова Елена Руководитель: Баранова Алевтина Владимировна 2010 Взаимодействие атомов элементов-металлов и элементов-неметаллов между собой. Ионная связь. (Тема 10)
Взаимодействие атомов элементов-металлов и элементов-неметаллов между собой. Ионная связь. (Тема 10) Солеобразующие оксиды
Солеобразующие оксиды Строение атома (лекция 3)
Строение атома (лекция 3) Предмет и задачи токсикологической химии. Взаимосвязь с другими дисциплинами. (Лекция 1)
Предмет и задачи токсикологической химии. Взаимосвязь с другими дисциплинами. (Лекция 1) Презентация по Химии "Сера" - скачать смотреть
Презентация по Химии "Сера" - скачать смотреть  Микрофлора и биохимические реакции подземных вод
Микрофлора и биохимические реакции подземных вод Алкены (этиленовые углеводороды, олефины)
Алкены (этиленовые углеводороды, олефины) Газовые законы
Газовые законы Наблюдения в сходящемся свете. Коноскопия
Наблюдения в сходящемся свете. Коноскопия