Содержание
- 2. 1 22.09.2016 Урок 9 класса. Степень диссоциации.
- 3. 8 Характерные черты ионов 28.09.2016 К+ ОН – Ba2+ CH3COO- Свойства ионов отличаются от свойств атомов.
- 4. 9 Характерные свойства ионов 28.09.2016 Н+ важный показатель кислотности (вспоминаем определение кислот с прошлого урока). Поэтому
- 5. 10 Характерные свойства ионов 28.09.2016 Вспомним принцип Ле Шателье: Если на систему, находящуюся в равновесии, воздействовать
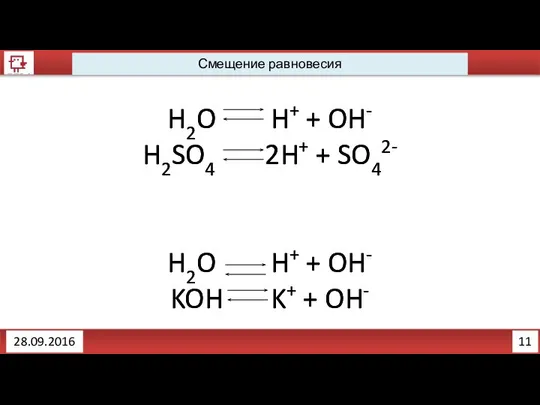
- 6. 11 Смещение равновесия 28.09.2016 H2O H+ + OH- H2SO4 2H+ + SO42- H2O H+ + OH-
- 7. 12 pH 28.09.2016 Когда [H+] > [OH−] говорят, что раствор является кислотным, а при [OH−] >
- 8. 13 Определение кислотности раствора 28.09.2016
- 9. 14 Определение галогенид-ионов 28.09.2016 Галогенид-ионы определяются при взаимодействиями с солями серебра: AgNO3 + KCl = KNO3
- 10. 15 Определение сульфидов 28.09.2016 Качественная реакция на соли меди: Cu2+ +2OH— → Cu(OH)2↓ Качественные реакции на
- 11. 16 Определение бария и сульфитов 28.09.2016 Ba2+ + SO4 -2 → BaSO4↓ качественная реакция на соли
- 12. 17 Образование алюминатов и цинкатов 28.09.2016 Al3+ + 3OH— = Al(OH)3↓ Zn2+ + 2OH— = Zn(OH)2↓
- 13. 18 Фосфатов 28.09.2016 3Ag+ + PO43- → Ag3PO4↓ Осадок желтого цвета образуется при приливании AgNO3; растворим
- 15. Скачать презентацию




![12 pH 28.09.2016 Когда [H+] > [OH−] говорят, что раствор является](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1315058/slide-6.jpg)






 Сульфаты. Лекция 13
Сульфаты. Лекция 13 Основные понятия химии
Основные понятия химии Фосфорная кислота
Фосфорная кислота Экспертные системы распознавания химических веществ
Экспертные системы распознавания химических веществ Обобщение и подготовка к химии 8 класс
Обобщение и подготовка к химии 8 класс Аттестационная работа. Методическая разработка индивидуальной исследовательской работы по химии педагогического колледжа
Аттестационная работа. Методическая разработка индивидуальной исследовательской работы по химии педагогического колледжа Квантовая механика- теоретическая основа современной химии
Квантовая механика- теоретическая основа современной химии Методы разделения белковых смесей. Электрофорез
Методы разделения белковых смесей. Электрофорез Коррозия металлов
Коррозия металлов Цікаві факти про воду
Цікаві факти про воду  Аминокислоты Модели молекул
Аминокислоты Модели молекул  Основные понятия и законы химии
Основные понятия и законы химии Неньютоновская жидкость
Неньютоновская жидкость Неделя химии в МБОУ Андреевская ООШ
Неделя химии в МБОУ Андреевская ООШ Геохимия природных процессов
Геохимия природных процессов Алкины
Алкины Мұнайды өңдеудің химиялық процестерінің теориялық негіздері
Мұнайды өңдеудің химиялық процестерінің теориялық негіздері Алюминий. Строение и свойства атома
Алюминий. Строение и свойства атома Кристаллография. История развития
Кристаллография. История развития Гетерофункциональные соединения. (Лекция 14)
Гетерофункциональные соединения. (Лекция 14) Презентация по Химии "Соединения серы (11 класс)" - скачать смотреть
Презентация по Химии "Соединения серы (11 класс)" - скачать смотреть  Презентация по Химии "РАСТВОРЕНИЕ. РАСТВОРЫ" - скачать смотреть бесплатно
Презентация по Химии "РАСТВОРЕНИЕ. РАСТВОРЫ" - скачать смотреть бесплатно Атомы, молекулы, химические элементы. Формы существования элементов в природе
Атомы, молекулы, химические элементы. Формы существования элементов в природе Углерод, физические и химические свойства
Углерод, физические и химические свойства Презентация Электролиз
Презентация Электролиз Дюралюминий. Дюраль
Дюралюминий. Дюраль Нефть Состав, свойства, переработка
Нефть Состав, свойства, переработка  Явления физические и химические. Признаки и условия протекания химических реакций
Явления физические и химические. Признаки и условия протекания химических реакций