Содержание
- 2. SO2 SO3 Н2S S Н2SO3 Натисніть на кружок – отримаєте формулу речовини. Опишіть фізичні властивості даної
- 3. Без цієї речовини не обходиться жодна галузь хімічної промисловості. Тому дану речовину називають “хлібом хімічної промисловості”
- 4. Цю кислоту можна придбати в магазині під назвою «акумуляторна» Н2SO4
- 5. Сульфатна кислота. Фізичні та хімічні властивості сульфатної кислоти. Тема уроку:
- 6. Мета уроку: познайомитися з фізичними і хімічними властивостями сульфатної кислоти.
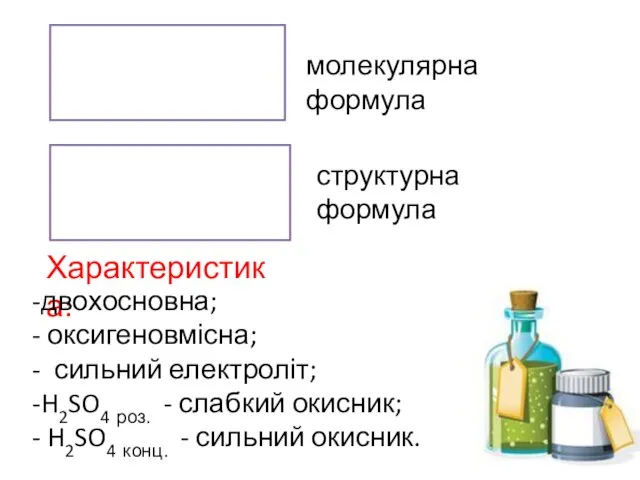
- 7. молекулярна формула структурна формула Характеристика: двохосновна; оксигеновмісна; сильний електроліт; H2SO4 роз. - слабкий окисник; H2SO4 конц.
- 8. Фізичні властивості H2SO4 конц : Робота з підручником с. 128 Безбарвна оліїста рідина. (H2SO4 конц) Важка
- 9. Правила з ТБ під час роботи з H2SO4. При розведенні треба лити кислоту у воду, а
- 10. Хімічні властивості H2SO4 роз. : Дослідіть хімічні властивості розведеної сульфатної кислоти, виконавши лабораторний дослід №3 H2SO4
- 11. Хімічні властивості H2SO4 конц. : 1. H2SO4 конц. – дуже гігроскопічна. Вона здатна відбирати воду навіть
- 12. 2. H2SO4 конц. – сильний окисник, тому взаємодіє з металами незалежно від їх положення в ряді
- 13. не реагують зовсім Li Rb K Ba Sr Ca Na Mg Al Mn Zn Cr Fe
- 14. Виробництво сульфатної кислоти контактним способом
- 15. Сировина: FeS2 – залізний колчедан, пірит S – сірка Сu2S, ZnS, PbS – сульфіди кольорових металів
- 16. І етап – некаталітичне окиснення. FeS2 + O2 → ІІ етап –каталітичне окиснення. V2O5 SO2 +
- 17. Аерозолі сірчаної і сірчистої кислот конденсуються у водяній парі атмосфери і стають причиною кислотних опадів. Вони
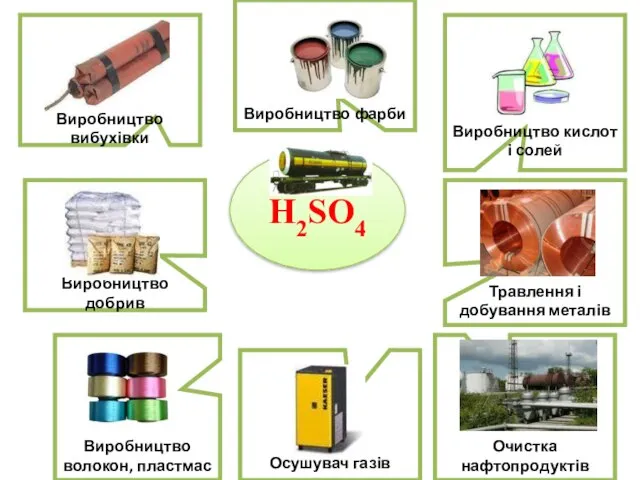
- 18. H2SO4 Виробництво вибухівки Виробництво добрив Виробництво волокон, пластмас Виробництво кислот і солей Виробництво фарби Очистка нафтопродуктів
- 19. З якими із запропонованих речовин: Na , Cu, Na2O, Cu(OH)2, Na2CO3, NaCl, BaCl2 буде реагувати а)
- 21. Скачать презентацию















 Реакционная способность аренов
Реакционная способность аренов Алкадиены. Строение, изомерия, номенклатура, физические и химические свойства
Алкадиены. Строение, изомерия, номенклатура, физические и химические свойства Получение препаратов алкалоидов
Получение препаратов алкалоидов Лекарственные препараты
Лекарственные препараты  Формы нахождения в природе и способы получения простых веществ
Формы нахождения в природе и способы получения простых веществ Химия в мире живописи
Химия в мире живописи Гидролиз
Гидролиз Этилен. Действие этилена на рост проростков гороха
Этилен. Действие этилена на рост проростков гороха Закон сохранения массы веществ
Закон сохранения массы веществ Знакомство с образцами химических средств санитарии и гигиены
Знакомство с образцами химических средств санитарии и гигиены Теорія хімічної будови органічних сполук О.М. Бутлерова
Теорія хімічної будови органічних сполук О.М. Бутлерова  Низшие олефины. Методы производства. Направления использования
Низшие олефины. Методы производства. Направления использования Оксиды углерода (II) и (IV). Качественная реакция на углекислый газ
Оксиды углерода (II) и (IV). Качественная реакция на углекислый газ Взаимодействие элементов-неметаллов между собой. 8 класс
Взаимодействие элементов-неметаллов между собой. 8 класс Биохимическая трансформация веществ (3)
Биохимическая трансформация веществ (3) Индикаторы в нашей жизни
Индикаторы в нашей жизни Бораты и силикаты как матрицы лазеров. Свойства и методы выращивания
Бораты и силикаты как матрицы лазеров. Свойства и методы выращивания Стеклянные товары. Основные сырьевые материалы для производства стекла
Стеклянные товары. Основные сырьевые материалы для производства стекла Строение электронных оболочек атомов
Строение электронных оболочек атомов Kirish. Geokimyoviy namunalarni tahlil qilish
Kirish. Geokimyoviy namunalarni tahlil qilish Обмен веществ и энергии в клетке
Обмен веществ и энергии в клетке Задачник. Основные физические величины в химии
Задачник. Основные физические величины в химии Презентация по Химии "Теория нормализации" - скачать смотреть бесплатно
Презентация по Химии "Теория нормализации" - скачать смотреть бесплатно Предельные углеводороды и их галогенопроизводные. Спирты, эфиры, альдегиды и их производные
Предельные углеводороды и их галогенопроизводные. Спирты, эфиры, альдегиды и их производные Презентация по Химии "Химические тайны запаха" - скачать смотреть
Презентация по Химии "Химические тайны запаха" - скачать смотреть  Сложные эфиры. Жиры
Сложные эфиры. Жиры Белки. Классификация белков. (Тема 2)
Белки. Классификация белков. (Тема 2) Кислотные дожди
Кислотные дожди