Содержание
- 2. ТЕПЛОНОСИТЕЛИ ЯДЕРНЫХ ЭНЕРГЕТИЧЕСКИХ УСТАНОВОК
- 3. ВОДА ГАЗЫ ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ ЖИДКИЕ МЕТАЛЛЫ
- 4. ОСНОВНЫЕ ХАРАКТЕРИСТИКИ ТЕПЛОНОСИТЕЛЕЙ ЯДЕРНЫЕ СВОЙСВА Изотопный состав Сечение захвата нейтронов Наведенная радиоактивность ФИЗИЧЕСКИЕ И ТЕПЛОФИЗИЧЕСКИЕ СВОЙСВА
- 5. ОСНОВНЫЕ ХАРАКТЕРИСТИКИ ТЕПЛОНОСИТЕЛЕЙ ХИМИЧЕСКИЕ СВОЙСВА Взаимодействие с газами Взаимодействие с водой Взаимодействие с технологическими средами Взаимодействие
- 6. Водяной теплоноситель Вода Тяжелая вода
- 7. Газовые теплоносители Углекислый газ Гелий Воздух Азот Водород Диссоциирующие газы
- 8. Свойства газов при давлении 105 Па
- 9. Возможные диссоциирующие системы
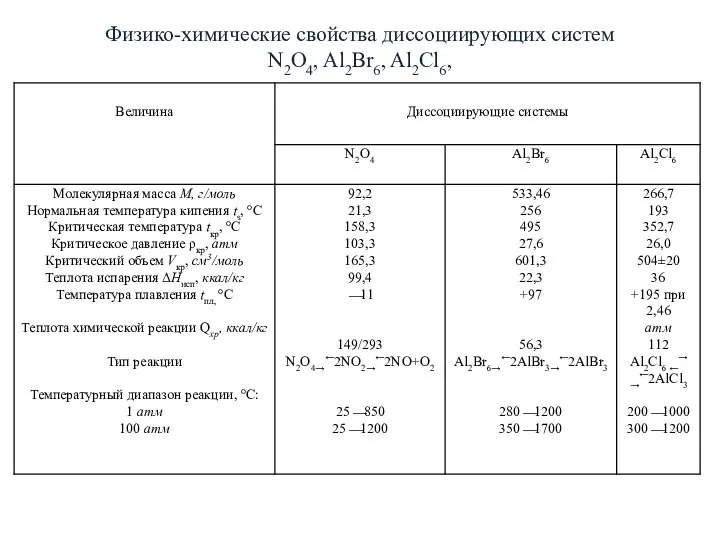
- 10. Физико-химические свойства диссоциирующих систем N2O4, Al2Br6, Al2Cl6,
- 11. Полифенилы: дифенил – С12Н10 терфенил – С18Н14 Органические теплоносители ТЕПЛОФИЗИЧЕСКИЕ СВОЙСТВА ПРИ 300оС
- 12. Жидкие металлы Термодинамика растворов Химическая и диффузионная кинетика Гидродинамика Теория теплообмена Теория массообмена
- 14. ЛИТИЙ Ядерные свойства Природный литий состоит из смеси изотопов 6Li и 7Li Содержание лития-6 в природной
- 15. Сечение реакции 6Li(n,α)T (1) и 7Li(n,n′α)T (2) в зависимости от энергии нейтронов; (3) - пороговая энергия
- 16. Сечения захватов щелочных металлов в зависимости от энергии нейтронов
- 17. ЛИТИЙ Физические, теплофизические свойства Z = 3 Потенциалы ионизации лития относительно высоки: I - 5,3918 эВ,
- 18. Основные свойства лития
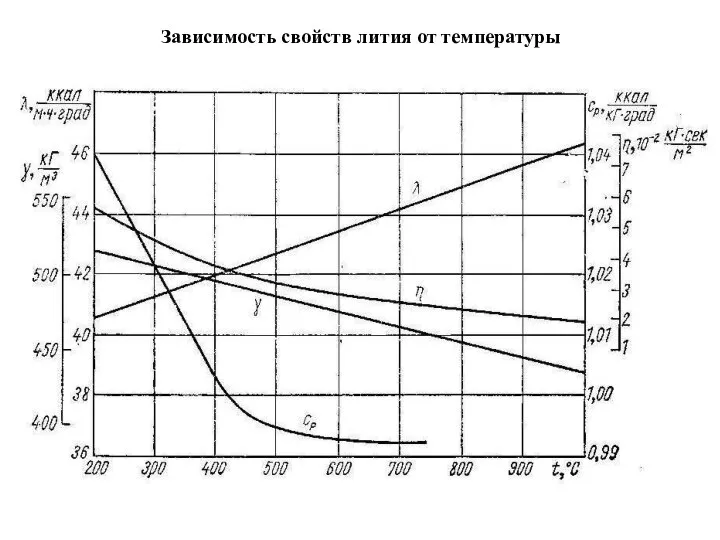
- 19. Зависимость свойств лития от температуры
- 20. Зависимость давления паров лития от температуры
- 21. НАТРИЙ Физические, теплофизические свойства Z = 11 Потенциалы ионизации натрия: I - 5,138 эВ, II -
- 23. НАТРИЙ Ядерные свойства Природный натрий имеет один стабильный изотоп 23Na Искусственные изотопы 20Na, 21Na, 22Na, 24Na
- 24. Основные свойства натрия
- 25. Зависимость давления паров натрия от температуры
- 26. КАЛИЙ Физические, теплофизические свойства Z = 19 Потенциалы ионизации калия: I - 4,339 эВ, II -
- 27. КАЛИЙ Ядерные свойства Природный калий является смесью стабильных изотопов 39К – 93% и 41К – 7%
- 28. Основные свойства калия
- 29. Зависимость давления паров калия от температуры
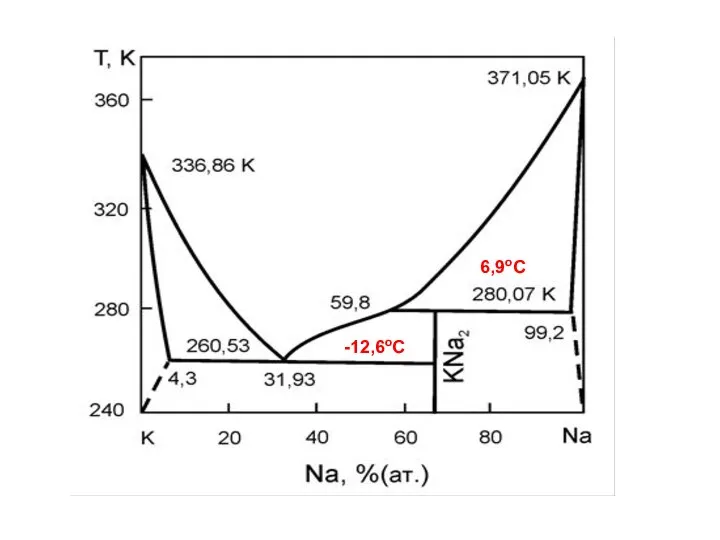
- 30. ЭВТЕКТИКА НАТРИЙ – КАЛИЙ 77,2%K – 22,8%Na
- 31. -12,6оС 6,9оС
- 32. Изотермы активности и коэффициента активности в системе Na - K
- 33. ЦЕЗИЙ Физические, теплофизические свойства Z = 55 Потенциалы ионизации цезия: I - 3,893 эВ, II -
- 34. ЦЕЗИЙ Ядерные свойств Природный цезий состоит из стабильного изотопа 133Cs
- 35. Основные свойства цезия
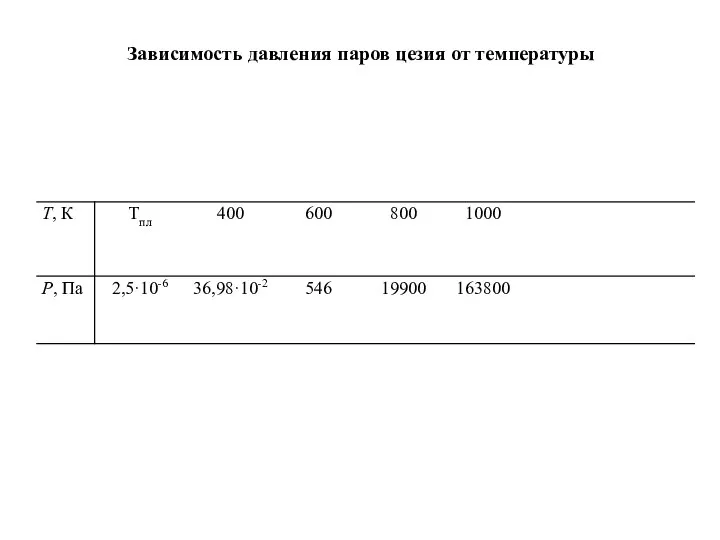
- 36. Зависимость давления паров цезия от температуры
- 37. СВИНЕЦ Физические, теплофизические свойства Z = 82 Потенциалы ионизации свинца: I - 7,415 эВ, II -
- 38. СВИНЕЦ Ядерные свойства Природный свинец является смесью стабильных изотопов 204Pb – 1,48%, 206Pb – 23,6%, 207Pb
- 39. Основные свойства свинца
- 40. Зависимость давления паров свинца от температуры
- 41. ВИСМУТ Физические, теплофизические свойства Z = 83 Потенциалы ионизации висмута: I - 7,237 эВ II -
- 42. ВИСМУТ Ядерные свойства Природный висмут имеет один стабильный изотоп 209Bi Висмут имеет более 20 искусственных изотопов
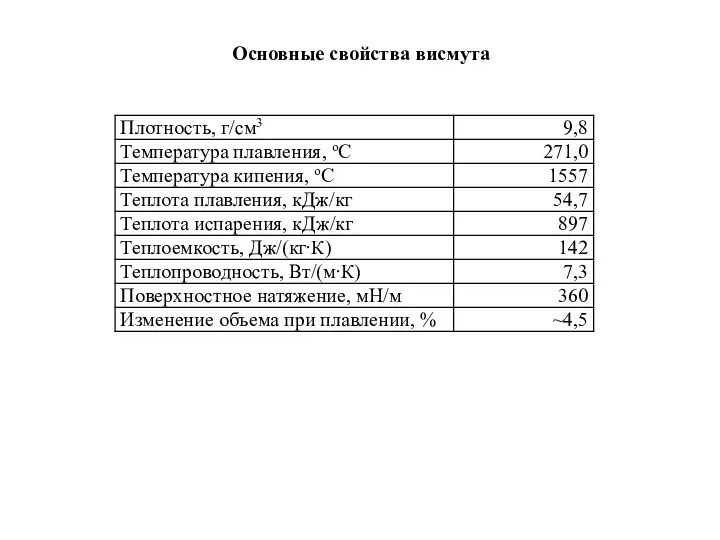
- 43. Основные свойства висмута
- 44. Зависимость давления паров висмута от температуры
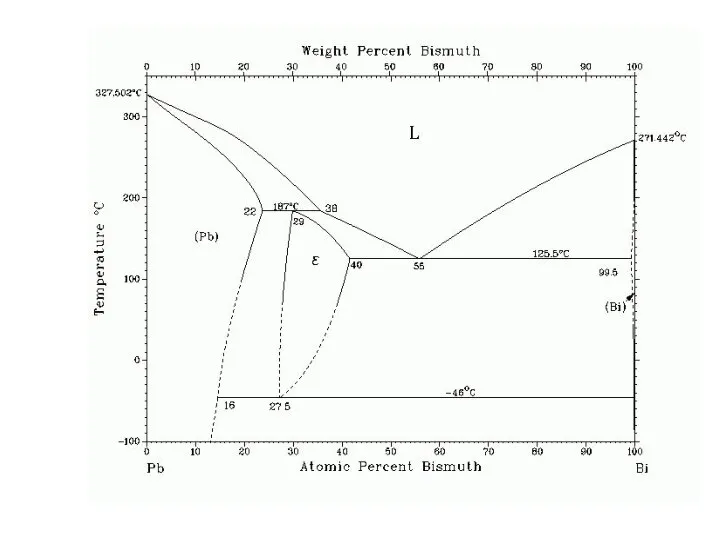
- 45. ЭВТЕКТИКА СВИНЕЦ– ВИСМУТ 45%Pb – 55%Bi
- 47. ЭВТЕКТИКА СВИНЕЦ– ЛИТИЙ 83%Pb – 17%Li Содержание лития в Li17Pb83 -0,065 г/см3
- 49. Как показали измерения, проведенные с помощью метода Кнудсена и метода определения ЭДС, жидкий раствор Li -
- 50. Основные свойства эвтектики 83%Pb – 17%Li
- 51. Давление паров Li17Pb83 можно вычислить по формуле Р = аLiРLi + аPbРPb, где а Li, аPb
- 52. ГАЛЛИЙ Физические, теплофизические свойства Z = 31 Потенциалы ионизации галлия: I - 6,00 эВ, II -
- 53. ГАЛЛИЙ Ядерные свойства Природный галлий состоит из двух стабильных изотопов 69Ga – 61% и 71Ga –
- 54. Основные свойства галлия
- 56. Зависимость давления паров галлия от температуры
- 57. ОЛОВО Физические, теплофизические свойства Z = 50 Потенциалы ионизации галлия: I - 7,33 эВ, II -
- 58. ОЛОВО Ядерные свойства Природный галлий состоит из десяти стабильных изотопов 112Sn – 0,95%, 114Sn – 0,65%,
- 59. Основные свойства олова
- 60. Зависимость давления паров олова от температуры
- 62. Скачать презентацию





















































 Наличие 2 х сигналов в ЯМР 1Н (задача)
Наличие 2 х сигналов в ЯМР 1Н (задача) обобщение знаний
обобщение знаний Простой борный суперфосфат
Простой борный суперфосфат Ассортимент и качество изделий из пластмасс (урок 84)
Ассортимент и качество изделий из пластмасс (урок 84) Жесткость воды и способы ее устранения
Жесткость воды и способы ее устранения Практика по химии
Практика по химии Галогены
Галогены Жири. Жири в природі. Біологічна роль жирів. Жири. Жири в природі. Біологічна роль жирів.
Жири. Жири в природі. Біологічна роль жирів. Жири. Жири в природі. Біологічна роль жирів.  Химический состав клетки. Неорганические вещества клетки. Глава 1
Химический состав клетки. Неорганические вещества клетки. Глава 1 Физико-химические свойства белков. Электрофоретические и хроматографические методы
Физико-химические свойства белков. Электрофоретические и хроматографические методы Технология получения полиуретанов
Технология получения полиуретанов Природные (натуральные) полимеры. Композиционные материалы
Природные (натуральные) полимеры. Композиционные материалы Химические реактивы
Химические реактивы Презентация по Химии "Строение атома" - скачать смотреть бесплатно_
Презентация по Химии "Строение атома" - скачать смотреть бесплатно_ Металлы ГОУ СОШ № 661 УЧИТЕЛЬ ХИМИИ Ефремова С.А.
Металлы ГОУ СОШ № 661 УЧИТЕЛЬ ХИМИИ Ефремова С.А. Машиностроительные материалы
Машиностроительные материалы Углерод и кремний
Углерод и кремний Химическая кинетика. Лекция 2
Химическая кинетика. Лекция 2 Положение в ПСХЭ Д.И.Менделеева и строение атома
Положение в ПСХЭ Д.И.Менделеева и строение атома Рождающий воду
Рождающий воду Химические формулы. Относительные атомная и молекулярная массы. Расчетные задачи
Химические формулы. Относительные атомная и молекулярная массы. Расчетные задачи Особенности строения, реакционной способности и методы синтеза аренов
Особенности строения, реакционной способности и методы синтеза аренов Лекарственное растительное сырье, содержащее алкалоиды
Лекарственное растительное сырье, содержащее алкалоиды Хімія та обмін ліпідів
Хімія та обмін ліпідів Химические свойства металлов
Химические свойства металлов «Аспирин» Выполнила ученица 11 «Б»класса Панина Евгения
«Аспирин» Выполнила ученица 11 «Б»класса Панина Евгения  Органические галогениды. (Лекция 7)
Органические галогениды. (Лекция 7) Кристаллохимия. Тығыз шарлар теориясы
Кристаллохимия. Тығыз шарлар теориясы