Содержание
- 2. Термодина́мика (греч. θέρμη — «тепло», δύναμις — «сила») Химическая термодинамика - это раздел термодинамики, изучающий взаимные
- 3. Основные понятия термодинамики Термодинамическая система (тдс) – это совокупность материальных объектов (тел, образованных различными веществами), отделенных
- 4. Системы бывают: открытые - могут обмениваться и энергией, и веществом. закрытые - могут обмениваться только энергией.
- 5. Определите тип тдс
- 6. Состояние системы – это совокупность всех физических и химических свойств системы. Это состояние описывают с помощью
- 7. Внутренняя энергия (U) – это энергия, которой обладает тело в состоянии равновесия, т.е. скрытая в веществах
- 8. 0-й закон (нулевое начало термодинамики) Равновесие Для каждой изолированной термодинамической системы существует состояние термодинамического равновесия, которого
- 9. Термодинамическое равновесие (тдс) динамическое, т.е. в системе продолжают протекать процессы, но в противоположном направлении и скорости
- 10. 1-й закон (первое начало термодинамики) Закон сохранения энергии Теплота, поглощенная системой или выделенная ею, расходуется на
- 11. Совокупность внутренней энергии тела и энергии его взаимодействия с окружающей средой объединяется понятием «энтальпия». (Н) Это
- 12. Термохимические уравнения - указывается агрегатное состояние веществ (г, ж, т); - указывается знак и значение теплового
- 13. Закон Лавуазье – Лапласа – еще одна формулировка закона сохранения энергии Если при образовании какого-либо соединения
- 14. Энтальпия образования вещества (теплота образования) ∆Н0 2Н2 (г) + О2 (г) = 2Н2О (г) + 483,68
- 15. Теплота сгорания вещества «Теплота сгорания», это количество теплоты, выделяющейся при окислении одного моля какого-то соединения. Например:
- 16. Расчеты по термохимическим уравнениям Какой объем углекислого газа выделится в реакции разложения известняка, если на реакцию
- 17. Закон Германа Гесса(1841) – еще одна формулировка закона сохранения энергии Тепловой эффект (энтальпия) процесса зависит только
- 18. Следствием из этого закона является возможность расчета теплового эффекта реакции. Математически это можно записать так: ΔНхимической
- 19. Расчеты по уравнению Гесса Определить тепловой эффект реакции взаимодействия метана с кислородом. Записать уравнение реакции Выписать
- 20. Измерение теплового эффекта химической реакции Калориметрическое определение ведется так, чтобы энергия химической реакции выделялась в виде
- 21. Всем живым организмам для роста и функционирования нужна энергия. Организм человека не продуцирует новую энергию. Все
- 22. Применение калориметрии в медицине Сравнение энергетики здоровых и больных клеток позволяет изучать различные патологические явления, разрабатывать
- 23. 2-й закон (второе начало) термодинамики. Закон возрастания энтропия (S). Второе начало термодинамики (закон возрастания энтропии) позволяет
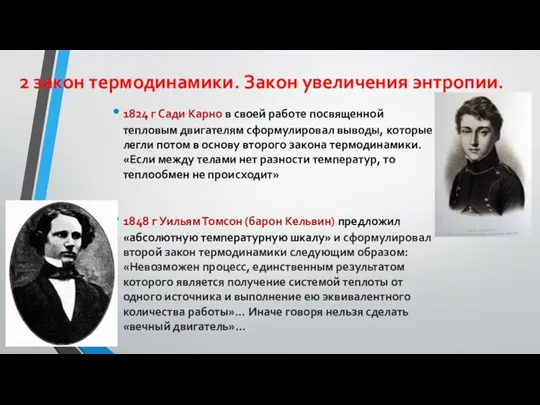
- 24. 2 закон термодинамики. Закон увеличения энтропии. 1824 г Сади Карно в своей работе посвященной тепловым двигателям
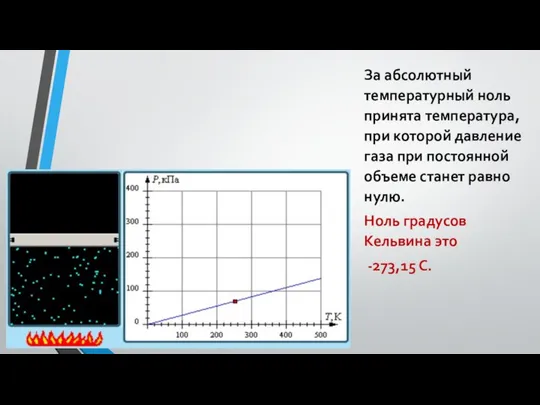
- 25. За абсолютный температурный ноль принята температура, при которой давление газа при постоянной объеме станет равно нулю.
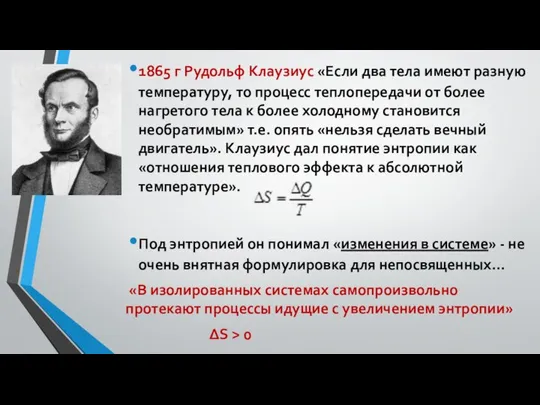
- 26. 1865 г Рудольф Клаузиус «Если два тела имеют разную температуру, то процесс теплопередачи от более нагретого
- 27. 1877 Людвиг Больцман показал связь между энтропией и вероятностью микросостояний физической системы. Закон возрастания энтропии у
- 28. 1876 г Джозайя Уиллард Гиббс сформулировал закон, согласно которому «любой самопроизвольно протекающий процесс идет в том
- 29. Итак, в химических процессах одновременно изменяются энергетический запас системы (энтальпийный фактор) и степень ее беспорядка (энтропийный
- 30. Чаще всего для определения возможности самопроизвольного процесса в тдс пользуются изменением изобарно-изотермического потенциала, т.н. свободной энергии
- 31. Определение возможности самопроизвольного процесса Определите, возможен ли самопроизвольный процесс по уравнению Al2O3 + H2 → H2O
- 32. Третий закон термодинамики. Абсолютный порядок. 1906 г Вальтер Герман Нернст опубликовал свою формулировку третьего закона термодинамики,
- 34. Скачать презентацию




























 ПРЕЗЕНТАЦІЯ З ХІМІЇ НА ТЕМУ: АЦЕТИЛЕН
ПРЕЗЕНТАЦІЯ З ХІМІЇ НА ТЕМУ: АЦЕТИЛЕН  Configuratia electronica. Sistemul periodic al elementelor. (Curs 3)
Configuratia electronica. Sistemul periodic al elementelor. (Curs 3) Устойчивость и резистентность вредных организмов к пестицидам и пути ее преодоления. (Лекция 4)
Устойчивость и резистентность вредных организмов к пестицидам и пути ее преодоления. (Лекция 4) Просто знать еще не все, знания необходимо еще использовать
Просто знать еще не все, знания необходимо еще использовать Программа дополнительного образования Химия, здоровье и окружающая среда
Программа дополнительного образования Химия, здоровье и окружающая среда Окислительно-восстановительные реакции
Окислительно-восстановительные реакции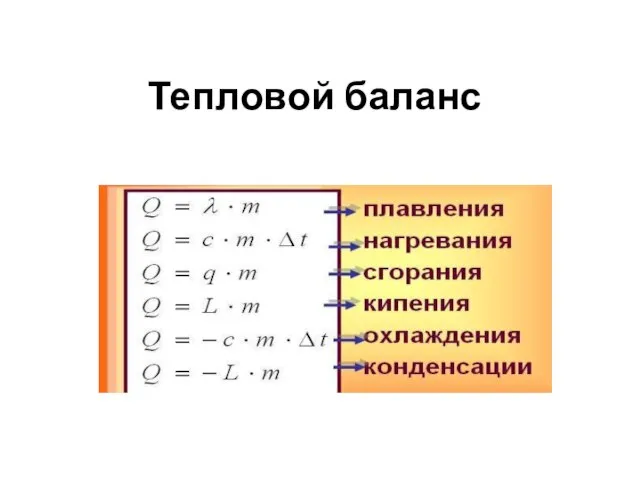 Тепловой баланс
Тепловой баланс Конструкция ферментатора
Конструкция ферментатора Хлорид калия KCI
Хлорид калия KCI Введение в химию органических соединений
Введение в химию органических соединений Вода. Твердість води
Вода. Твердість води  Презентация на тему: Кислотные дожди
Презентация на тему: Кислотные дожди Анализ процесса гальванического нанесения рения. Поиск альтернативных способов нанесения рения
Анализ процесса гальванического нанесения рения. Поиск альтернативных способов нанесения рения Біоорганічна хімія. Реакційна здатність біоорганічних сполук
Біоорганічна хімія. Реакційна здатність біоорганічних сполук Массовая доля элемента в соединении
Массовая доля элемента в соединении Алканы: метан, пропан, этан, бутан
Алканы: метан, пропан, этан, бутан Реакции ионного обмена
Реакции ионного обмена Пиролиз. Паровой крекинг углеводородов
Пиролиз. Паровой крекинг углеводородов Работу выполнила: Пьянкова Елена Руководитель: Баранова Алевтина Владимировна 2010
Работу выполнила: Пьянкова Елена Руководитель: Баранова Алевтина Владимировна 2010 Взаимодействие атомов элементов-металлов и элементов-неметаллов между собой. Ионная связь. (Тема 10)
Взаимодействие атомов элементов-металлов и элементов-неметаллов между собой. Ионная связь. (Тема 10) Солеобразующие оксиды
Солеобразующие оксиды Строение атома (лекция 3)
Строение атома (лекция 3) Предмет и задачи токсикологической химии. Взаимосвязь с другими дисциплинами. (Лекция 1)
Предмет и задачи токсикологической химии. Взаимосвязь с другими дисциплинами. (Лекция 1) Презентация по Химии "Сера" - скачать смотреть
Презентация по Химии "Сера" - скачать смотреть  Микрофлора и биохимические реакции подземных вод
Микрофлора и биохимические реакции подземных вод Алкены (этиленовые углеводороды, олефины)
Алкены (этиленовые углеводороды, олефины) Газовые законы
Газовые законы Наблюдения в сходящемся свете. Коноскопия
Наблюдения в сходящемся свете. Коноскопия