Тема урока Железо Цель урока: Рассмотреть электронное строение атома железа, дать общую характеристику его. Изучить основные
Содержание
- 2. Проверка домашнего задания Упражнение №5 Al2 (SO4)3+ KOH(нед) = Al 2(SO4)3+ KOH(изб.) = Упражнение №6 Al
- 3. Ответы Упражнения №5 1.Al2 (SO4)3 + 6KOH(нед.) = 2AL(OH)3 +3K2SO4 2. Al2 (SO4)3 + 8KOH(изб) =
- 4. Упражнение №6 2Al +3Cl2 = 2AlCl3 AlCl3 + 3NaOH =Al(OH)3 + 3NaCl 2Al(OH)3 = Al2O3 +
- 5. Изучение нового материала Характеристика по плану: 1.Положение железа в ПСХЭ (период, ряд, группа, подгруппа, порядковый номер)
- 6. Характеристика элемента 4-период, 4ряд, 8-группа, побочная подгруппа, порядковый номер 26 26 электронов, 26 протонов, относительная атомная
- 7. Физические свойства железа Серебристо-серый, мягкий металл, обладает хорошей пластичностью, ковкостью и способностью к намагничиванию. Плотность 7,864г/см3,
- 8. Степени окисления Fe0 +2 +2; +3; +3 S, Cu+2 ,HCl(раз) , O2 H2O Cl2 HNO3 H2SO4(раз)
- 9. Химические свойства При нагревании 2Fe + 3Cl2 =2FeCl3 3Fe +2O2= Fe3O4 (FeO Fe2O3) Fe +S =FeS
- 10. Химические свойства Fe + CuSO4 = Cu + FeSO4 Fe + 2HClр = FeCl2 + H2
- 11. При нагревании 2Fe + 6H2SO4(k)=Fe2(SO4)3 + 3SO2+6H2O Fe+ 6HNO3(k)= Fe(NO3)3+ 3NO2+ 3H2O
- 12. Химические свойства Fe0 + HNO3 (p) = Fe +2(NO3 )2 + N20 + H2 O Fe0
- 13. Уравнивание реакций 5Fe0 + 12 HN+5 O3 (p) = 5Fe +3(NO3 )2 + N20 +6 H2
- 14. Минералы железо Fe3O4 магнитный железняк или магнетит Fe2O3 красный железняк или гематит 2Fe2O3.3H2O бурый железняк или
- 15. Применение Магнитный, красный, бурый железняки –для производства черной металлургии (чугуна и стали) Железный колчедан – для
- 16. Источники железа Шпинат Салат Капуста Черная черешня Говядина Телятина
- 18. Скачать презентацию















 Синтетические моющие средства
Синтетические моющие средства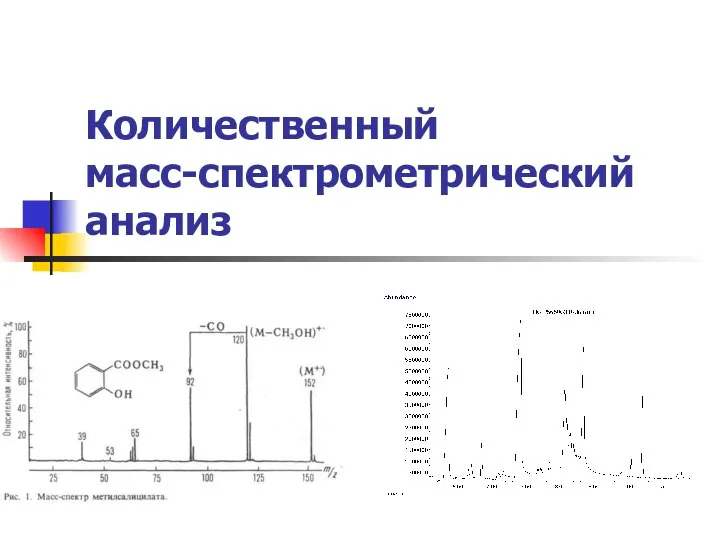 Количественный масс-спектрометрический анализ
Количественный масс-спектрометрический анализ Растворы ВМС и их свойства
Растворы ВМС и их свойства Псевдовідкриття хімічних елементів
Псевдовідкриття хімічних елементів Водород на Земле и в космосе
Водород на Земле и в космосе Коллигативные свойства растворов. Осмос. Осмотическое давление
Коллигативные свойства растворов. Осмос. Осмотическое давление Гидрокарбонат натрия NaHCO₃
Гидрокарбонат натрия NaHCO₃ Atomic structure. Introduction
Atomic structure. Introduction ЕГЭ 2017. Подготовка к вопросу № 26
ЕГЭ 2017. Подготовка к вопросу № 26 Green chemistry application to intermolecular forces
Green chemistry application to intermolecular forces Сера. Историческая справка
Сера. Историческая справка Экзогенная серия Осадочная группа
Экзогенная серия Осадочная группа Элементы группы галогенов
Элементы группы галогенов Аттестационная работа. Рабочая программа курса внеурочной деятельности «Химия. Мои первые опыты»
Аттестационная работа. Рабочая программа курса внеурочной деятельности «Химия. Мои первые опыты» Растворы. Часть 2
Растворы. Часть 2 Натрий (Na)
Натрий (Na) Природный и попутный газы, их состав и использование
Природный и попутный газы, их состав и использование Важнейшие понятия химии и их взаимосвязь
Важнейшие понятия химии и их взаимосвязь Водород. Получение водорода
Водород. Получение водорода Введение в химию. Теоретические основы химии
Введение в химию. Теоретические основы химии Химия: основные понятия
Химия: основные понятия Темір және оның маңызды қосылыстары
Темір және оның маңызды қосылыстары Генетическая связь веществ Задачи урока : 1.Познакомиться с понятием «генетическая связь» 2. Научиться составлять генетические р
Генетическая связь веществ Задачи урока : 1.Познакомиться с понятием «генетическая связь» 2. Научиться составлять генетические р Плазма та її властивості. Практичне застосування плазми. (11 клас)
Плазма та її властивості. Практичне застосування плазми. (11 клас) Цикл три і дикарбонових кислот (Цикл Кребса)
Цикл три і дикарбонових кислот (Цикл Кребса) Хром
Хром Алкины
Алкины Презентация по Химии "Электролитическая диссоциация веществ" - скачать смотреть
Презентация по Химии "Электролитическая диссоциация веществ" - скачать смотреть