Для обеспечения этих критериев необходимо соблюдение, по крайней мере, следующих условий:
1)
молекулы органических реагентов должны содержать ФАГ;
2) ФАГ должны иметь такую пространственную конфигурацию и взаимное расположение донорных атомов (азота, кислорода, серы, фосфора, мышьяка и др.), чтобы могла реализоваться возможность образования наиболее устойчивых пяти- и шестичленных металлоциклов;
3) молекула органического лиганда должна иметь, по возможности, большую молекулярную массу – это понижает погрешности определения металлов.
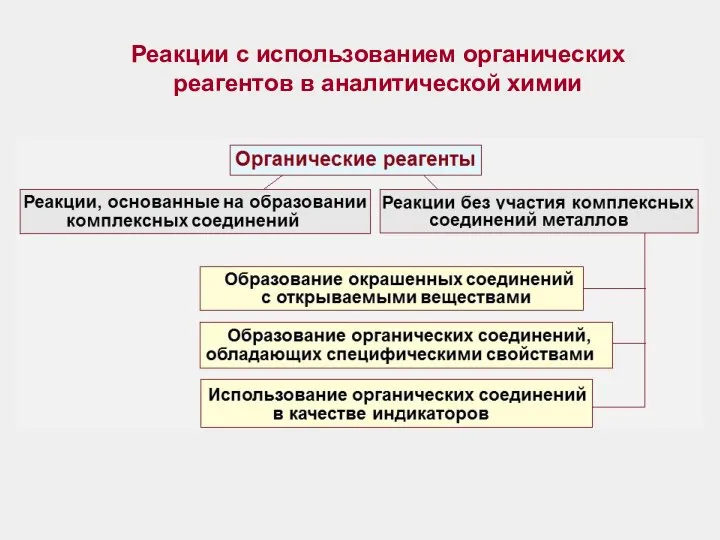
Некоторые органические реагенты позволяют открывать или определять целый ряд катионов.
К числу таких органических реагентов относятся соединения группы арсеназо, содержащие мышьяк, азогруппы, SO3H, ОН (арсеназо І, арсеназо ІІ, арсеназо ІІІ, полиарсеназо).
С помощью арсеназо I можно определять уранильную группу UO22+, катионы кальция Са2+, бериллия Ве2+, меди Сu2+, кобальта Со2+, никеля Ni2+, А13+, редкоземельных металлов, титан(III), цирконий(IV), торий(IV), ванадий(V), ниобий(V), тантал(V), а также анионы F‾, BF4‾.
Арсеназо III позволяет определять катионы Ве2+, Mg2+, Ca2+, Zn2+, Cd2+, Hg2+, Al3+, Pb2+, редкоземельных металлов, титан(IV), цирконий(IV), гафний(IV), торий(IV).









 Гиалурон қышқылы
Гиалурон қышқылы Минералы
Минералы Водорастворимые витамины. 7 свойств водорастворимых витаминов
Водорастворимые витамины. 7 свойств водорастворимых витаминов Азот в природе
Азот в природе Сапфиры. Месторождения сапфира
Сапфиры. Месторождения сапфира Основные понятия и законы химии
Основные понятия и законы химии - Это оружие массового поражения, действие которого основано на токсических свойствах химических веществ. - Это оружие массового
- Это оружие массового поражения, действие которого основано на токсических свойствах химических веществ. - Это оружие массового  Особенности химии, связанные с её физикализацией. Дифференциация и интеграция науки
Особенности химии, связанные с её физикализацией. Дифференциация и интеграция науки Презентация по Химии "Алкены." - скачать смотреть бесплатно_
Презентация по Химии "Алкены." - скачать смотреть бесплатно_ Прогнозування хімічної обстановки під час застосування хімічної зброї
Прогнозування хімічної обстановки під час застосування хімічної зброї Каталитическое жидкофазное окисление глюкозы в глюконовую кислоту в присутствии катализаторов Pd-Sn/Al2O3
Каталитическое жидкофазное окисление глюкозы в глюконовую кислоту в присутствии катализаторов Pd-Sn/Al2O3 Викторина Своя игра по химии
Викторина Своя игра по химии Химическая реакция
Химическая реакция Чистящие и моющие средства для мытья посуды
Чистящие и моющие средства для мытья посуды Коллоидная химия
Коллоидная химия Аміак
Аміак  Қазіргі кезде қолданылатын дезинсектицидтер
Қазіргі кезде қолданылатын дезинсектицидтер Федеральное агентство по образованию Государственное образовательное учреждение высшего профессионального образования Томский
Федеральное агентство по образованию Государственное образовательное учреждение высшего профессионального образования Томский Хімія та обмін ліпідів
Хімія та обмін ліпідів Исследование свойств моющих средств
Исследование свойств моющих средств Личностно – ориентированный подход в обучении химии Талавир С.Е. Учитель химии МОУ СОШ№5
Личностно – ориентированный подход в обучении химии Талавир С.Е. Учитель химии МОУ СОШ№5 Силикатная промышленность
Силикатная промышленность Генетическая связь между классами веществ
Генетическая связь между классами веществ Химическая викторина Пятый элемент
Химическая викторина Пятый элемент Хлор. Отравления хлором
Хлор. Отравления хлором Презентация по Химии "Основания, их классификация и свойства в свете теории электролитической диссоциации" - скачать смотрет
Презентация по Химии "Основания, их классификация и свойства в свете теории электролитической диссоциации" - скачать смотрет Металлокомплексный катализ. (Лекция 16)
Металлокомплексный катализ. (Лекция 16) Серосодержащие макрогетероциклы (тиакраун-соединения)
Серосодержащие макрогетероциклы (тиакраун-соединения)