Содержание
- 2. Когда-нибудь настанет время – и это время не за горами, – когда мерилом ценности станет не
- 3. Начало всех начал – водород! Водород — основная составная часть звёзд и межзвёздного газа. В условиях
- 4. Водород в космосе
- 5. Ближайшая к нам звезда Галактики, которую мы знаем под именем «Солнце», на 70 % своей массы
- 6. Водород на Земле Вода Нефть Природный газ
- 7. В 1766 году известный английский ученый Генри Кавендиш получил «искусственный воздух» (так часто называли в то
- 8. Химический элемент Порядковый номер 1 Группа – I Период – 1 Электронная формула 1s1 Степени окисления:
- 9. Физические свойства Водород — легчайшее из всех известных веществ (в 14,4 раза легче воздуха), это бесцветный
- 10. Опыт Пилатра де Розьера Как-то он решил проверить, что будет, если вдохнуть водород; до него никто
- 11. В промышленности: 2NaCl + 2H2O → H2↑ + 2NaOH + Cl2 СН4 + 2Н20 = CO2
- 12. В лаборатории: Zn + 2HCl → ZnCl2 + H2↑ Ca + 2H2O → Ca(OH)2 + H2↑
- 13. 1. Взаимодействие с активными металлами – окислительные свойства При комнатной температуре 2K + H2→2KH (гидрид калия)
- 14. Вывод: В соединениях с металлами,водород образует гидриды – бинарные соединения, твердые солеподобные вещества. (KH, CaH2, AlH3)
- 15. 2. Взаимодействие с неметаллами – восстановительные свойства При комнатной температуре водород реагирует с фтором F2+H2→2HF↑ (фтороводород),
- 16. при нагревании водород взаимодействует с серой: Н2 + S→Н2S↑ (сероводород) при высокой температуре, давлении и в
- 17. Вывод: В результате реакций с неметаллами образуются газообразные вещества ( HF↑ , HCl ↑, Н2S↑, NH3↑
- 18. 3. Реакция горения При взаимодействии водорода с кислородом образуется вода. Водород без примесей сгорает спокойно. 2
- 19. Гремучая смесь Наиболее взрывчата смесь, состоящая из двух объёмов водорода и одного объёма кислорода – «гремучий
- 20. 4.Взаимодействие с оксидами не активных металлов ОксидыОксиды восстанавливаются до металлов: СuO + H2 = H2O +
- 21. Вывод: Водород восстанавливает металлы из их оксидов, поэтому водород является восстановителем. H2 восстановитель
- 22. Выводы: 1). В обычных условиях молекулярный водород взаимодействует лишь с наиболее активными веществами - фтором, натрием
- 23. Применение водорода в промышленности
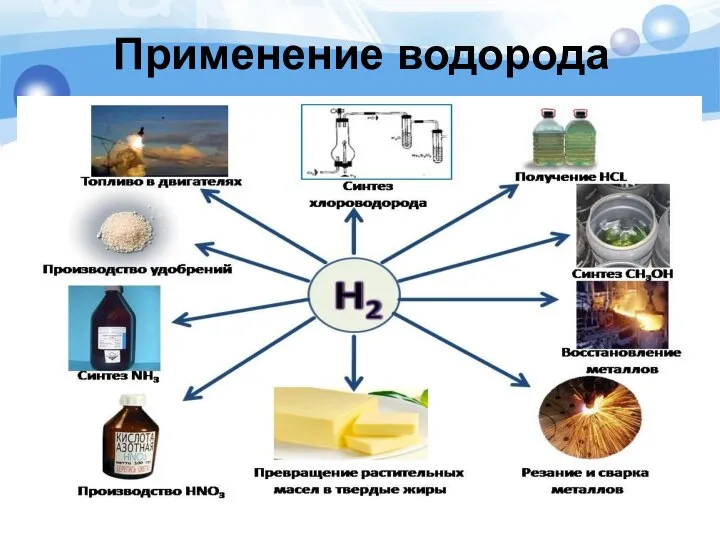
- 24. Использование водорода в качестве топлива автомобилей При сгорании водорода в кислороде образуется экологически чистый продукт –
- 25. Использование водорода в ракетных двигателях Жидкий водород является распространенным компонентом ракетного топлива
- 26. Использование водорода в металлургической промышленности Водород как восстановитель, для получения металлов и неметаллов (кремния, вольфрама)
- 27. Сварка металла Смесь кислорода с водородом используют при сварке и резке металлов.
- 28. Производство стекла Водород является активным газом и в соединениях с азотом может использоваться в производстве листового,
- 29. В пищевой промышленности Превращение жидких растительных масел в твердые жиры – маргарин.
- 30. В продажу водород поступает в баллонах под давлением свыше 150 атм. Они окрашены в тёмно-зелёный цвет
- 31. Применение водорода
- 32. Задачи: Какая масса водорода потребуется для его взаимодействия с 64г серы. Какой объём водорода израсходуется на
- 34. Скачать презентацию






























 Топливо и его свойства
Топливо и его свойства Квалификация химических реактивов, принятая в РФ
Квалификация химических реактивов, принятая в РФ Термокаталитические процессы. Каталитический крекинг. Классификация и основные факторы процесса
Термокаталитические процессы. Каталитический крекинг. Классификация и основные факторы процесса Комплексные соединения. Лекция № 3
Комплексные соединения. Лекция № 3 Ферменти мікробіологічного синтезу
Ферменти мікробіологічного синтезу Анілін. Фізичні властивості
Анілін. Фізичні властивості Биохимия нервной и мышечной ткани
Биохимия нервной и мышечной ткани Реакции горения и материальный баланс котла
Реакции горения и материальный баланс котла Устойчивость и коагуляция коллоидных растворов
Устойчивость и коагуляция коллоидных растворов Молекулярная адсорбция. (Лекция 2)
Молекулярная адсорбция. (Лекция 2) Железо Железо не только основа всего мира, самый главный металл окружающей нас природы, оно – основа культуры и промышленности,
Железо Железо не только основа всего мира, самый главный металл окружающей нас природы, оно – основа культуры и промышленности,  Симметрия, структура и свойства твердых тел – кристаллография и кристаллофизика
Симметрия, структура и свойства твердых тел – кристаллография и кристаллофизика ГИА. А1: Строение атомов первых 20 химических элементов ПСХЭ
ГИА. А1: Строение атомов первых 20 химических элементов ПСХЭ Стартап. Производство минерального удобрения
Стартап. Производство минерального удобрения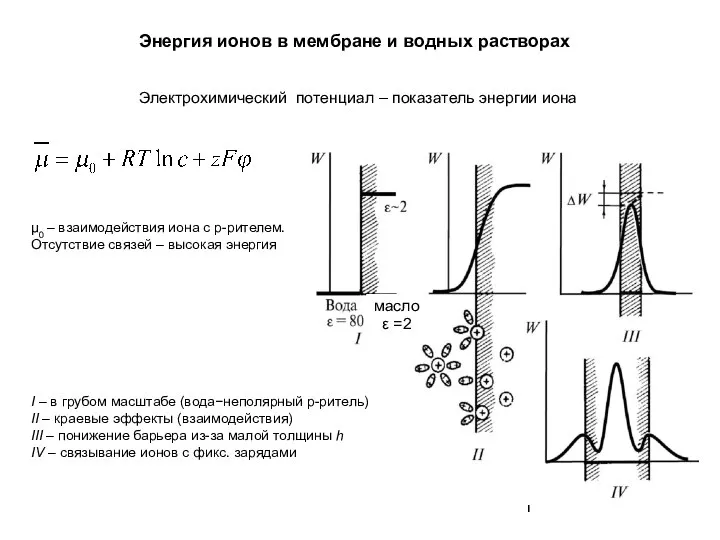 Энергия ионов в мембране и водных растворах
Энергия ионов в мембране и водных растворах Правила техники безопасности. Приемы обращения с лабораторным оборудованием
Правила техники безопасности. Приемы обращения с лабораторным оборудованием Карбонові кислоти. Насичені карбонові кислоти
Карбонові кислоти. Насичені карбонові кислоти Регуляция и патология липидного обмена
Регуляция и патология липидного обмена Количество вещества
Количество вещества Окислительно - восстановительные реакции
Окислительно - восстановительные реакции Химиялық реакцияның жылдамдығы. Катализ
Химиялық реакцияның жылдамдығы. Катализ Автоматизована мікропроцесорна система контролю концентрації речовин в розчинах
Автоматизована мікропроцесорна система контролю концентрації речовин в розчинах “ КОРОЗІЯ МЕТАЛІВ. ЗАХИСТ ВІД КОРОЗІЇ ” Підготував: Учень 10-А класу ЗОШ №25 м. Луцька Матвійчук Роман
“ КОРОЗІЯ МЕТАЛІВ. ЗАХИСТ ВІД КОРОЗІЇ ” Підготував: Учень 10-А класу ЗОШ №25 м. Луцька Матвійчук Роман  Качество питьевой воды
Качество питьевой воды Основные законы химии
Основные законы химии Рецепторы анионов
Рецепторы анионов Мұнай, құрамыөңдеу әдістері
Мұнай, құрамыөңдеу әдістері Фосфор, строение, свойства
Фосфор, строение, свойства