Загальна характеристика неметалічних елементів. Неметали як прості речовини. Явище алотропії, алотропні видозміни Оксигену і
Содержание
- 2. Прості речовини поділяють на: метали (натрій Na, цинк Zn, барій Ва, магній Mg) неметали (сірка S,
- 4. Неметали – це хімічні элементи, які утворюють в вільному вигляді прості речовини, які немають фізичних властивостей
- 5. Неметали Неметали – прості речовини, які не мають властивостей металів, а саме: металічного блиску, непридатні для
- 6. Неметали
- 7. Властивості неметалів Неметали можуть мати як молекулярну, так і немолекулярну структури. Вони погано проводять теплоту й
- 8. Сірка Фосфор Карбон
- 9. Неметали мають різний агрегатний стан за звичайних умов:
- 10. Азот Гелій Сіліцій Бром
- 12. Положення неметалів в ПС Неметали розташовані в основному в правому верхньому куті ПС, умовно обмеженому діагоналлю
- 14. Особливості будови атомів неметалів. Атоми неметалічних елементів на зовнішньому енергетичному рівні мають, як правило, від 4
- 15. Приклад перетворення атома Сульфуру на сульфід-іон:
- 16. Елементи - неметали більш здатні, в порівнянні з металами, до алотропії. Здатність атомів одного хімічного елемента
- 17. Алотропні модифікації Алотропія (від гр. ἄλλος, állos — інший і τρόπος, trópos — властивість Здатність атомів
- 18. Поширення в природі. Оксиген – найпоширеніший елемент у природі. Входить до складу води, багатьох мінералів і
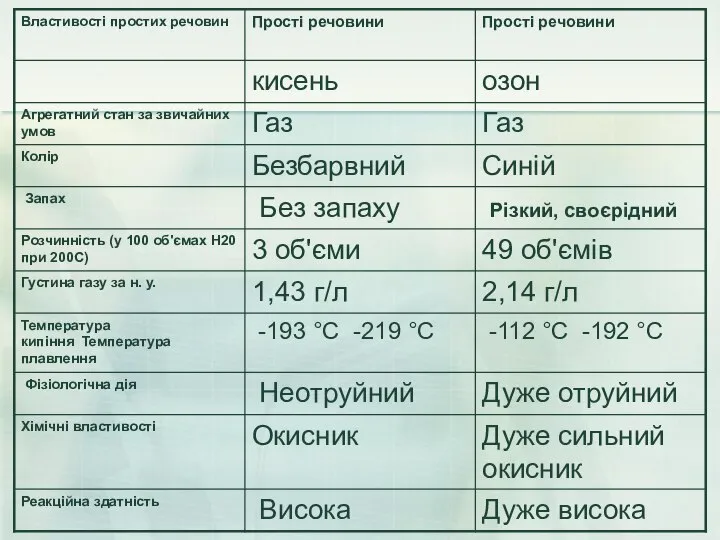
- 19. озон O3 кисень O2
- 21. Фізичні властивості. Озон – газ синього кольору із своєрідним різким запахом, розчинність у воді майже в
- 22. Озон можна добути в лабораторії
- 23. Поширення в природі Озон присутній в атмосфері Землі. Біля поверхні Землі озону мало. Його концентрація у
- 24. Алотропні модифікації карбону
- 27. Дві основні різновиди вуглецю - графіт і алмаз - істотно відрізняються за властивостями. М'який графіт має
- 28. Структура алмазу типово тетраедрична; атоми вуглецю міцно з'єднані за рахунок перекриття sp3-орбіталей.
- 29. Фізичні властивості алмазу і графіту. Алмаз Прозорий, безбарвний. Не проводить електричний струм, оскільки немає вільних електронів.
- 30. Хоча в звичайних умовах алмаз нестабільний, але практично він може зберігатися невизначено довгий час. При сильному
- 31. Всі атоми вуглецю знаходяться тут у стані sp2-гібридизації Кожен з них утворює три ковалентні зв'язки з
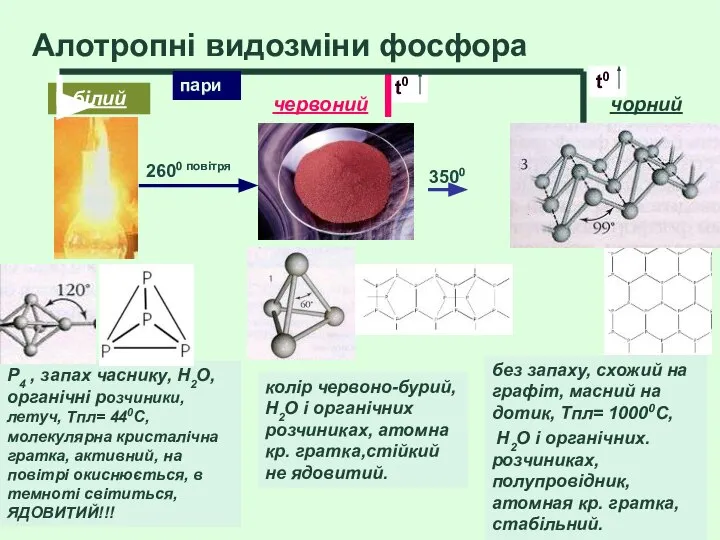
- 32. Алотропні видозміни фосфора P4 , запах часнику, H2O, органічні розчиники, летуч, Tпл= 440С, молекулярна кристалічна гратка,
- 33. Хімічний елемент Сульфур утворює дві алотропні модифікації – ромбічну і моноклінну сірку. Обидві складаються з молекул
- 34. Селе́н / Selenium (Se) Чорні, сірі і червоні алотропні модификації
- 35. Фулерени Фулерени - молекулярні з'єднання, що належать класу алотропних форм вуглецю (інші - алмаз, карбін і
- 36. Відкриття фулеренів - нової форми існування одного з найпоширеніших елементів на Землі - вуглецю, визнано одним
- 38. Скачать презентацию

































 Наличие 2 х сигналов в ЯМР 1Н (задача)
Наличие 2 х сигналов в ЯМР 1Н (задача) обобщение знаний
обобщение знаний Простой борный суперфосфат
Простой борный суперфосфат Ассортимент и качество изделий из пластмасс (урок 84)
Ассортимент и качество изделий из пластмасс (урок 84) Жесткость воды и способы ее устранения
Жесткость воды и способы ее устранения Практика по химии
Практика по химии Галогены
Галогены Жири. Жири в природі. Біологічна роль жирів. Жири. Жири в природі. Біологічна роль жирів.
Жири. Жири в природі. Біологічна роль жирів. Жири. Жири в природі. Біологічна роль жирів.  Химический состав клетки. Неорганические вещества клетки. Глава 1
Химический состав клетки. Неорганические вещества клетки. Глава 1 Физико-химические свойства белков. Электрофоретические и хроматографические методы
Физико-химические свойства белков. Электрофоретические и хроматографические методы Технология получения полиуретанов
Технология получения полиуретанов Природные (натуральные) полимеры. Композиционные материалы
Природные (натуральные) полимеры. Композиционные материалы Химические реактивы
Химические реактивы Презентация по Химии "Строение атома" - скачать смотреть бесплатно_
Презентация по Химии "Строение атома" - скачать смотреть бесплатно_ Металлы ГОУ СОШ № 661 УЧИТЕЛЬ ХИМИИ Ефремова С.А.
Металлы ГОУ СОШ № 661 УЧИТЕЛЬ ХИМИИ Ефремова С.А. Машиностроительные материалы
Машиностроительные материалы Углерод и кремний
Углерод и кремний Химическая кинетика. Лекция 2
Химическая кинетика. Лекция 2 Положение в ПСХЭ Д.И.Менделеева и строение атома
Положение в ПСХЭ Д.И.Менделеева и строение атома Рождающий воду
Рождающий воду Химические формулы. Относительные атомная и молекулярная массы. Расчетные задачи
Химические формулы. Относительные атомная и молекулярная массы. Расчетные задачи Особенности строения, реакционной способности и методы синтеза аренов
Особенности строения, реакционной способности и методы синтеза аренов Лекарственное растительное сырье, содержащее алкалоиды
Лекарственное растительное сырье, содержащее алкалоиды Хімія та обмін ліпідів
Хімія та обмін ліпідів Химические свойства металлов
Химические свойства металлов «Аспирин» Выполнила ученица 11 «Б»класса Панина Евгения
«Аспирин» Выполнила ученица 11 «Б»класса Панина Евгения  Органические галогениды. (Лекция 7)
Органические галогениды. (Лекция 7) Кристаллохимия. Тығыз шарлар теориясы
Кристаллохимия. Тығыз шарлар теориясы