Содержание
- 2. Железный век или немного из истории
- 3. Визитная карточка атома железа Задание: охарактеризуйте положение химического элемента железа в ПСХЭ Д. И. Менделеева и
- 4. Физические свойства Железо - сравнительно мягкий ,ковкий, серебристо-серый металл. Температура плавления – 1535 0С Температура кипения
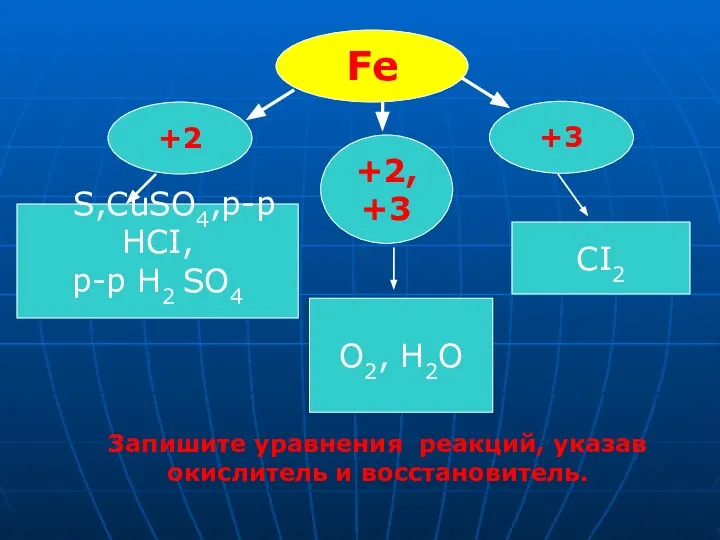
- 5. Fe +3 +2 +2, +3 O2, H2O CI2 S,CuSO4,р-р HCI, р-р H2 SO4 Запишите уравнения реакций,
- 6. Внимание! Эксперимент!
- 7. Качественные реакции на ионы Fe²⁺ и Fe³⁺ Fe³⁺ реактив – роданид калия KSCN или желтая кровяная
- 8. Биологическая роль железа Железо играет важную роль в жизнедеятельности земных организмов. Fe
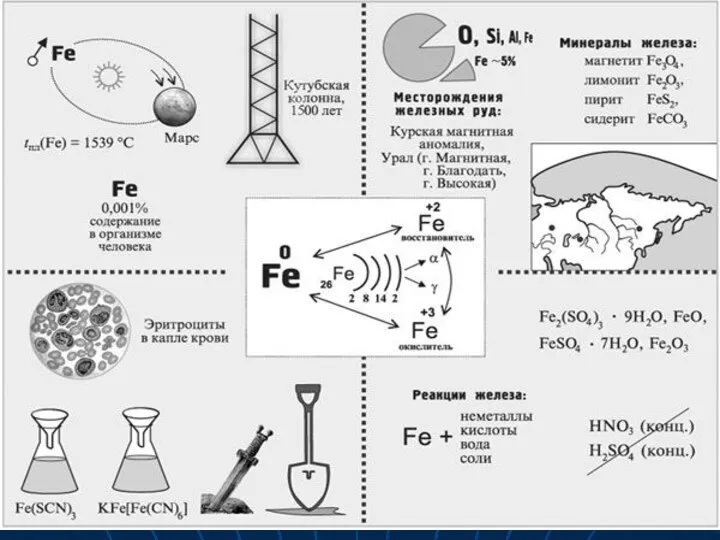
- 9. Опорный конспект «Железо»
- 10. Выберите правильные ответы, указав их номера через запятую. Вариант 1. 1. Железо – это активный щелочной
- 11. Ответы 1 вариант 2,3,4,5,7 2 вариант 1,2,5,6,7
- 13. Скачать презентацию








 Химическая связь
Химическая связь Главная подгруппа IV группы
Главная подгруппа IV группы Понятие об адсорбционной влаге
Понятие об адсорбционной влаге Химическая термодинамика. (Лекция 4)
Химическая термодинамика. (Лекция 4) Методи визначення питомої поверхні
Методи визначення питомої поверхні Анализ ЕГЭ по химии 2011
Анализ ЕГЭ по химии 2011 XXI ғасыр көшбасшысы
XXI ғасыр көшбасшысы Аминокислоты. Белки. Пептиды
Аминокислоты. Белки. Пептиды Фосфор и его соединения
Фосфор и его соединения Виконала Учениця 11-А класу Рокосівської ЗОШ Білецька Олеся
Виконала Учениця 11-А класу Рокосівської ЗОШ Білецька Олеся  Презентация Воздух, его состав и значение.
Презентация Воздух, его состав и значение.  Гетерофункціональні сполуки. Галогенозамiщенi кислоти
Гетерофункціональні сполуки. Галогенозамiщенi кислоти Каталитическое жидкофазное окисление глюкозы в глюконовую кислоту в присутствии катализаторов Pd-Sn/Al2O3
Каталитическое жидкофазное окисление глюкозы в глюконовую кислоту в присутствии катализаторов Pd-Sn/Al2O3 Средние породы
Средние породы Chemistry quiz
Chemistry quiz Физико-химические основы дезодорации растительных масел
Физико-химические основы дезодорации растительных масел Тотығып фосфорлану
Тотығып фосфорлану Хлор
Хлор Презентация Фосфор 9 класс
Презентация Фосфор 9 класс Расчетная ячейка при МД моделировании. Граничные условия. Элементарная ячейка для атомов аргона
Расчетная ячейка при МД моделировании. Граничные условия. Элементарная ячейка для атомов аргона Второй закон термодинамики
Второй закон термодинамики Наноструктурные и нанокристаллические материалы
Наноструктурные и нанокристаллические материалы Силікон Корєшкова А. В. 11-М
Силікон Корєшкова А. В. 11-М  Термодинамика поверхностных явлений. (Часть 1)
Термодинамика поверхностных явлений. (Часть 1) Бериллий: основные свойства, технологии получения, применение
Бериллий: основные свойства, технологии получения, применение Химические свойства металлов
Химические свойства металлов Коррозия металлов
Коррозия металлов Химические реакции
Химические реакции