Содержание
- 2. ПЛАН: I. ЖЕЛЕЗО КАК ХИМИЧЕСКИЙ ЭЛЕМЕНТ. II. НАХОЖДЕНИЕ В ПРИРОДЕ И ПРИМЕНЕНИЕ ЖЕЛЕЗА III. ФИЗИЧЕСКИЕ СВОЙСТВА.
- 3. I. КАК ХИМИЧЕСКИЙ ЭЛЕМЕНТ Химический элемент VIII гр. Периодической системы Д.И. Менделеева. Атомный номер 26, атомная
- 4. II. НАХОЖДЕНИЕ В ПРИРОДЕ В земной коре железо распространено достаточно широко. На его долю приходится: Около
- 5. Fe красный железняк (руда гематит Fe2O3) магнитный железняк (руда магнетит Fe2O4) бурый железняк (руда гидрогетит НFeO2·nH2O)
- 6. КРАСНЫЙ ЖЕЛЕЗНЯК (РУДА ГЕМАТИТ Fe2O3) БУРЫЙ ЖЕЛЕЗНЯК (РУДА ГИДРОГЕТИТ НFEO2 · NH2O)
- 7. ШПАТОВЫЙ ЖЕЛЕЗНЯК (РУДА СИДЕРИТ FEСO3) магнитный железняк (руда магнетит Fe2O4)
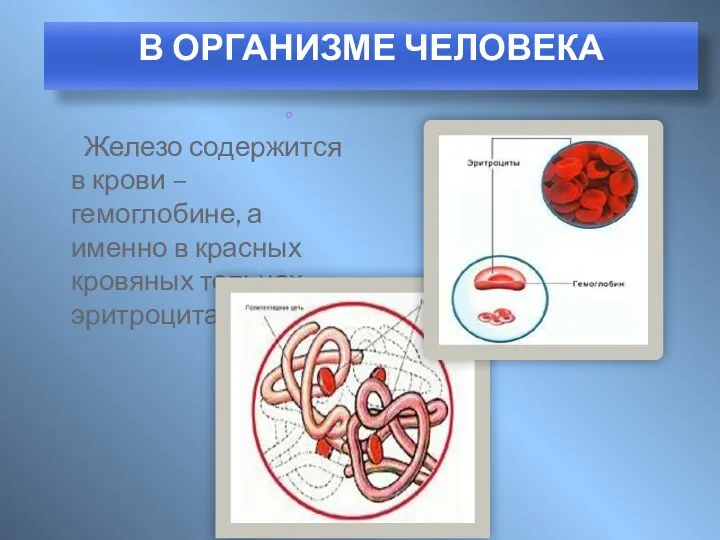
- 8. Железо содержится в крови – гемоглобине, а именно в красных кровяных тельцах – эритроцитах. о В
- 9. Железо влияет на процесс фотосинтеза. В РАСТЕНИЯХ
- 10. Из железа изготавливают различные виды транспорта В БЫТУ ЧЕЛОВЕКА
- 11. В ВОЕННОЙ ПРОМЫШЛЕННОСТИ
- 12. В истории железо известно очень давно. из него изготовляли многое. Например доспехи, латы, оружие и т.
- 13. Железо - сравнительно мягкий, ковкий, серебристо-серый металл. Температура плавления – 1535 град. Температура кипения около 2800
- 14. Железо, отдавая два внешних электрона, проявляет степень окисления +2; отдавая три электрона (два внешних и один
- 15. Железо — активный металл. На воздухе образуется защитная оксидная пленка, препятствующая ржавению металла. 3Fe + 2O2
- 16. 3. Взаимодействие с простыми веществами: 3.1 Горит в кислороде 3 Fe + 2 O2 =Fe3 O4
- 17. 4.Железо вытесняет из растворов солей металлы, находящиеся в электрохимическом ряду напряжений правее железа: Fe + CuSO4
- 18. 6. С КИСЛОТАМИ: С соляной и разбавленной (приблизительно 20%-й) серной кислотами железо реагирует с образованием солей
- 19. 7. ОКИСЛЕНИЕ ЖЕЛЕЗА При хранении водных растворов солей железа(II) наблюдается окисление железа(II) до железа(III): 4FeCl2 +
- 20. ОКСИД ЖЕЛЕЗА 1. Проявляет основные свойства, взаимодействуя с кислотами: FeO+H2SO4 = FeSO4 + H2O 2. Оксид
- 21. КАЧЕСТВЕННЫЕ РЕАКЦИИ НА ИОНЫ FE2+ И FE3+. FeSO4 + K3 [Fe(CN)6 ] = KFe +2 [Fe
- 22. Когда открыто железо никто не знает и не узнает, так как это было слишком давно. Но
- 24. Скачать презентацию




















 Химическая связь
Химическая связь Главная подгруппа IV группы
Главная подгруппа IV группы Понятие об адсорбционной влаге
Понятие об адсорбционной влаге Химическая термодинамика. (Лекция 4)
Химическая термодинамика. (Лекция 4) Методи визначення питомої поверхні
Методи визначення питомої поверхні Анализ ЕГЭ по химии 2011
Анализ ЕГЭ по химии 2011 XXI ғасыр көшбасшысы
XXI ғасыр көшбасшысы Аминокислоты. Белки. Пептиды
Аминокислоты. Белки. Пептиды Фосфор и его соединения
Фосфор и его соединения Виконала Учениця 11-А класу Рокосівської ЗОШ Білецька Олеся
Виконала Учениця 11-А класу Рокосівської ЗОШ Білецька Олеся  Презентация Воздух, его состав и значение.
Презентация Воздух, его состав и значение.  Гетерофункціональні сполуки. Галогенозамiщенi кислоти
Гетерофункціональні сполуки. Галогенозамiщенi кислоти Каталитическое жидкофазное окисление глюкозы в глюконовую кислоту в присутствии катализаторов Pd-Sn/Al2O3
Каталитическое жидкофазное окисление глюкозы в глюконовую кислоту в присутствии катализаторов Pd-Sn/Al2O3 Средние породы
Средние породы Chemistry quiz
Chemistry quiz Физико-химические основы дезодорации растительных масел
Физико-химические основы дезодорации растительных масел Тотығып фосфорлану
Тотығып фосфорлану Хлор
Хлор Презентация Фосфор 9 класс
Презентация Фосфор 9 класс Расчетная ячейка при МД моделировании. Граничные условия. Элементарная ячейка для атомов аргона
Расчетная ячейка при МД моделировании. Граничные условия. Элементарная ячейка для атомов аргона Второй закон термодинамики
Второй закон термодинамики Наноструктурные и нанокристаллические материалы
Наноструктурные и нанокристаллические материалы Силікон Корєшкова А. В. 11-М
Силікон Корєшкова А. В. 11-М  Термодинамика поверхностных явлений. (Часть 1)
Термодинамика поверхностных явлений. (Часть 1) Бериллий: основные свойства, технологии получения, применение
Бериллий: основные свойства, технологии получения, применение Химические свойства металлов
Химические свойства металлов Коррозия металлов
Коррозия металлов Химические реакции
Химические реакции