Содержание
- 3. Работа мозга
- 5. Что такое медиаторы? Это вещества которые регулируют работу нашего мозга, формируют наши эмоции и наше сознание.
- 9. Что такое наркотики?
- 11. Нейрохимические механизмы действия наркотиков - Синтез нейромедиатора. Наркотик увеличивает или уменьшает количество вырабатываемых нейромедиаторов Транспортировка нейромедиатора.
- 12. -Выделение нейромедиатора. Наркотик вызывает преждевременное выделение молекул нейромедиатора в синапс. -Распад нейромедиатора. Наркотик влияет на распад
- 13. Главные медиаторы ЦНС: Глютаминовая кислота и ГАМК.
- 20. Агонисты Дофамина \адреналина – кокаин, экстази,амфетамин.
- 36. Генетические факторы, влияющие на восприимчивость к алкоголю и наркотическим веществам. Анализ наличия полиморфизмов в генах DAT,
- 37. Рецепторы, взаимодействующие с эндогенными нейромедиаторами Эндогенные неромедиаторы – биологически активные химические вещества, посредством которых осуществляется передача
- 38. Эндорфины образуются из вырабатываемого гипофизом вещества — беталипотрофина (beta-lipotrophin); считается, что они контролируют деятельность эндокринных желез
- 40. Скачать презентацию
Работа мозга
Работа мозга
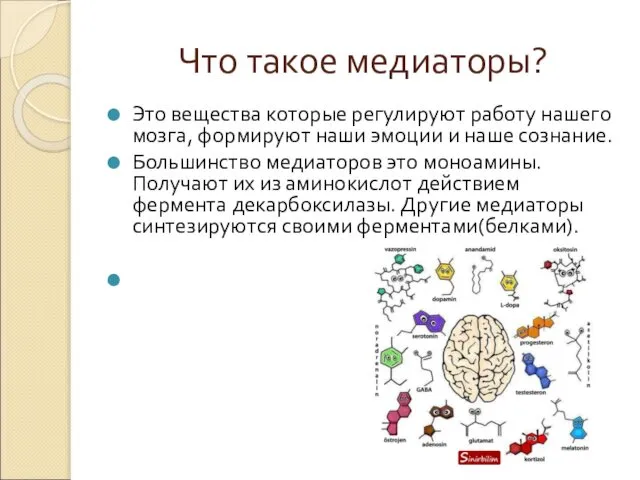
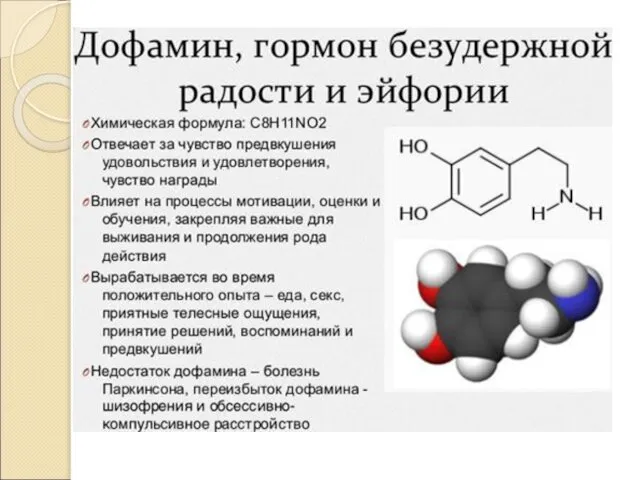
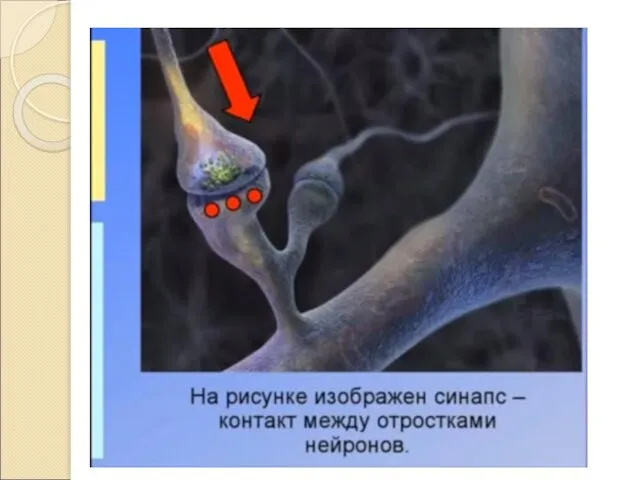
Что такое медиаторы?
Это вещества которые регулируют работу нашего мозга, формируют наши
Что такое медиаторы?
Это вещества которые регулируют работу нашего мозга, формируют наши
Большинство медиаторов это моноамины. Получают их из аминокислот действием фермента декарбоксилазы. Другие медиаторы синтезируются своими ферментами(белками).
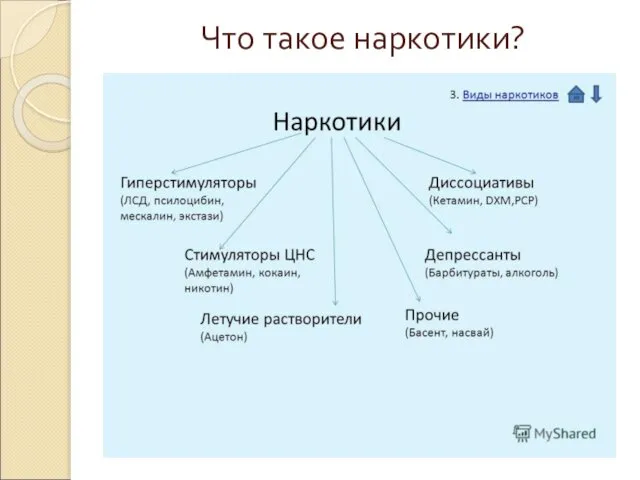
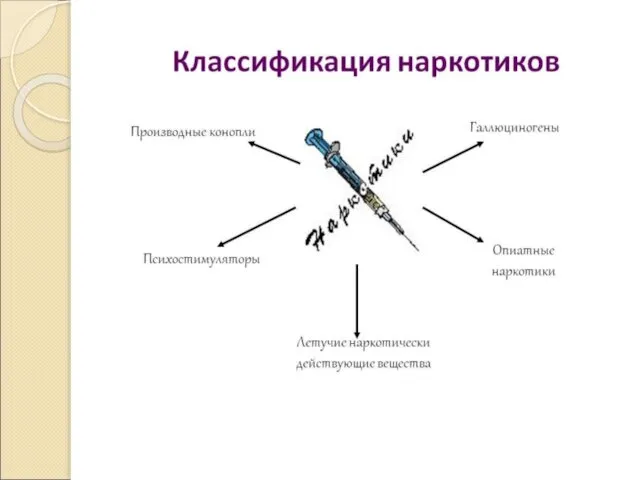
Что такое наркотики?
Что такое наркотики?
Нейрохимические механизмы действия наркотиков
- Синтез нейромедиатора. Наркотик увеличивает или уменьшает количество
Нейрохимические механизмы действия наркотиков
- Синтез нейромедиатора. Наркотик увеличивает или уменьшает количество
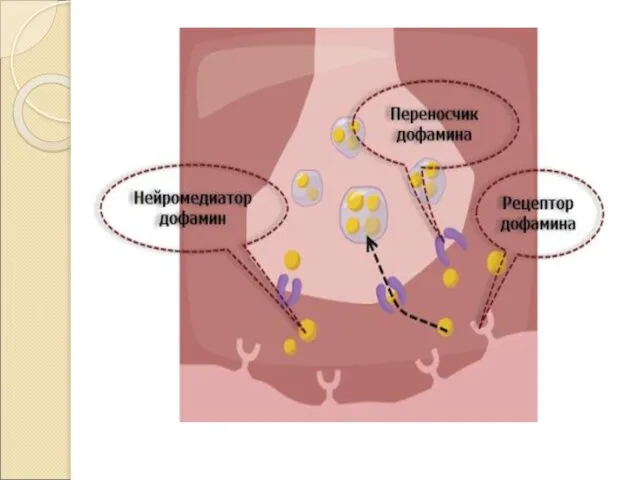
Транспортировка нейромедиатора. Наркотик вмешивается в процесс доставки молекул нейромедиатора к нервным окончаниям.
Накопление нейромедиатора. Наркотик вмешивается в процесс накопления нейромедиатора в пузырьках нервных окончаний
-Выделение нейромедиатора. Наркотик вызывает преждевременное выделение молекул нейромедиатора в синапс.
-Распад
-Выделение нейромедиатора. Наркотик вызывает преждевременное выделение молекул нейромедиатора в синапс.
-Распад
-Обратное поглощение нейромедиатора. Наркотик блокирует обратное поглощение нейромедиатора в нервные окончания.
- Активизация рецептора. Наркотик активизирует рецептор благодаря мимикрии.
-Блокировка рецептора. Наркотик делает рецептор инертным, блокируя его.
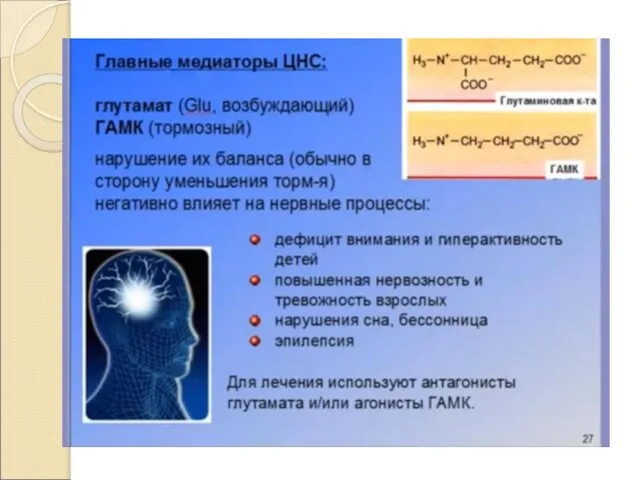
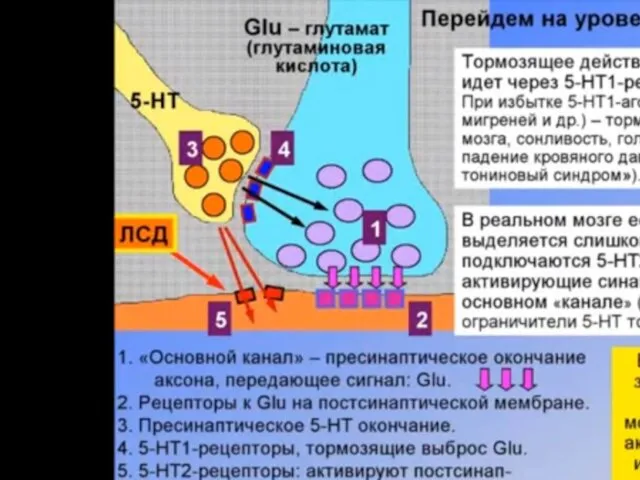
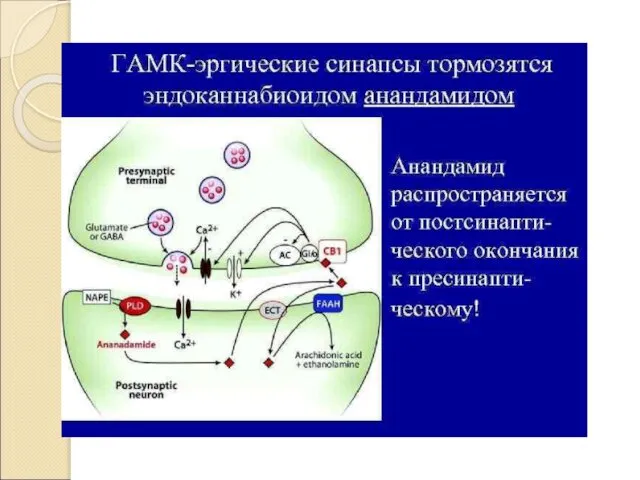
Главные медиаторы ЦНС: Глютаминовая кислота и ГАМК.
Главные медиаторы ЦНС: Глютаминовая кислота и ГАМК.
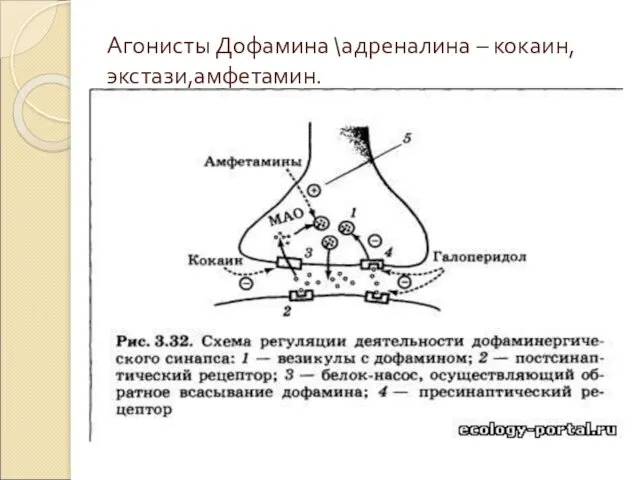
Агонисты Дофамина \адреналина – кокаин, экстази,амфетамин.
Агонисты Дофамина \адреналина – кокаин, экстази,амфетамин.
Генетические факторы, влияющие на восприимчивость к алкоголю и наркотическим веществам.
Анализ наличия
Генетические факторы, влияющие на восприимчивость к алкоголю и наркотическим веществам.
Анализ наличия
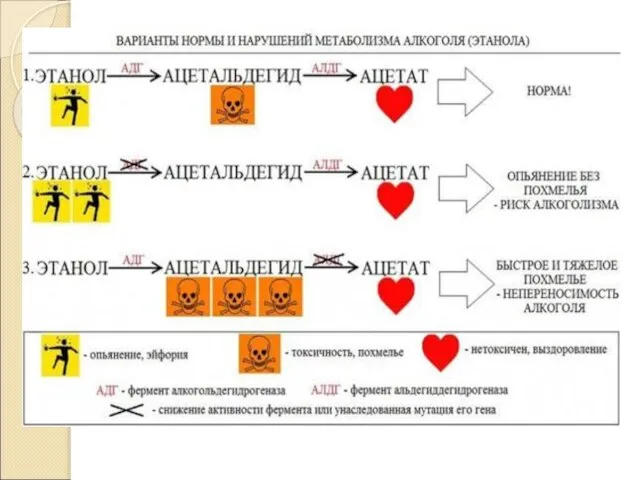
Ферменты участвующие в метаболизме алкоголя
Ключевыми ферментами, участвующими в метаболизме этанола являются алкольдегидрогеназа и альдегиддегидрогеназа. На первом этапе метаболизма алкогольдегидрогеназа превращает этанол в ацетальдегид, а далее ацетальдегид при помощи фермента альдегиддегидрогеназы до нетоксичных продуктов ацетата, СО2 и воды. Описано, что в различных популяциях существуют разные изоформы этих ферментов: активная и неактивная. Активность фермента алкогольдегидрогеназы определяется аминокислотой в 48 положении белка, гистидин в этом положении характерен для активной формы (ADH1B*2), а аргинин для малоактивной (ADH1B*1). Активность альдегиддегидрогеназы определяется аминокислотой в положении 504: глютамин – активная форма (ALDH2*1), лизин – неактивная (ALDH2*2). Наличие в генотипе человека аллеля, кодирующего активную форму алкогольдегидрогеназы (p.48His, c.143A, ADH1B*2) и/или неактивную форму альдегиддегидрогеназы (р.504Lys, c.1510A, ALDH2*2) приводит к повышению концентраций альдегида, вызывающего ряд таких неприятных симптомов, как тошнота, головокружение, гиперемия кожных покровов лица, субъективно оцениваемые «неприятные ощущения» в теле и т. д., что приводит к более редкому употреблению алкоголя и употреблению его в меньших количествах. Таким образом, наличие в генотипе аллелей c.143A гена ADH2 и c.1510A гена ALDH2 может рассматриваться как протективный фактор, однако не может являться препятствием для развития алкогольной зависимости.
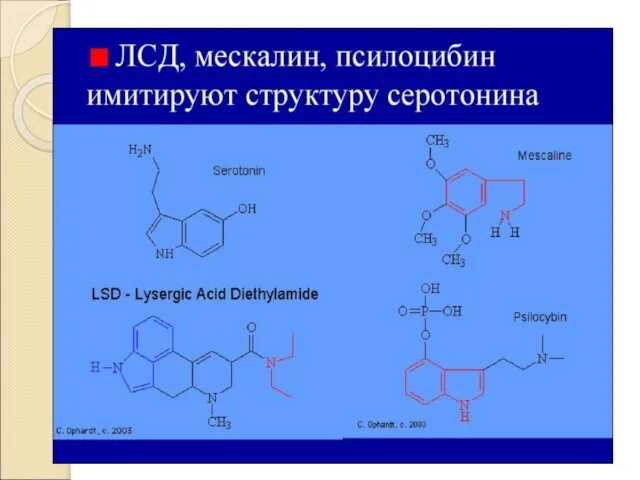
Рецепторы, взаимодействующие с эндогенными нейромедиаторами
Эндогенные неромедиаторы – биологически активные химические вещества,
Рецепторы, взаимодействующие с эндогенными нейромедиаторами
Эндогенные неромедиаторы – биологически активные химические вещества,
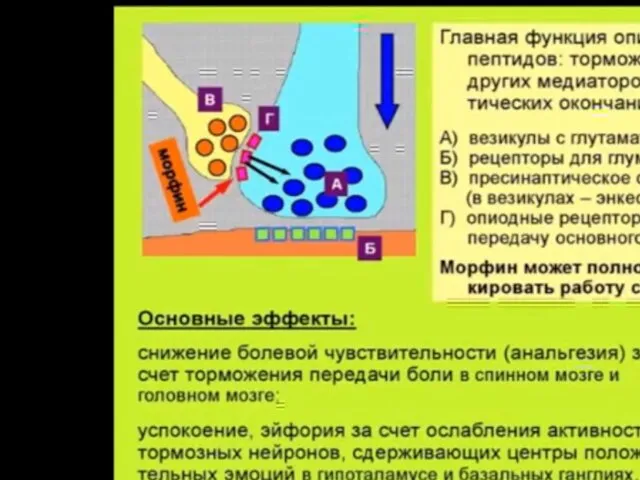
Эндорфины образуются из вырабатываемого гипофизом вещества — беталипотрофина (beta-lipotrophin); считается, что
Эндорфины образуются из вырабатываемого гипофизом вещества — беталипотрофина (beta-lipotrophin); считается, что
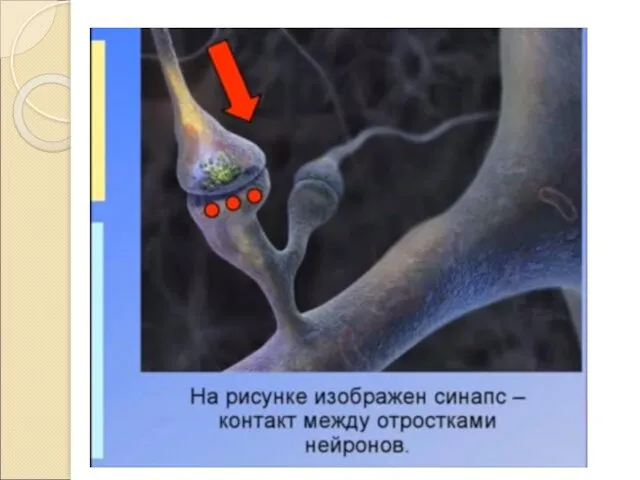



















 Infográficos de Gatilhos de Asma
Infográficos de Gatilhos de Asma Правила биоэтики: правило конфиденциальности (врачебная тайна). Правило информированного согласия. Этические комитеты
Правила биоэтики: правило конфиденциальности (врачебная тайна). Правило информированного согласия. Этические комитеты Введение в спланхнологию. Закономерности развития и строения пищеварительной системы. Особенности у детей
Введение в спланхнологию. Закономерности развития и строения пищеварительной системы. Особенности у детей Как устроена обида
Как устроена обида Psychological contract
Psychological contract СПИД и его профилактика
СПИД и его профилактика Цереброваскулярные болезни. Ревматизм. Приобретенные пороки сердца
Цереброваскулярные болезни. Ревматизм. Приобретенные пороки сердца Внутрибольничные инфекции. Тема 10
Внутрибольничные инфекции. Тема 10 Умножение обыкновенных дробей
Умножение обыкновенных дробей Особенности эмоционально-волевой и личностной сфер при нарушениях слуха
Особенности эмоционально-волевой и личностной сфер при нарушениях слуха Десмургия - раздел хирургии, изучающий виды повязок
Десмургия - раздел хирургии, изучающий виды повязок Асептика. Источники хирургической инфекции
Асептика. Источники хирургической инфекции Рак мочевого пузыря. Эпидемиология. Классификация. Этиология. Патогенез. Клиническая картина
Рак мочевого пузыря. Эпидемиология. Классификация. Этиология. Патогенез. Клиническая картина Болезни сердца
Болезни сердца Еда и мозг на практике Перлмуттер. Врач невролог (1)
Еда и мозг на практике Перлмуттер. Врач невролог (1) Белок и его роль в сбалансированном питании
Белок и его роль в сбалансированном питании Вирусный гепатит С. Диагностика и лечение
Вирусный гепатит С. Диагностика и лечение Адамның репродуктивті қызметінің жастық ерекшеліктері
Адамның репродуктивті қызметінің жастық ерекшеліктері Хронический эндометрит в структуре женского бесплодия
Хронический эндометрит в структуре женского бесплодия Изменение физических свойств при почечной патологии
Изменение физических свойств при почечной патологии Вакцинация
Вакцинация Синкопальные состояния
Синкопальные состояния Электрокардиограмма при нарушениях ритма сердца
Электрокардиограмма при нарушениях ритма сердца Детский травматизм. Что нужно знать о травме!
Детский травматизм. Что нужно знать о травме! Дифференциальная диагностика ОРВИ
Дифференциальная диагностика ОРВИ Содержательная теория мотивации. Теория мотивации Дэвида МакКлелланда
Содержательная теория мотивации. Теория мотивации Дэвида МакКлелланда Артериальная гипертензия
Артериальная гипертензия Современные подходы к оценке больного с хронической обструктивной болезнью легких
Современные подходы к оценке больного с хронической обструктивной болезнью легких