Содержание
- 2. Лабораторные занятия по иммунологии для факультета ветеринарной медицины
- 3. Дисциплина: Иммунология
- 4. ИММУНОЛОГИЧЕСКИЕ МЕТОДЫ ИССЛЕДОВАНИЯ В ВЕТЕРИНАРИИ В настоящее время иммунология эмбриогенеза выделилась в отдельную отрасль науки -
- 5. СОВРЕМЕННЫЕ ПРЕДСТАВЛЕНИЯ ОБ ИММУННОЙ СИСТЕМЕ Под термином иммунитет понимается способ защиты организма от живых тел и
- 6. Способность организма развивать высокоспецифическую ответную реакцию на чужеродные молекулы называется иммунологической реактивностью. Иммунологическая реактивность проявляется иммунным
- 7. В иммунной системе различают центральные органы (вилочковая железа, сумка Фабрициуса у птиц, пейеровы бляшки, костный мозг)
- 8. В- компонент иммунитета не зависит от тимуса и осуществляет гуморальный иммунный ответ. В- лимфоцит после взаимодействия
- 9. Т- помощники (helper) - включают В- лимфоцит в пролиферацию и дифференцировку, обеспечивают накопление соответствующего клона зрелых
- 10. Иммуноглобулин А (Ig A) – встречается в моно-, ди– и полимерной форме в сыворотке крови, секреторных
- 11. В- супрессоры – (относятся к пре В- клеткам,) тормозят синтез ДНК и пролиферацию предшественников антителопродуцентов, регулируют
- 12. NK- клетки (Natural killer cells) - естественные клетки киллеры. Они осуществляют независимый от антител и комплемента
- 13. Для иммунологического распознавания и взаимодействия клеток в иммунном ответе важное значение имеют антигены, контролируемые главной генетической
- 14. 1.КОМПЛЕКС ТЕСТОВ 1 УРОВНЯ Выявление как первичных, так и вторичных иммунодефицитных состояний (ИДС) среди животных имеет
- 15. 1.2. Морфологическая картина крови 1.2.1. Подсчет лейкоцитов В пробирки Флоринского или в лунки полистироловых пластин разливают
- 16. 1.2.2. Определение лейкограммы Готовят мазок и окрашивают по Романовскому-Гимзе. Готовую краску предварительно разводят дистиллированной водой из
- 18. 1.3. ОПРЕДЕЛЕНИЕ ДИФФЕРЕНЦИРОВКИ Т-, В -, NK-ЛИМФОЦИТОВ В МАЗКАХ КРОВИ И БИОЛОГИЧЕСКИХ ЖИДКОСТЯХ ЖИВОТНЫХ ( по
- 19. Первичная реакция (реакция ферментативного расщепления) - гидролиза нафтилацетата с участием фермента эстеразы: ОСОН3 Фермент + Н2О
- 20. Вторичная реакция (реакция сочетания) т.е. взаимодействия α- нафтола с нейтральным прочным синим В:
- 21. Взятие крови, приготовление и фиксация мазков Кровь для исследования берут у сельскохозяйственных животных из яремной вены,
- 22. Приготовление буферных растворов В состав буферной смеси входят: раствор А и Б в соотношении 1:20. Приготовление
- 23. Приготовление инкубационной смеси Правильное приготовление инкубационной смеси имеет немаловажное значение для дальнейшей окраски мазков. Готовят раствор
- 24. Инкубация мазков Инкубацию мазков проводят в темной комнате в течение 2-х часов. На фиксированные формалином мазки
- 25. 1.4. Постановка реакций розеткообразования 1.4.1. Выделение лейкоцитарной взвеси для постановки реакции розеткообразования Для этого проводят лизис
- 26. 1.4.2. Постановка реакции розеткообразования для определения Т-лимфоцитов - Е-розеткообразование. (Р. В. Петров и соавт., 1992 г.)
- 27. Учет результатов: Т- лимфоциты хорошо просматриваются в обычном световом микроскопе при увеличении 7×90. Подсчитывают 100 -
- 28. 1.5. Постановка реакции розеткообразования для определения В - лимфоцитов Для определения В- лимфоцитов с помощью розеткообразования
- 29. 1.5.1. Определение В-лимфоцитов с помощью ЕАС - розеткообразования (Гущин И.С. и соавторы 1981 г.) Для определения
- 30. 1.5.3. Приготовление комплемента В пробирку смоченную физиологическим раствором вносят 0,5 - 0,8 мл крови мыши и
- 31. 1.5.5. Приготовление фиксированной ЕАС- системы Для этого к 1,6 мл 2,5 % взвеси фиксированных эритроцитов быка
- 32. 1.5.6. Постановка реакции ЕАС - розеткообразования В лунку планшета помещают 50 мкл лейкоцитов выделенных при помощи
- 34. 1.6. Постановка реакций розеткообразования для определения субпопуляций нейтрофильных гранулоцитов Подобно другим клеткам участвующими в иммунном ответе
- 35. 1.6.1. Метод определения р.Е - РОН ( Нестерова И.В., Колесникова Н.В., Чудилова Г.А. 1996г.) В лунку
- 37. 1.6.2. Метод определение поздних Е-РОН (Нестерова И.В., Колесникова Н.В., Чудилова Г.А. 1996г.) В лунку круглодонного планшета
- 39. 1.6.3. Определения ЕАС - РОН (Нестерова И.В., Колесникова Н.В., Чудилова Г.А. 1991г.) В лунку круглодонного планшета
- 40. Учет результатов: при увеличении (7×90) ЕАС - РОН - подсчитывают в обычном световом микроскопе, на 100-200
- 41. 1.7.Постановка нагрузочных тестов in vitro Постановка нагрузочных тестов in vitro целесообразна в тех случаях, когда проводится
- 42. 1.8. Определение циркулирующих иммунных комплексов (ЦИК) Метод основан на изменении величины светового рассеивания раствора полиэтиленгликоля вследствие
- 43. Постановка реакции В 0,3 мл сыворотки крови добавляют 0,6 мл 0,1 М боратного буфера. Берут 2
- 44. 1.9. Определение содержания иммуноглобулинов (Ig A, Ig M, Ig G) в сыворотке крови (Манчини и соавт.,
- 45. Приготовление реактивов Веронал-мединаловый буфер (рН = 8,6) имеет следующий состав: 4,38 г мединала и 0,69 г
- 46. Постановка реакции Перед работой 1,5 % раствор агара подогревают на водяной бане до 50-60 °С. Затем
- 47. Уровень иммуноглобулинов определяют по формуле: Расчет концентрации искомой сыворотки: а) определение коэффициента наклона (КН) стандартной сыворотки
- 48. 1.10. Реакция бактериального фагоцитоза нейтрофилов с определением степени завершенности (Нестерова И.В., Колесникова Н.В., Чудилова Г.А. 1989
- 49. Кислородзависимые механизмы Происходит резкая активация гексозомонофосфатного шунта, генерирующего НАДФ-Н, который используется для восстановления молекулярного кислорода, связанного
- 50. Кислороднезависимые механизмы При реализации этого процесса происходят дисмутации надпероксидазы, потребляются ионы водорода и слегка повышается рН,
- 51. Получение проб крови, молока, молозива и маточной слизи или лохий проводят по описанной выше методике. Для
- 52. Оценка поглотительной способности и переваривающей функции фагоцитов Для оценки поглотительной функции фагоцитов: в мазке подсчитывается 100
- 53. Для оценки поглотительной функции фагоцитов: в мазке подсчитывается 100 нейтрофилов, в каждом из них определяется: -
- 54. Фагоцитарный интегральный индекс (ФИИ) , где Ф - 100 посчитанных нейтрофилов. Завершенность фагоцитарного акта оценивают по
- 55. Интегральный показатель переваривающей активности (ИППА) - позволяет оценить фагоцитарную активность нейтрофилов в абсолютных значениях
- 56. 1.11. Определение лизоцимной активности в сыворотке крови (Стогник В.И., Голик В.П., 1989 г.) Лизоцим является одним
- 57. Расчет лизоцимной активности производят по формуле: где ЛА - лизоцимная активность сыворотки крови в (%) До
- 58. 1.12. Определение бактерицидной активности в сыворотке крови - БАСК (О.В Смирнов., Т.А Кузьмина. 1989 г.) Метод
- 59. 1.12.1. Метод определения бактерицидной активности в сыворотке крови На физиологическом растворе готовят смесь из суточной культуры
- 60. Бактерицидную активность сыворотки крови вычисляют по следующей формуле: где БАСК- бактерицидная активность в (%) До- оптическая
- 61. ОПРЕДЕЛЕНИЕ Т-, В-, NK-ЛИМФОЦИТОВ В МАЗКАХ КРОВИ ЖИВОТНЫХ (по Пирсу,1962 г., в модификации Гугушвили Н. Н.,
- 62. Приготовление буферных растворов В состав буферной смеси входят: раствор А и Б в соотношении 1:20. Приготовление
- 63. Инкубация мазков Инкубацию мазков проводят в темной комнате в течение 2-х часов. На фиксированные формалином мазки
- 64. Реакция бактериального фагоцитоза нейтрофилов с определением степени завершенности (НЕСТЕРОВА И.В., КОЛЕСНИКОВА Н.В., ЧУДИЛОВА Г.А. 1989 Г.)
- 65. Кислородзависимые механизмы. Происходит резкая активация гексозомонофосфатного шунта, генерирующего НАДФ-Н, который используется для восстановления молекулярного кислорода, связанного
- 66. Получение проб крови, молока, молозива и маточной слизи или лохий проводят по описанной выше методике. Для
- 67. Оценка поглотительной способности и переваривающей функции фагоцитов Для оценки поглотительной функции фагоцитов: в мазке подсчитывается 100
- 68. Фагоцитарный интегральный индекс (ФИИ) где Ф - 100 посчитанных нейтрофилов. Завершенность фагоцитарного акта оценивают по показателям:
- 69. Индекс переваривания (ИП) – среднее число убитых микробов на 1 подсчитанный нейтрофил (ф), т.е. на 100
- 70. ОПРЕДЕЛЕНИЕ АКТИВНОСТИ МИЕЛОПЕРОКСИДАЗЫ (по Sato, 1928г., в модификации Гугушвили Н.Н., 2000г.) Активность миелопероксидазы присуща молодым клеткам.
- 71. Для обнаружения миелопероксидазы применяют метод бензидиновой реакции, основанный на окислении бензидина пероксид-пероксидазной системой до нестабильного бензидинового
- 72. Фиксация мазков На приготовленные высушенные мазки крови наливают 96 об.%о этиловый спирт и фиксируют в течение
- 73. Инкубация мазков После фиксации мазки хорошо промывают в дистиллированной воде и сушат на воздухе. Инкубацию проводят
- 74. ОПРЕДЕЛЕНИЕ АКТИВНОСТИ ЩЕЛОЧНОЙ ФОСФАТАЗЫ В МАЗКАХ КРОВИ ЖИВОТНЫХ (по Шубичу М.Г., 1965г., в модификации Гугушвили Н.Н.,
- 75. Фиксация мазков Мазки крови сушат на воздухе и фиксируют в парах 40 % формалина в течение
- 76. Инкубация мазков На фиксированные формалином мазки наносят равномерным слоем инкубационную смесь. Необходимо строго соблюдать температурный режим
- 77. ОПРЕДЕЛЕНИЕ АКТИВНОСТИ КИСЛОЙ ФОСФАТАЗЫ В МАЗКАХ КРОВИ И В БИОЛОГИЧЕСКИХ ЖИДКОСТЯХ (по Шубичу М.Г.., 1980г., в
- 78. Фиксация мазков Мазки готовят сразу после взятия крови и сушат на воздухе, затем фиксируют в парах
- 79. Инкубация мазков На фиксированные формалином мазки наносится равномерным слоем инкубационная смесь. Периодически необходимо добавлять смесь, так
- 80. ЛИЗОСОМАЛЬНО-КАТИОННЫЙ ТЕСТ ПО В. М. Пигаревскому (1979г.) Принцип метода основан на цитохимическом выявлении лизосомально- катионных белков,
- 81. Приготовление буферного раствора и инкубационной смеси В состав буферной смеси входят: 0,1М раствор триса, раствор –
- 82. Микроскопия мазков Микроскопию проводят при увеличении (90×15) с использованием иммерсионной системы. Лизосомально-катионные белки окрашены в бирюзовый,
- 83. СПОНТАННЫЙ И СТИМУЛИРОВАННЫЙ NBT-ТЕСТ (Нестерова И.В., Колесникова Н.В., Чудилова Г.А., 1980г.) Принцип метода основан на цитохимическом
- 84. Кровь берут из вены и стабилизируют 2,7%-ным раствором ЭДТА в соотношении 10:1(10 частей крови и 1
- 85. Результаты реакции: формазан-позитивные гранулы окрашиваются в синий цвет, ядра - в красный. Подсчитывается процент формазан-позитивных нейтрофилов
- 86. Определение NBT –теста нами разработано, также в молоке, в молозиве, в маточной слизи или лохиях после
- 88. Скачать презентацию
Лабораторные занятия
по иммунологии
для факультета
ветеринарной медицины
Лабораторные занятия
по иммунологии
для факультета
ветеринарной медицины
Дисциплина:
Иммунология
Дисциплина:
Иммунология
ИММУНОЛОГИЧЕСКИЕ МЕТОДЫ ИССЛЕДОВАНИЯ В ВЕТЕРИНАРИИ
В настоящее время иммунология эмбриогенеза выделилась
ИММУНОЛОГИЧЕСКИЕ МЕТОДЫ ИССЛЕДОВАНИЯ В ВЕТЕРИНАРИИ
В настоящее время иммунология эмбриогенеза выделилась
СОВРЕМЕННЫЕ ПРЕДСТАВЛЕНИЯ ОБ ИММУННОЙ СИСТЕМЕ
Под термином иммунитет понимается способ защиты организма
СОВРЕМЕННЫЕ ПРЕДСТАВЛЕНИЯ ОБ ИММУННОЙ СИСТЕМЕ
Под термином иммунитет понимается способ защиты организма
Способность организма развивать высокоспецифическую ответную реакцию на чужеродные молекулы называется
Способность организма развивать высокоспецифическую ответную реакцию на чужеродные молекулы называется
В иммунной системе различают центральные органы (вилочковая железа, сумка Фабрициуса у
В иммунной системе различают центральные органы (вилочковая железа, сумка Фабрициуса у
Иммунная система организма животных и человека состоит из трех самостоятельно развивающихся, но совместно функционирующих клеточных компонентов – Т- лимфоцитов,
В- лимфоцитов и макрофагов. Т- клеточный компонент иммунитета в своем развитии и функционировании зависит от тимуса и носит название тимусзависимого. Тимусзависимая система реализует иммунный ответ клеточного типа с накоплением клеток эффекторов и ответственна за развитие реакций гиперчувствительности замедленного типа, трансплантационного и противоопухолевого иммунитета, других реакций, в которых эффектором выступает сенсибилизированный Т- лимфоцит- киллер.
В- компонент иммунитета не зависит от тимуса и осуществляет гуморальный иммунный
В- компонент иммунитета не зависит от тимуса и осуществляет гуморальный иммунный
Достижения иммунологии последних десятилетий позволили выделить среди лимфоцитов их субпопуляции. Среди Т- лимфоцитов различают: Т- эффекторы (killer) - осуществляют клеточные формы иммунного ответа реакцию гиперчувствительности замедленного типа, отторжение трансплантанта, специфический лизис клеток мишеней, противоопухолевый и противовирусный иммунитет и некоторые другие феномены.
Т- помощники (helper) - включают В- лимфоцит в пролиферацию и дифференцировку,
Т- помощники (helper) - включают В- лимфоцит в пролиферацию и дифференцировку,
Т- супрессоры (suppressor) - тормозят включение В- лимфоцитов в пролифе-рацию и дифференцировку, ингибируют выработку антител и развитие реакций гипер-чувствительности замедленного типа, определяют феномен иммунологической толерантности.
Т- усилители (amplifier) - разновидность Т- хелперов - усиливают функцию
Т- эффекторов, Т- супрессоров и других клеток.
Т- дифференцирующиеся лимфоциты, взаимодействуют с кроветворными стволовыми клетками и оказывают влияние на их миграцию, пролиферацию и дифференцировку.
Среди В- лимфоцитов выделяют предшественники иммунопродуцентов иммуноглобулинов различных классов -А, М, G.
Иммуноглобулин А (Ig A) – встречается в моно-, ди– и полимерной
Иммуноглобулин А (Ig A) – встречается в моно-, ди– и полимерной
Иммуноглобулин G (Ig G) - единственный из иммуноглобулинов, который проходит через плаценту и обеспечивает защиту от инфекционных болезней в первые недели жизни. В основном образуется при повторной иммунизации.
Иммуноглобулин M (Ig M) располагается по поверхности клетки и выполняет функцию рецептора. Низкоактивные, появляются первыми после антигенного раздражения.
В- супрессоры – (относятся к пре В- клеткам,) тормозят синтез ДНК
В- супрессоры – (относятся к пре В- клеткам,) тормозят синтез ДНК
Нулевые клетки - лимфоциты, не несущие отличительных маркеров Т- или В- лимфоцитов или имеющие очень низкую плотность соответствующих структур на своей поверхности. Они способны осуществлять антителозависимый, не требующий присутствия комплемента, лизис клеток-мишеней, т.е. разрушение аутологичных, аллогенных или ксеногенных клеток в присутствии специфичных антител.
L- и К- лимфоциты - разновидности нулевых лимфоцитов, также способны осуществлять антителозависимый не требующий присутствия комплемента лизис клеток-мишеней.
NK- клетки (Natural killer cells) - естественные клетки киллеры. Они осуществляют
NK- клетки (Natural killer cells) - естественные клетки киллеры. Они осуществляют
Т- лимфоцит после взаимодействия с макрофагом включает В- лимфоцит в антителогенез. Т- хелперы и Т- супрессоры выступают в качестве главных регуляторов иммунной системы на клеточном уровне. Три типа зрелых Т- лимфоцитов, три типа зрелых В- лимфоцитов и макрофаги - основные клеточные партнеры, осуществляющие всю гамму высокоспецифических ответных реакций организма животных.
Для иммунологического распознавания и взаимодействия клеток в иммунном ответе важное значение
Для иммунологического распознавания и взаимодействия клеток в иммунном ответе важное значение
Регуляция иммунного ответа осуществляется на трех уровнях: (внутриклеточный, клеточный, органный уровень). Внутриклеточный уровень регуляции опосредован генной информацией, заложенной в ДНК каждой клетки, которая представлена генами главного комплекса гистосовместимости и генетическим аппаратом кодирования синтеза молекул иммуноглобулинов и рецепторных структур лимфоцитов. Клеточный уровень регуляции иммунного ответа обусловлен гетерогенностью лимфоидных клеток, присутствием в их популяции киллерных, хелперных и супрессорных субъединиц. Наличие в иммунной системе центральных и периферических органов свидетельствует о том, что имеется регуляция иммунного ответа и на органном уровне.
1.КОМПЛЕКС ТЕСТОВ 1 УРОВНЯ
Выявление как первичных, так и вторичных иммунодефицитных состояний
1.КОМПЛЕКС ТЕСТОВ 1 УРОВНЯ
Выявление как первичных, так и вторичных иммунодефицитных состояний
Оценку иммунного статуса организма животных можно осуществить с помощью тестов I и II уровня. По тестам I уровня (общее число лейкоцитов, фагоцитоз, уровень Т- и В- лимфоцитов, сывороточные иммуноглобулины классов -А, М, G) можно выявить “грубые” поломки и дефекты в иммунитете.
1.1. Взятие крови из ярёмной вены в объеме 10-15 мл. Кровь в объеме 5 мл переносят в центрифужную пробирку, добавляют 2,7 % ЭДТА - (этилендиаминтетрауксусная кислота), и несколько раз встряхивают. С момента взятия до начала анализа кровь может храниться 2-3 часа при комнатной температуре.
1.2. Морфологическая картина крови
1.2.1. Подсчет лейкоцитов
В пробирки Флоринского или в лунки
1.2. Морфологическая картина крови
1.2.1. Подсчет лейкоцитов
В пробирки Флоринского или в лунки
Стеклянным капилляром набирают предварительно перемешанную кровь до метки 0,02 мл (20 мм 3). Наружную поверхность капилляра вытирают от крови и плавно выдувают содержимое на дно пробирки (лунки) с жидкостью Тюрка. Несколько раз капилляр промывают, насасывая и выдувая содержимое пробирки (лунки) и вносят в сеточную камеру Горяева при помощи глазной пипетки. Выждав 1-2 минуты, пока клетки осядут, их подсчитывают под микроскопом при увеличении 10×10 или 10×20. Клетки подсчитывают в 25 больших квадратах (разделенных на 16 малых), начиная с левого верхнего угла сетки и далее сверху вниз (итого в пяти вертикальных рядах - по пять в ряду). В каждом квадрате считают клетки, находящиеся внутри, а также лежащие на левых и нижних линиях и в левых углах квадрата.
Для подсчета содержания лейкоцитов в 1 мкл крови число подсчитанных в 25-ти квадратах клеток умножают на 200.
1.2.2. Определение лейкограммы
Готовят мазок и окрашивают по Романовскому-Гимзе. Готовую краску предварительно
1.2.2. Определение лейкограммы
Готовят мазок и окрашивают по Романовскому-Гимзе. Готовую краску предварительно
Мазки крови микроскопируют под увеличением 90х15 с использованием иммерсионной системы.
Мазок условно делят на 4 участка и, отступив от края мазка на 3-4 поля зрения, внимательно просматривают его зигзагообразно, то есть 3-5 полей - вдоль края мазка, затем 3-5 полей - под прямым углом к середине, далее 3-5 полей параллельно краю мазка и снова под прямым углом возвращаются к краю мазка. В таком порядке микроскопируют каждый из условно разделенных участков. Для подсчета лейкоцитов пользуются счетчиком, подсчитывают 100 клеток.
1.3. ОПРЕДЕЛЕНИЕ ДИФФЕРЕНЦИРОВКИ Т-, В -, NK-ЛИМФОЦИТОВ В МАЗКАХ КРОВИ И
1.3. ОПРЕДЕЛЕНИЕ ДИФФЕРЕНЦИРОВКИ Т-, В -, NK-ЛИМФОЦИТОВ В МАЗКАХ КРОВИ И
( по Пирсу, 1962 г., в модификации Гугушвили Н.Н., 2000г.)
Данная методика является экспресс методом для определения неспецифической эстеразы в клетках крови: Т-, NK- лимфоцитов. Эстеразы входят в подгруппу (3.1). Механизм их действия на бактерии заключается в их переваривании благодаря способности гидролизовать белковые субстраты. Эстераза, или эластаза разрушает пептидогликаны бактериальной стенки. Одновременно в одном препарате можно определить В - клетки по окраске ядер. Применение методики основано на взаимодействии неспецифической эстеразы с а- нафтилацетатом. Эстераза способствует гидролизу α- нафтилацетата с образованием α- нафтола и уксусной кислоты (первичная реакция), которая создает слабокислую среду. Для поддержания рН в пределах 8,0 - 8,2 в систему вводят буферную смесь, предложенную нами, состоящую из КН2РО4 и Na2HРО4, что оказывало влияние на активность фермента эстеразы (изобретение по заявке № 000344 от10.01.2000г). Затем а-нафтол взаимодействует с красителем - нейтральным прочным синим В с образованием комплексного соединения азокрасителя (вторичная реакция). Образовавшийся комплекс (азокраситель) окрашивает эстеразу содержащуюся внутри Т-, и NК- лимфоцитов.
Первичная реакция (реакция ферментативного расщепления) - гидролиза нафтилацетата с участием фермента
Первичная реакция (реакция ферментативного расщепления) - гидролиза нафтилацетата с участием фермента
ОСОН3
Фермент
+ Н2О
ОН
α- нафтол
+СН3СООН
α-нафтилацетат
Вторичная реакция (реакция сочетания) т.е. взаимодействия α- нафтола с нейтральным прочным
Вторичная реакция (реакция сочетания) т.е. взаимодействия α- нафтола с нейтральным прочным
Взятие крови, приготовление и фиксация мазков
Кровь для исследования берут у сельскохозяйственных
Взятие крови, приготовление и фиксация мазков
Кровь для исследования берут у сельскохозяйственных
Приготовление буферных растворов
В состав буферной смеси входят: раствор А и Б
Приготовление буферных растворов
В состав буферной смеси входят: раствор А и Б
Приготовление раствора А
Для приготовления раствора А берут 0,34 г КН2РО4 (однозамещенного фосфорнокислого калия) и растворяют в небольшом количестве дистиллированной воды затем в мерной колбе объемом 25 мл доводят до метки.
Приготовление раствора Б
Берут 8,9 г Na2HPO4, (двузамещенного фосфорнокислого натрия) и растворяют в небольшом количестве дистиллированной воды и в мерной колбе объемом 500 мл доводят до метки.
Для лучшей диффузии растворы А и Б оставляют на сутки в темном месте. Тщательно перемешивают 25 мл раствора А и 475 мл раствора Б, оставляют на сутки и затем измеряют рН буферного раствора. При этом необходимо получить рН от 8,0 до 8,2.
Приготовление инкубационной смеси
Правильное приготовление инкубационной смеси имеет немаловажное значение для дальнейшей
Приготовление инкубационной смеси
Правильное приготовление инкубационной смеси имеет немаловажное значение для дальнейшей
Приготовление раствора 1
2,5 мг α- нафтилацетата растворяют в 0,125 мл ацетона разбавленного таким же количеством дистиллированной воды, добавляя небольшими порциями. После растворения к нему постепенно добавляют 6,25 мл дистиллированной воды.
Приготовление раствора 2
6,25 мг нейтрального прочного синего растворяют в 6,25 мл дистиллированной воды, смешивая их постепенно. Для поддержания рН добавляют 0,125 мл буферного раствора с рН = 8,0-8,2.
Полученные растворы 1 и 2 смешивают, фильтруют в темной комнате через стеклянный фильтр.
Инкубация мазков
Инкубацию мазков проводят в темной комнате в течение 2-х часов.
Инкубация мазков
Инкубацию мазков проводят в темной комнате в течение 2-х часов.
Для дифференцировки лимфоцитов от других клеток крови в дальнейшем окрашивают ядра клеток (0,5 - 1 минуту) 0,25 % водным раствором Азуром-II, или 0,5% нейтральным красным приготовленным на физиологическом растворе. Затем краску сливают, промывают дистиллированной водой, мазки высушивают на воздухе в темной комнате.
Микроскопия мазков
Микроскопию проводят при увеличении (90×15) с использованием иммерсионной системы. При этом Т- лимфоциты содержат одну или несколько гранул темного цвета расположенных по периферии клетки, ядра хорошо выражены; в NK- клетках ядра хорошо выражены, а цитоплазма окрашена диффузно в серый цвет. В- лимфоциты имеют хорошо выраженные ядра, со слабо окрашенной цитоплазмой, клетки гранул не содержат (рис.1).
1.4. Постановка реакций розеткообразования
1.4.1. Выделение лейкоцитарной взвеси для постановки реакции розеткообразования
Для
1.4. Постановка реакций розеткообразования
1.4.1. Выделение лейкоцитарной взвеси для постановки реакции розеткообразования
Для
0,083 % NH4C1 + 0,04 г/л ЭДТА, рН 7,2 - 7,5 доводится 1 % Na2CO3
Ход исследования
К 0,5 мл крови, взятую с ЭДТА (1:9) добавляют 1 мл гемолитической жидкости и перемешивают в течение 30 сек., быстро добавляют 2-5 мл забуференного физиологичекого раствора (ЗФР), для предотвращения разрушения лейкоцитов. Затем центрифугируют в течение 10 минут при 1500 об/мин. Из центрифугата надосадочную жидкость удаляют, и к осадку добавляют 1-2 мл гемолитической жидкости, встряхивают пробирку в течение 3 - 5 сек. Затем добавляют 10 мл ЗФР и центрифугируют 10 минут при 1500 об/мин. Надосадочную жидкость удаляют, к осадку лейковзвеси добавляют 0,4-0,5 мл ЗФР и ресуспендируют. Готовят рабочую концетрацию лейковзвеси с добавлением ЗФР до 2 - 4 - 106 мл. Количество клеток подсчитывают в сеточной камере Горяева.
1.4.2. Постановка реакции розеткообразования для определения Т-лимфоцитов - Е-розеткообразование. (Р. В.
1.4.2. Постановка реакции розеткообразования для определения Т-лимфоцитов - Е-розеткообразование. (Р. В.
Для идентификации Т- лимфоцитов крупного рогатого скота используется способность Т- клеточного антигена (CD3) взаимодействовать с эритроцитами барана (ЭБ). Эта возможность реализуется с помощью обычной реакции розеткообразования.
Для проведения данной реакции в лунку круглодонного планшета вносят 50 мкл исследуемой клеточной суспензии и 50 мкл 0,5 % суспензии ЭБ, приготовленной на ЗФР. Планшет центрифугируют в течение 5 минут при 1500 об/мин после чего ставят в холодильник (4°С) на 30 минут. Не удаляя надосадочную жидкость, осторожно вносят в лунку 50 мкл 1% глутарового альдегида приготовленного на изотоническом растворе хлорида натрия и выдерживают при комнатной температуре 5-7 минут. Надосадочную жидкость из лунок удаляют путем встряхивания с планшета. В лунки к осадку добавляют 100 мкл ЗФР. Осадок тщательно ресуспендируют. На обычных предметных стеклах готовят препарат-каплю, которую высушивают при комнатной температуре и фиксируют 10 минут в метаноле, затем окрашивают по Романовскому - Гимзе в разведении 1 : 5 в течение 5 минут.
Учет результатов: Т- лимфоциты хорошо просматриваются в обычном световом микроскопе при
Учет результатов: Т- лимфоциты хорошо просматриваются в обычном световом микроскопе при
1.5. Постановка реакции розеткообразования для определения
В - лимфоцитов
Для определения В- лимфоцитов
1.5. Постановка реакции розеткообразования для определения
В - лимфоцитов
Для определения В- лимфоцитов
Белки системы комплемента, относятся к факторам неспецифической защиты и одновременно, участвуют в реакциях специфического иммунного реагирования (иммунный лизис клеток мишеней). Т.к. В– клетки не имеют рецепторов к эритроцитам барана или быка, поэтому непосредственное взаимодействие таких эритроцитов с В- лимфоцитами невозможно. Для того, чтобы присоединение эритроцитов к В- лимфоцитам состоялось, т.е. образовалась розетка, необходимо посредничество комплемента и антиэритроцитарных антител. С этой целью эритроциты обрабатывают гемолитической сывороткой, содержащей антиэритроцитарные антитела, при этом создается комплекс антиген - антитело, с которым и связывается комплемент. Все В- лимфоциты имеют рецепторы к Сз компоненту комплемента и по розеткообразованию, т.е. по количеству лимфоцитов, присоединивших комплекс эритроцит - антитело - комплемент (ЕАС), можно судить о количестве В- лимфоцитов. Розеткообразующей клеткой ЕАС - РОК считается лимфоцит, к которому присоединились три и более ЕАС- комплекса.
1.5.1. Определение В-лимфоцитов с помощью ЕАС - розеткообразования
(Гущин И.С. и
1.5.1. Определение В-лимфоцитов с помощью ЕАС - розеткообразования
(Гущин И.С. и
Для определения В - лимфоцитов в реакции ЕАС - розеткообразования необходимо приготовление диагностикума, получаемого при иммунизации чужеродными эритроцитами (ЭБ) и инкубации последних с иммунными сыворотками в присутствии комплемента.
1.5.2. Приготовление взвеси эритроцитов быка
Из хорошо отмытых эритроцитов быка готовят 5 мл 2,5 % взвеси и добавляют к нему 1,25 мл 0,5 % раствора глутарового альдегида. Раствор хорошо размешивают и помещают на 20 минут в термостат при 37°С. Фиксированные эритроциты осаждают центрифугированием и ресуспендируют в 5 мл ЗФР.
1.5.3. Приготовление комплемента
В пробирку смоченную физиологическим раствором вносят 0,5 - 0,8
1.5.3. Приготовление комплемента
В пробирку смоченную физиологическим раствором вносят 0,5 - 0,8
1.5.4. Получение кроличьей антисыворотки против эритроцитов быка
В краевую вену уха кролика вводят 20 мл 10 % взвеси эритроцитов быка тремя инъекциями в течение 16 часов: 10 мл - изначально и по 5 мл через 6 и 16 часов после первой инъекции. На 7-е сутки после первой инъекции у кролика берут из уха кровь, которую помещают на 30 минут в термостат (37°С). Образовавшийся сгусток обводят для наступления ретракции и оставляют пробирку на ночь в холодильнике. Затем сыворотку отбирают, освобождают от примесей эритроцитов центрифугированием (10 минут при 1500 об/мин.) и выдерживают в холодильнике сутки. После этого, сыворотку вновь отсасывают, центрифугируют, прогревают 30 минут на водяной бане при 56°С (для инактивации комплемента) и определяют титр антиэритроцитарных антител. В замороженном виде сыворотка хранится в течение 8-12 месяцев.
1.5.5. Приготовление фиксированной ЕАС- системы
Для этого к 1,6 мл 2,5 %
1.5.5. Приготовление фиксированной ЕАС- системы
Для этого к 1,6 мл 2,5 %
1.5.6. Постановка реакции ЕАС - розеткообразования
В лунку планшета помещают 50 мкл
1.5.6. Постановка реакции ЕАС - розеткообразования
В лунку планшета помещают 50 мкл
1.6. Постановка реакций розеткообразования для определения субпопуляций нейтрофильных гранулоцитов
Подобно другим клеткам
1.6. Постановка реакций розеткообразования для определения субпопуляций нейтрофильных гранулоцитов
Подобно другим клеткам
Показано, что увеличение р. Е - РОН, дает возможность оценить степень и стадию воспалительного процесса на до клиническом уровне, когда еще не происходит увеличение общего количества лейкоцитов и скорости оседания эритроцитов (СОЭ). По показателю п.Е - РОН можно определить активность воспалительного процесса, если уровень п.Е - РОН увеличивается, если же п.Е - РОН снижается, то степень дефицита можно оценить по системе нейтрофильных гранулоцитов, обусловленного нарушением костномозгового созревания нейтрофильных гранулоцитов (НГ). С помощью определения количества ЕАС – РОН возможно оценить способность участия нейтрофилов в цитотоксических реакциях и их участие в иммунном фагоцитозе.
1.6.1. Метод определения р.Е - РОН ( Нестерова И.В., Колесникова Н.В.,
Чудилова
1.6.1. Метод определения р.Е - РОН ( Нестерова И.В., Колесникова Н.В.,
Чудилова
В лунку круглодонного планшета вносят 50мкл исследуемой суспензии клеток полученных методом, описанным в (1.4.; 1.4.1.) и 50 мкл 0,5 % суспензии ЭБ трижды отмытых ЗФР. Инкубируют в холодильнике (4°С) в течение 5минут и центрифугируют 5 минут при 1500 об/мин. Не удаляя надосадочную жидкость, осторожно в лунку вносят 50 мкл 1 % глутарового альдегида и выдерживают в течение 5-7 минут. Надосадочную жидкость из лунок удаляют путем встряхивания с планшета. К осадку добавляют 100 мкл ЗФР, хорошо ресуспендируют и на предметных стеклах готовят препарат - каплю. Препарат высушивают при комнатной температуре, фиксируют 10 минут в метаноле и окрашивают 5 минут по Романовскому - Гимзе в разведении 1:5.
Учет результатов: при увеличении (7×90) р. Е - РОН - подсчитывают в обычном световом микроскопе, на 100-200 нейтрофилов присоединивших 3 и более эритроцита быка нагруженных антигеном и комплементом. Исходя из общего числа лейкоцитов; нейтрофилов по количеству НГ- образующих розетки определяют абсолютное число р. Е - РОН.
1.6.2. Метод определение поздних Е-РОН (Нестерова И.В., Колесникова Н.В.,
Чудилова Г.А. 1996г.)
В
1.6.2. Метод определение поздних Е-РОН (Нестерова И.В., Колесникова Н.В.,
Чудилова Г.А. 1996г.)
В
Учет результатов: при увеличении (7×90) п.Е - РОН - подсчитывают в обычном световом микроскопе, на 100-200 нейтрофилов присоединивших 3 и более эритроцита быка нагруженных антигеном и комплементом. Исходя из общего числа лейкоцитов; нейтрофилов по количеству НГ- образующих розетки определяют абсолютное число п.Е– РОН по следующей формуле:
1.6.3. Определения ЕАС - РОН (Нестерова И.В., Колесникова Н.В.,
Чудилова Г.А. 1991г.)
В
1.6.3. Определения ЕАС - РОН (Нестерова И.В., Колесникова Н.В.,
Чудилова Г.А. 1991г.)
В
Учет результатов: при увеличении (7×90) ЕАС - РОН - подсчитывают в
Учет результатов: при увеличении (7×90) ЕАС - РОН - подсчитывают в
1.7.Постановка нагрузочных тестов in vitro
Постановка нагрузочных тестов in vitro целесообразна в
1.7.Постановка нагрузочных тестов in vitro
Постановка нагрузочных тестов in vitro целесообразна в
1.7.1 Постановка нагрузочных тестов с тимогеном, аргэхином, содэхином (Нестерова И.В.. Колесникова HLB., Чудилова Г.А. 1991г., Гугушвили Н.Н.2000г.)
Для нагрузочного теста используют следующие концентрации препаратов: Тимоген - 1,5 • 10-4 мл, Содэхин - 1,2 • 10-3 мл и Аргэхин -1,2 • 10-3 мл для взрослых коров (массой 450-550 кг) и телят (массой 80-116; 303-370 кг). Концетрации препаратов рассчитывались по аналогии расчета на килограмм массы взрослого животного, и предлагаемых терапевтических доз для телят.
В пробирку помещают 2 мл цельной крови, куда добавляют 2 мл препаратов (тимогена, аргэхина, содэхина) рассчитанных в соответствующих концентрациях. Инкубацию проводят в течение 30 минут в термостате при 37°С, после инкубации из цельной крови выделяют лейкоциты путем лизиса гемолитической жидкостью описанным в пункте (1.4.; 1.4.1.). Подсчитывают количество лейкоцитов в сеточной камере Горяева, доводят ЗФР до рабочей концентрации 2- 4 • 106 мл. Оценку действия препаратов, для определения уровня Т - лимфоцитов, В - лимфоцитов, р. Е - РОН; п. Е - РОН и ЕАС - РОН проводят, осуществляя постановку тестов розеткообразования.
1.8. Определение циркулирующих иммунных комплексов (ЦИК)
Метод основан на изменении величины светового
1.8. Определение циркулирующих иммунных комплексов (ЦИК)
Метод основан на изменении величины светового
Циркулирующие иммунные комплексы возникают в ходе иммунного ответа. Высокий уровень ЦИК является неблагоприятным признаком, и часто сопровождает системные заболевания, такие как красная волчанка, склеродермия и т.д.
1.8.1. Определение количества ЦИК в сыворотке крови (Digeon, 1977 г.)
Кровь берут из вены без добавления антикоагулянта, и инкубируют в течение 2-х часов для осаждения грубодисперсных белков, не имеющих отношения к ЦИК.
Приготовление боратного буфера: для этого берут 55 мл 1,24 % раствора борной кислоты добавляют 45 мл 1 % раствора буры. В смесь, добавляют 200 мл дистиллированной воды, доводя рН до 9,18. Готовят 3,75 % раствор полиэтиленгликоля (ПЭГ 6000) на боратном буфере.
Постановка реакции
В 0,3 мл сыворотки крови добавляют 0,6 мл 0,1 М
Постановка реакции
В 0,3 мл сыворотки крови добавляют 0,6 мл 0,1 М
ЦИК = (E1-Eo) × 1000,
где: E1 - экстинция опытной пробы
Е0- экстинция контрольной пробы.
1.9. Определение содержания иммуноглобулинов (Ig A, Ig M, Ig G) в
1.9. Определение содержания иммуноглобулинов (Ig A, Ig M, Ig G) в
По концентрации иммуноглобулинов основных (A, M, G) адекватно оценивается гуморальное звено иммунитета. Принцип метода основан на иммунологическом феномене преципитации. Антигены (в данном случае иммуноглобулины исследуемой сыворотки) дифференцируют в геле, образуя прочные оседлые, локализованные в ячейках геля иммунные комплексы с антителами (моноспецифической сывороткой против иммуноглобулинов), содержащиеся в геле. Исследуемая сыворотка, внесенная в лунки, диффундирует радиально с образованием колец преципитации. По диаметру кольца преципитации, в сравнении с контролем, определяют концентрацию антигена.
Приготовление реактивов
Веронал-мединаловый буфер (рН = 8,6) имеет следующий состав: 4,38 г
Приготовление реактивов
Веронал-мединаловый буфер (рН = 8,6) имеет следующий состав: 4,38 г
Для приготовления агарозы берут 1,5 % агар. К 1,5 г агара добавляют 100 мл веронал-мединалового буфера, закрывают колбу пробкой и варят на водяной бане 1,5 часа. Приготовленный агар хранят в холодильнике.
Постановка реакции
Перед работой 1,5 % раствор агара подогревают на водяной бане
Постановка реакции
Перед работой 1,5 % раствор агара подогревают на водяной бане
d =2 мм на расстоянии 15 мм друг от друга. Начало отсчета на чашке Петри отмечают карандашом. Аналогично пробивают лунки в агаре, содержащим анти-IgM- и aнти-IgG-сыворотки. Перед заполнением лунок исследуемыми сыворотками, чашки Петри ставят на черную бумагу и вносят по 20 мкл исследуемой сыворотки и стандартную сыворотку - известной концентрации разведенную физиологическим раствором 1:1. Чашки Петри помещают во влажный эксикатор, который ставят на холод (4°С) для IgA - и -IgG - тестирования - на 24 часа, а для IgM - оценки - на 48 часов. По истечении времени замеряют два взаимно перпендикулярных диаметра кольца преципитации в миллиметрах.
Уровень иммуноглобулинов определяют по формуле:
Расчет концентрации искомой сыворотки:
а) определение коэффициента наклона
Уровень иммуноглобулинов определяют по формуле:
Расчет концентрации искомой сыворотки:
а) определение коэффициента наклона
где d -квадрат кольца преципитации
б) концентрация исследуемой сыворотки (С)
d 2 исследуемой сыворотки
С = ———————————————— = мг / мл
КН
1.10. Реакция бактериального фагоцитоза нейтрофилов с определением степени завершенности (Нестерова И.В.,
1.10. Реакция бактериального фагоцитоза нейтрофилов с определением степени завершенности (Нестерова И.В.,
Оценка основной функции нейтрофилов - фагоцитарной с определением степени завершенности фагоцитарного акта (килинг, переваривания) позволяет судить о состоятельности неспецифического звена иммунной системы, и, в частности, системы НГ при бактериальной инфекции и других агентов воздействия. Принцип основан на количественном определении поглощенных и переваренных нейтрофилами микроорганизмов при совместной инкубации исследуемой крови с микробной тест культурой Staphylococcus aureus (штамма 209).
Уничтожение живых объектов, или завершенный фагоцитоз, следует рассматривать как итоговый феномен, в котором сфокусированы многие звенья эффекторного потенциала клетки - рецепция, поглощение, активация метаболизма, секреторная дегрануляция, образование пищеварительных вакуолей - фагосом. После образования фагосомы, захваченный микроорганизм подвергается действию целого ряда бактерицидных механизмов. Уничтожение чужеродных клеток проходят по двум механизмам - кислородзависимым и кислороднезависимым.
Кислородзависимые механизмы
Происходит резкая активация гексозомонофосфатного шунта, генерирующего НАДФ-Н, который используется для
Кислородзависимые механизмы
Происходит резкая активация гексозомонофосфатного шунта, генерирующего НАДФ-Н, который используется для
Кислороднезависимые механизмы
При реализации этого процесса происходят дисмутации надпероксидазы, потребляются ионы водорода
Кислороднезависимые механизмы
При реализации этого процесса происходят дисмутации надпероксидазы, потребляются ионы водорода
Получение проб крови, молока, молозива и маточной слизи или лохий проводят
Получение проб крови, молока, молозива и маточной слизи или лохий проводят
Для определения степени завершенности фагоцитоза берут каплю венозной крови на середину хорошо обезжиренного стекла, добавляют 10 мкл гепарина, затем 10 мкл
мясопептонного бульона и 10 мкл микробной взвеси лабораторного штамма № 209 на физиологическом растворе в концетрации 1 ×106. Покачиванием предметного стекла хорошо перемешивают ее содержимое и затем инкубируют в течение 120 минут во влажной камере в термостате при температуре 37 °С. После инкубации излишек крови осторожно удаляется при наклоне предметного стекла под углом 45°, и на предметном стекле остается микролейкоконцентрат, ограниченный хорошо видимыми контурами капли. Мазки высушивают на воздухе и фиксируют в течение 5минут в метаноле. Зафиксированные мазки окрашивают по Романовскому в течение 5-10 минут. Промывают дистиллированной водой, высушивают на воздухе, затем микроскопируют под иммерсией при увеличении 10×90.
Оценка поглотительной способности и переваривающей функции фагоцитов
Для оценки поглотительной функции
Оценка поглотительной способности и переваривающей функции фагоцитов
Для оценки поглотительной функции
Определяются следующие показатели:
«Активный» нейтрофил — нейтрофил, поглотивший микроб(ы). Процент фагоцитоза (% ФА) —процент «активных» нейтрофилов из общего числа посчитанных нейтрофилов.
Фагоцитарное число (ФЧ)—среднее число фагоцитированных микробов, деленное на 1 активный нейтрофил (ФА) Оценка поглотительной способности и переваривающей функции фагоцитов
Для оценки поглотительной функции фагоцитов: в мазке подсчитывается 100 нейтрофилов, в
Для оценки поглотительной функции фагоцитов: в мазке подсчитывается 100 нейтрофилов, в
Определяются следующие показатели:
«Активный» нейтрофил — нейтрофил, поглотивший микроб(ы). Процент фагоцитоза (% ФА) —процент «активных» нейтрофилов из общего числа посчитанных нейтрофилов.
Фагоцитарное число (ФЧ)—среднее число фагоцитированных микробов, деленное на 1 активный нейтрофил (ФА)
,
где М– число фагоцитированных микробов
Фагоцитарный интегральный индекс (ФИИ)
,
где Ф - 100 посчитанных нейтрофилов.
Завершенность фагоцитарного акта
Фагоцитарный интегральный индекс (ФИИ)
,
где Ф - 100 посчитанных нейтрофилов.
Завершенность фагоцитарного акта
Процент переваривания (%П) - отношение числа убитых бактерий (Муб) к общему числу фагоцитированных бактерий (м)
Индекс переваривания (ИП)- среднее число убитых микробов на 1 подсчитанный нейтрофил (ф), т.е. на 100 клеток
Интегральный показатель переваривающей активности (ИППА) - позволяет оценить фагоцитарную активность нейтрофилов
Интегральный показатель переваривающей активности (ИППА) - позволяет оценить фагоцитарную активность нейтрофилов
1.11. Определение лизоцимной активности в сыворотке крови
(Стогник В.И., Голик В.П.,
1.11. Определение лизоцимной активности в сыворотке крови (Стогник В.И., Голик В.П.,
Лизоцим является одним из показателей естественной резистентности и отвечает за бактерицидность крови, слюны и других биологических жидкостей.
В основу данного метода положена способность лизоцима быстро лизировать эталонную культуру Mycroccocus lisodeiticus.
1.11.1. Методика определения лизоцимной активности
В химическую пробирку вносят 4,9 мл 0,5 % раствора хлорида натрия и 0,1 мл сыворотки крови, добавляя в нее 1 млрд. суспензии Mycroccocus lisodeiticus. Измеряют оптическую плотность приготовленной суспензии на спектрофотометре (СФ - 46) с длиной волны λ = 540 нм (зеленый светофильтр). Затем пробирки помещают в термостат, при температуре 37°С на три часа для инкубации. После инкубации вновь измеряют оптическую плотность.
Оценка результатов лизоцимной активности (ЛА) проводится с помощью нефелометрии по изменению оптической плотности суспензии Mycroccocus lisodeiticus после добавления в нее сыворотки.
Расчет лизоцимной активности производят по формуле:
где ЛА - лизоцимная активность сыворотки
Расчет лизоцимной активности производят по формуле:
где ЛА - лизоцимная активность сыворотки
До и Д1 - оптическая плотность содержимого испытуемых проб соответственно до и после инкубации;
К - константа, равная 1,0 - для крупного рогатого скота.
1.12. Определение бактерицидной активности в сыворотке крови - БАСК
(О.В Смирнов.,
1.12. Определение бактерицидной активности в сыворотке крови - БАСК (О.В Смирнов.,
Метод основан на свойствах сыворотки крови, оказывать бактерицидное и бактериологическое действие на микроорганизмы (тест - E.coli).
Используемый фотонефелометрический метод основан на учете изменения оптической плотности питательной среды при добавлении в нее сыворотки.
Наибольшее распространение в практике получил упрощенный фотонефелометрический метод определения БАСК по О.В. Смирнову и Т.А. Кузьминой.
1.12.1. Метод определения бактерицидной активности в сыворотке крови
На физиологическом растворе готовят
1.12.1. Метод определения бактерицидной активности в сыворотке крови
На физиологическом растворе готовят
В пробирки вносят стерильно по 4,5 мл мясопептонного бульона. В обычную пробирку добавляют 1 мл исследуемой сыворотки, а в контрольную 1 мл физиологического раствора. Для получения очищенной сыворотки от форменных элементов и пластин, проводят осаждение примесей центрифугированием. Затем во все пробирки вносят (с помощью микропипетки или шприца) по одной капле 24 - часовой культуры Е. Coli. Содержимое пробирок перемешивают и измеряют оптическую плотность на спектрофотометре СФ - 46. Смесь, оставшуюся в пробирках, инкубируют в термостате три часа при температуре 37°С, после чего вновь измеряют оптическую плотность содержимого пробирок.
Бактерицидную активность сыворотки крови вычисляют по следующей формуле:
где БАСК- бактерицидная активность
Бактерицидную активность сыворотки крови вычисляют по следующей формуле:
где БАСК- бактерицидная активность
До- оптическая плотность опытной пробирки; Дк - оптическая плотность контрольной пробирки.
ОПРЕДЕЛЕНИЕ Т-, В-, NK-ЛИМФОЦИТОВ В МАЗКАХ КРОВИ ЖИВОТНЫХ
(по Пирсу,1962 г., в
ОПРЕДЕЛЕНИЕ Т-, В-, NK-ЛИМФОЦИТОВ В МАЗКАХ КРОВИ ЖИВОТНЫХ
(по Пирсу,1962 г., в
Данная методика является экспресс методом для определения. неспецифической эстеразы в клетках крови: Т-, NK - лимфоцитов Эстеразы входят в подгруппу (3.1). Механизм их действия на бактерии заключается в их переваривании благодаря способности гидролизовать белковые субстраты. Эстераза, или эластаза разрушает пептидогликаны бактериальной стенки. Одновременно в одном препарате можно определить В - клетки по окраске ядер. Применение методики основано на взаимодействии неспецифической эстеразы с α- нафтилацетатом. Эстераза способствует гидролизу α- нафтилацетата с образованием α - нафтола и уксусной кислоты (первичная реакция), которая создает слабокислую среду. Для поддержания рН в пределах 8,0 - 8,2 в систему вводят буферную смесь, предложенную нами, состоящую из КН2РО4 и Na2HРО4, что оказывало влияние на активность фермента эстеразы. Затем а- нафтол взаимодействует с красителем - нейтральным прочным синим В с образованием комплексного соединения азокрасителя (вторичная реакция). Образовавшийся комплекс (азокраситель) окрашивает эстеразу содержащуюся внутри Т-, и NК- лимфоцитов.
Кровь для исследования берут у сельскохозяйственных животных из яремной вены, из которой готовят мазок. Для этого каплю, крови наносят на край сухого обезжиренного стекла, которое удерживают между большим и средним пальцами левой руки. Впереди капли под углом 45° подводят шлифованный край покровного стекла так, чтобы образовавшийся угол между стеклами был равномерно заполнен кровью. Движением правой руки от себя каплю распределяют тонким слоем по поверхности предметного стекла без просветов в виде равномерной полоски, не выходящей за ее края. Мазки сушат на воздухе и фиксируют в парах 40% раствора формалина в течение 5 минут.
Приготовление буферных растворов
В состав буферной смеси входят: раствор А и Б
Приготовление буферных растворов
В состав буферной смеси входят: раствор А и Б
Приготовление раствора А. Для приготовления раствора А берут 0,34 г КН2РО4 (однозамещенного фосфорнокислого калия) и растворяют в небольшом количестве дистиллированной воды, затем в мерной колбе объемом 25 мл доводят до метки.
Приготовление раствора Б. Берут 8,9 г Na2HPO4, (двузамещенного фосфорнокислого натрия) и растворяют в небольшом количестве дистиллированной воды и в мерной колбе объемом 500 мл доводят до метки. Для лучшей диффузии растворы А и Б оставляют на сутки в темном месте. Затем смешивают 25 мл раствора А и 475 мл раствора Б, оставляют на сутки и змеряют рН буферного раствора. При этом необходимо получить рН от 8,0 до 8,2.
Приготовление инкубационной смеси
Правильное приготовление инкубационной смеси имеет немаловажное значение для дальнейшей окраски мазков. Готовят раствор 1 и 2.
Приготовление раствора 1
2,5 мг α- нафтилацетата растворяют в 0,125 мл ацетона разбавленного таким же количеством дистиллированной воды, добавляя небольшими порциями. После растворения к нему постепенно добавляют 6,25 мл дистиллированной воды.
Приготовление раствора 2
6,25 мг нейтрального прочного синего В растворяют в 6,25 мл дистиллированной воды, смешивая их постепенно. Для поддержания рН добавляют 0,125 мл буферного раствора с рН = 8,0-8,2.
Полученные растворы 1 и 2 смешивают, фильтруют в темной комнате через стеклянный фильтр.
Инкубация мазков
Инкубацию мазков проводят в темной комнате в течение 2-х часов.
Инкубация мазков
Инкубацию мазков проводят в темной комнате в течение 2-х часов.
Для дифференцировки лимфоцитов от других клеток крови в дальнейшем окрашивают ядра клеток (0,5–1 минуту) 0,25 % водным раствором Азуром-II, или 0,5% нейтральным красным, приготовленным на физиологическом растворе. Затем краску сливают, промывают дистиллированной водой, мазки высушивают на воздухе в темной комнате.
Микроскопия мазков
Микроскопию проводят при увеличении (90×15) с использованием иммерсионной системы. При этом Т- лимфоциты содержат одну или несколько гранул темного цвета расположенных по периферии клетки, ядра хорошо выражены; в NK- клетках ядра хорошо выражены, а цитоплазма окрашена диффузно в серый цвет. В- лимфоциты имеют хорошо выраженные ядра, со слабо окрашенной цитоплазмой, клетки гранул не содержат.
Реакция бактериального фагоцитоза нейтрофилов с определением степени завершенности (НЕСТЕРОВА И.В., КОЛЕСНИКОВА
Реакция бактериального фагоцитоза нейтрофилов с определением степени завершенности (НЕСТЕРОВА И.В., КОЛЕСНИКОВА
Оценка основной функции нейтрофилов – фагоцитарной с определением степени завершенности фагоцитарного акта (килинг, переваривания) позволяет судить о состоятельности неспецифического звена иммунной системы, и, в частности, системы НГ при бактериальной инфекции и других агентов воздействия. Принцип основан на количественном определении поглощенных и переваренных нейтрофилами микроорганизмов при совместной инкубации исследуемой крови с микробной тест культурой Staphylococcus aureus (штамма 209).
Уничтожение живых объектов, или завершенный фагоцитоз, следует рассматривать как итоговый феномен, в котором сфокусированы многие звенья эффекторного потенциала клетки - рецепция, поглощение, активация метаболизма, секреторная дегрануляция, образование пищеварительных вакуолей - фагосом. После образования фагосомы, захваченный микроорганизм подвергается действию целого ряда бактерицидных механизмов. Уничтожение чужеродных клеток проходят по двум механизмам - кислородзависимым и кислород независимым.
Кислородзависимые механизмы. Происходит резкая активация гексозомонофосфатного шунта, генерирующего НАДФ-Н, который используется
Кислородзависимые механизмы. Происходит резкая активация гексозомонофосфатного шунта, генерирующего НАДФ-Н, который используется
Кислороднезависимые механизмы. При реализации этого процесса происходят дисмутации надпероксидазы, потребляются ионы водорода и слегка повышается рН, а это создаст оптимальные условия для функционирования семейства катионных белков, которые еще не полностью охарактеризованы. Эти белки разрушают бактериальную мембрану как за счет протеиназного эффекта (нейтральная протеиназа, катепсин G), так и за счет непосредственного присоединения к поверхности микроорганизма. Низкие значения рН, лизоцим и лактоферрин представляет собой кислороднезависимые бактерицидные и бактериостатические факторы, которые могут действовать в анаэробных условиях. Убитые микроорганизмы расщепляются гидролитическими ферментами и продукты дегенерации высвобождаются из клетки.
Получение проб крови, молока, молозива и маточной слизи или лохий проводят
Получение проб крови, молока, молозива и маточной слизи или лохий проводят
Для определения степени завершенности фагоцитоза берут каплю венозной крови на середину хорошо обезжиренного стекла, добавляют 10 мкл гепарина, затем 10 мкл мясопептонного бульона и 10 мкл микробной взвеси лабораторного штамма № 209 на физиологическом растворе в концетрации 1×106. Покачиванием предметного стекла хорошо перемешивают ее содержимое и затем инкубируют в течение 120 минут во влажной камере в термостате при температуре 37°С. После инкубации излишек крови осторожно удаляется при наклоне предметного стекла под углом 45°, и на предметном стекле остается микролейкоконцентрат, ограниченный хорошо видимыми контурами капли. Мазки высушивают на воздухе и фиксируют в течение 5минут в метаноле. Зафиксированные мазки окрашивают по Романовскому в течение 5–10 минут. Промывают дистиллированной водой, высушивают на воздухе, затем микроскопируют под иммерсией при увеличении 10×90.
Оценка поглотительной способности и переваривающей функции фагоцитов
Для оценки поглотительной функции фагоцитов:
Оценка поглотительной способности и переваривающей функции фагоцитов
Для оценки поглотительной функции фагоцитов:
Определяются следующие показатели:
«Активный» нейтрофил – нейтрофил, поглотивший микроб (ы). Процент фагоцитоза (% ФА) – процент «активных» нейтрофилов из общего числа посчитанных нейтрофилов.
Фагоцитарное число (ФЧ)—среднее число фагоцитированных микробов, деленное на 1активный нейтрофил (ФА)
где М – число фагоцитированных микробов
Фагоцитарный интегральный индекс (ФИИ)
где Ф - 100 посчитанных нейтрофилов.
Завершенность фагоцитарного акта
Фагоцитарный интегральный индекс (ФИИ)
где Ф - 100 посчитанных нейтрофилов.
Завершенность фагоцитарного акта
Процент переваривания (% П) - отношение числа убитых бактерий (Муб) к общему числу фагоцитированных бактерий (м)
Индекс переваривания (ИП) – среднее число убитых микробов на 1 подсчитанный
Индекс переваривания (ИП) – среднее число убитых микробов на 1 подсчитанный
Интегральный показатель переваривающей активности (ИППА) –- позволяет оценить фагоцитарную активность нейтрофилов в абсо абсолютных значениях:
ОПРЕДЕЛЕНИЕ АКТИВНОСТИ МИЕЛОПЕРОКСИДАЗЫ
(по Sato, 1928г., в модификации Гугушвили Н.Н., 2000г.)
Активность
ОПРЕДЕЛЕНИЕ АКТИВНОСТИ МИЕЛОПЕРОКСИДАЗЫ
(по Sato, 1928г., в модификации Гугушвили Н.Н., 2000г.)
Активность
Определение миелопероксидазы (пероксидазы) – является одним из звеньев выявления микробицидных свойств системы крови. Простетическая в пероксидазе группа представлена гемом. Пероксидаза донор: Н2О2 – оксидоредуктаза, (код фермента (КФ) – 1.11.1.7) относятся к оксидоредуктазам (1). Фермент катализирует окисление различных веществ с помощью перекиси водорода: Донор + Н2О2 = Окислительный донор + 2Н2О.
Данный метод является быстрым и точным. Фермент пероксидаза поступает из тканей (жировых) в форменные элементы крови и локализуется в их цитоплазме в виде гранул (лизосом).
Для обнаружения миелопероксидазы применяют метод бензидиновой реакции, основанный на окислении бензидина
Для обнаружения миелопероксидазы применяют метод бензидиновой реакции, основанный на окислении бензидина
Фиксация мазков
На приготовленные высушенные мазки крови наливают 96 об.%о этиловый спирт
Фиксация мазков
На приготовленные высушенные мазки крови наливают 96 об.%о этиловый спирт
Приготовление буферных растворов
В состав буферной смеси входят: 0,1 М раствор триса C4H11NO3 (молекулярной массой 121,14), 0,1 М НСl (молекулярной массой 36,465). К 50 мл 0,1 М раствора триса добавляют 44,7 мл 0,1 М раствора НСl и доводят дистиллированной водой до 100 мл. Раствором 0,1 М НСl доводят рН смеси до 7,2 –7,5.
Приготовление инкубационной смеси
В инкубационную смесь входят растворы 1 и 2.
Приготовление раствора 1
1 г медного купороса растворяют в небольшом количестве воды и доливают до 100 мл буферной смесью (рН = 7,5).
Приготовление раствора 2
10 мг основного бензидина растворяют в 1,5 мл 96 об % этиловом спирте, добавляют 10 мл дистиллированной воды небольшими порциями. Затем в раствор вносят 14 мл буферной смеси, и 2-3 капли 1 % раствора перекиси водорода. Полученный раствор фильтруют через стеклянный фильтр.
Инкубация мазков
После фиксации мазки хорошо промывают в дистиллированной воде и сушат
Инкубация мазков
После фиксации мазки хорошо промывают в дистиллированной воде и сушат
В дальнейшем для дифференцировки нейтрофильных гранулоцитов от других клеток крови их ядра докрашивают (0,5–1 минуту) 0,5% раствором нейтральным красным, приготовленным на физиологическом растворе. Затем краску сливают, промывают дистиллированной водой и высушивают на воздухе.
Микроскопия мазков
Микроскопию проводят при увеличении (90×15) с использованием иммерсионной системы. Активность миелопероксидазы определяют по количеству гранул сине- коричневого цвета в цитоплазме нейтрофилов, ядра которых докрашены в красный цвет. Визуально проводят оценку цитохимической реакции по Kaplow,1955г. (рис.2.).
ОПРЕДЕЛЕНИЕ АКТИВНОСТИ ЩЕЛОЧНОЙ ФОСФАТАЗЫ В МАЗКАХ КРОВИ ЖИВОТНЫХ
(по Шубичу М.Г., 1965г.,
ОПРЕДЕЛЕНИЕ АКТИВНОСТИ ЩЕЛОЧНОЙ ФОСФАТАЗЫ В МАЗКАХ КРОВИ ЖИВОТНЫХ
(по Шубичу М.Г., 1965г.,
Фосфатазы относятся к гидролазам (3), щелочная фосфатаза (3.1.3.1.), которая способна разрывать связи Р --- О. Щелочная фосфатаза катализирует реакцию гидролиза моноэфира ортофосфата, расщепляя на спирт и фосфорную кислоту:
Моноэфир ортофосфат + Н2О = Спирт + Н3РО4
Активность щелочной фосфатазы присуща зрелым клеткам. Резкое уменьшение активности фермента в клетках приводит к снижению иммунитета, который наблюдается при хроническом миелолейкозе. Понижение естественной резистентности влечет за собой нарушение гомеостаза организма и приводит к снижению сохранности молодняка, репродуктивной способности и т. д.
Данный способ определения щелочной фосфатазы является наиболее быстрым и точным, т.к. фермент поступает из тканей, где они выполняют определённые внутриклеточные функции в форменные элементы крови, и локализуются в их цитоплазме в виде гранул – лизосом.
В инкубационной смеси щелочная фосфатаза приводит к ферментативному расщеплению α - нафтилфосфата до α-нафтола и двузамещенного фосфорнокислого натрия (первичная реакция). Затем α-нафтол связывается с прочным синим В, образуя азокраситель (вторичная реакция).
Фиксация мазков
Мазки крови сушат на воздухе и фиксируют в парах 40
Фиксация мазков
Мазки крови сушат на воздухе и фиксируют в парах 40
Приготовление буферных растворов
В состав буферной смеси входят (раствор – А): 0,025 М тетраборат натрия (Na2B407·10H20 с относительной молекулярной массой 382), для этого тетраборат натрия 0,953 г растворяют в дистиллированной воде в мерной колбе объёмом на 100 мл; (раствор – Б) - 0,1 М HCl (с относительной молекулярной массой 36,465). К 50 мл раствора А - добавляют раствор Б 4,6 - 5 мл. Доводят рН смеси до 9,18– 9,19.
Приготовление инкубационной смеси
Инкубационную смесь готовят в затемненной комнате. Для этого готовят раствор 1 и 2.
Приготовление раствора 1
В состав раствора 1 входят: 2,5 мг α-нафтилфосфат натрия и 2,5 мл боратного буфера. Растворяют α-нафтилфосфат натрия в небольшом количестве, а затем постепенно добавляют остальную часть боратного буфера.
Приготовление раствора 2
5 мг нейтрального прочного синего растворяют в 2,5 мл боратного буфера, смешивая их постепенно (рН = 9,18).
Полученные растворы 1 и 2 смешивают, фильтруют через стеклянный фильтр.
Инкубация мазков
На фиксированные формалином мазки наносят равномерным слоем инкубационную смесь. Необходимо
Инкубация мазков
На фиксированные формалином мазки наносят равномерным слоем инкубационную смесь. Необходимо
Микроскопия мазков
Микроскопию проводят при увеличении (90×15) с использованием иммерсионной системы. Активность щелочной фосфатазы определяют по количеству гранул коричневого цвета в цитоплазме нейтрофилов, ядра которых докрашены в красный цвет. Визуально проводят оценку цитохимической реакции по Kaplow, 1955г.
ОПРЕДЕЛЕНИЕ АКТИВНОСТИ КИСЛОЙ ФОСФАТАЗЫ В МАЗКАХ КРОВИ И В БИОЛОГИЧЕСКИХ ЖИДКОСТЯХ
(по
ОПРЕДЕЛЕНИЕ АКТИВНОСТИ КИСЛОЙ ФОСФАТАЗЫ В МАЗКАХ КРОВИ И В БИОЛОГИЧЕСКИХ ЖИДКОСТЯХ
(по
Кислая фосфатаза локализуется в НГ, относится к гидролазам - 3 (КФ 3.1.3.2.), которая способна разрывать связи Р --- О. Кислая фосфатаза катализирует реакцию гидролиза моноэфира ортофосфата, расщепляя на спирт и фосфорную кислоту:
Моноэфир ортофосфат + Н2О = Спирт + Н3РО4
Кислая фосфатаза присуща молодым клеткам. По повышению или понижению активности кислой фосфатазы в той или иной степени можно судить о патологическом процессе в организме животных. Так, снижение активности фермента в лимфоцитах наблюдается при хроническом лимфолейкозе, а повышение при инфекционном мононуклеозе.
Данный способ может быть экспресс методом для проведения цитохимического анализа активности кислой фосфатазы в нейтрофильных гранулоцитах в мазках крови. Применение методики основано на взаимодействии кислой фосфатазы с α-нафтилфосфатом натрия. Фосфатаза катализирует гидролиз α-нафтилфосфата натрия с образованием α-нафтола и фосфорнокислого двузамещенного натрия (первичная реакция). Для активации кислой фосфатазы в систему нами предложено ввести буферную смесь, янтарную кислоту (C4H6O4 с молекулярной массой 118,09), которая является естественным субстратом клеточных ферментов, участвующих в основном при внутриклеточном дыхании в синтезе АТР. Затем α-нафтол взаимодействует с красителем нейтральным прочным синим В с образованием комплексного соединения азокрасителя (вторичная реакция). Образовавшийся комплекс (азокраситель) окрашивает, кислую фосфатазу, содержащуюся внутри в виде гранул в цитоплазме нейтрофильных гранулоцитов.
Фиксация мазков
Мазки готовят сразу после взятия крови и сушат на воздухе,
Фиксация мазков
Мазки готовят сразу после взятия крови и сушат на воздухе,
Приготовление буферных растворов
В состав буферной смеси входят раствор А и Б : 0,2М раствор янтарной кислоты (с молекулярной массой 118,09), раствор – А, для этого берут 2,362 г янтарной кислоты и растворяют в дистиллированной воде в объёме на 100 мл; раствор – Б 0,2 М NaOH (молекулярной массой 36,465). Затем к 25 мл раствора А –(янтарной кислоты), добавляют 12 мг ЭДТА и 0,2М NaOH 32 мл, доводят рН до 4,9–5,0.
Приготовление инкубационной смеси
Инкубационную смесь готовят в затемненной комнате. Для этого готовят раствор 1 и 2.
Приготовление раствора 1
2,0 мг α-нафтилфосфата натрия растворяют в 1,3 мл дистиллированной воды и в 0,6612 мл буферной смеси, добавляя небольшими порциями, перемешивая.
Приготовление раствора 2
5 мг нейтрального прочного синего В растворяют в 2,5 мл буферной смеси, смешивая их постепенно (рН = 5,0).
Полученные растворы 1 и 2 смешивают, фильтруют в темной комнате через стеклянный фильтр.
Инкубация мазков
На фиксированные формалином мазки наносится равномерным слоем инкубационная смесь. Периодически
Инкубация мазков
На фиксированные формалином мазки наносится равномерным слоем инкубационная смесь. Периодически
Для дифференцировки НГ от других клеток крови в дальнейшем окрашивают ядра клеток (0,5–1 минуту) 0,5% водным раствором метиленовой сини. После окраски мазки промывают дистиллированной водой и высушивают на воздухе в темной комнате.
Микроскопия мазков
Микроскопию проводят при увеличении (90×15) с использованием иммерсионной системы. Активность кислой фосфатазы определяют по количеству гранул красно-коричневого цвета в цитоплазме нейтрофилов, ядра которых докрашены в голубой цвет. Визуально проводят оценку цитохимической реакции по Kaplow, 1955г. (рис.2).
ЛИЗОСОМАЛЬНО-КАТИОННЫЙ ТЕСТ ПО
В. М. Пигаревскому (1979г.)
Принцип метода основан на цитохимическом
ЛИЗОСОМАЛЬНО-КАТИОННЫЙ ТЕСТ ПО
В. М. Пигаревскому (1979г.)
Принцип метода основан на цитохимическом
Приготовление буферного раствора и инкубационной смеси
В состав буферной смеси входят: 0,1М
Приготовление буферного раствора и инкубационной смеси
В состав буферной смеси входят: 0,1М
Приготовление забуференного спиртового раствора прочного зеленого В
К 50 мл раствора А –(триса) добавляют 105 мл метанола и раствор Б 0,1М HCl – 45мл, которым доводят рН до 8,1- 8,2. Затем 100 мг прочного зеленого В растворяют в 100 мл метанолового буфера.
Фиксация и инкубация мазков
Фиксация и инкубация мазков проводится одновременно забуференным спиртовым раствором прочного зеленого В в течение 15 минут. После инкубации мазки промывают под проточной водой, затем дистиллированной водой и высушивают на воздухе в темной комнате. Затем докрашивают ядра клеток (2–3 минуты) 0,25%-ным раствором азура- II. Краску сливают, промывают дистиллированной водой и сушат мазки на воздухе в темном месте.
Микроскопия мазков
Микроскопию проводят при увеличении (90×15) с использованием иммерсионной системы. Лизосомально-катионные
Микроскопия мазков
Микроскопию проводят при увеличении (90×15) с использованием иммерсионной системы. Лизосомально-катионные
СПОНТАННЫЙ И СТИМУЛИРОВАННЫЙ NBT-ТЕСТ
(Нестерова И.В., Колесникова Н.В., Чудилова Г.А., 1980г.)
Принцип
СПОНТАННЫЙ И СТИМУЛИРОВАННЫЙ NBT-ТЕСТ
(Нестерова И.В., Колесникова Н.В., Чудилова Г.А., 1980г.)
Принцип
NBT-тест отражает степень активации кислородзависимого метаболизма, прежде всего функцию ГМФШ (гексозомонофосфатный шунт) и связанных с ним свободных радикалов. Никотинамиддинуклеотидфосфат (НАДФН) – оксидазный комплекс локализуется в плазматической мембране и при фагоцитозе вместе с ней инвагинируется во внутрь клетки. Поэтому активация, связанная с поглощением сопровождается внутрифагосомальным восстановлением NBT.
Кровь берут из вены и стабилизируют 2,7%-ным раствором ЭДТА в соотношении
Кровь берут из вены и стабилизируют 2,7%-ным раствором ЭДТА в соотношении
Результаты реакции: формазан-позитивные гранулы окрашиваются в синий цвет, ядра - в
Результаты реакции: формазан-позитивные гранулы окрашиваются в синий цвет, ядра - в
Средний цитохимический индекс расчитывают по формуле:
где a, b, c, d, e – количество НГ соответственно 0, 1, 2, 3, 4 степени.
Выведение коэффициента мобилизации (КМ) осуществляют по следующей формуле:
Определение NBT –теста нами разработано, также в молоке, в молозиве, в
Определение NBT –теста нами разработано, также в молоке, в молозиве, в
Заключение. При необходимости экспресс диагностики иммунного статуса в качестве ориентировочных тестов, позволяющих оценить грубые дефекты в иммунной системе, рекомендуются следующие тесты определения количества нейтрофильных гранулоцитов - Т-, В-, NK- клетки; бактериальный фагоцитоз и NBT-сп. и NBT-ст. - тесты по выше описанным методикам.
Комплексное исследование состояния микробицидных систем нейтрофилов у стельных животных, а также молодняка имеет важное значение для своевременного предупреждения различных заболеваний, предродовой и послеродовой патологии. Уточнение уровня повреждения нейтрофильных гранулоцитов дает возможность проведения полноценной иммунокоррекции в сочетании с базисной терапией основного заболевания, что улучшает результаты лечения и прогноз.





















































































 Қазақстан Республикасында мүгедектерді әлеуметтік қорғау
Қазақстан Республикасында мүгедектерді әлеуметтік қорғау Жасанды мүшелер
Жасанды мүшелер Клиническая фармакология препаратов, влияющих на сосудистый тонус
Клиническая фармакология препаратов, влияющих на сосудистый тонус Неполные аборты
Неполные аборты Нарциссическая организация личности. Подход О. Кернберга
Нарциссическая организация личности. Подход О. Кернберга Современные аспекты сердечно-легочной реанимации
Современные аспекты сердечно-легочной реанимации Психологическое консультирование
Психологическое консультирование Измерение артериального давления
Измерение артериального давления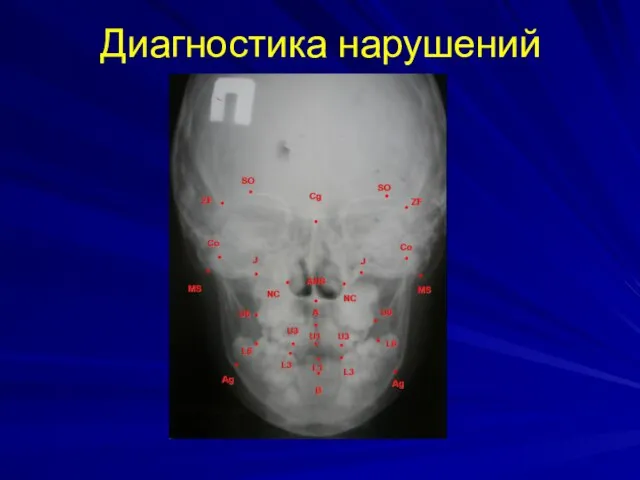 Диагностика нарушений
Диагностика нарушений Отрочество – особая пора жизни
Отрочество – особая пора жизни Лейкоциты. Роль нейтрофилов в организме
Лейкоциты. Роль нейтрофилов в организме Миокард инфарктісінің ЭКГ диагностикасы
Миокард инфарктісінің ЭКГ диагностикасы Механізми антитоксичної дії деяких компонентів рослинного походження
Механізми антитоксичної дії деяких компонентів рослинного походження Биоэтические проблемы человечества. Эвтаназия
Биоэтические проблемы человечества. Эвтаназия Может ли психика быть вечной?
Может ли психика быть вечной? Электроэнцефалография, как метод оценки функционального состояния коры большого мозга человека
Электроэнцефалография, как метод оценки функционального состояния коры большого мозга человека Трихоцефалез-қоздырғышы нематода
Трихоцефалез-қоздырғышы нематода Паранеопластические синдромы в неврологии
Паранеопластические синдромы в неврологии Заболевания гипофиза
Заболевания гипофиза Синдром Вискотта-Олдрича
Синдром Вискотта-Олдрича Медична служба українських збройних сил. Домедична допомога в умовах бойових дій. Евакуація
Медична служба українських збройних сил. Домедична допомога в умовах бойових дій. Евакуація Сироты (67)
Сироты (67) Нефротический синдром (2018)
Нефротический синдром (2018) Оказание неотложной помощи в быту
Оказание неотложной помощи в быту Теокомпозит при микроспории собак
Теокомпозит при микроспории собак Пухлини нирок
Пухлини нирок Вакцинация детей
Вакцинация детей Тема урока: Зрительный анализатор
Тема урока: Зрительный анализатор