Содержание
- 2. СПИСОК СОКРАЩЕНИЙ АГ –артериальная гипертензия АД- артетиальное давление ГП – глюкоза плазмы ГПП-1 –глюкагоноподобный пептид 1
- 3. Роль почки в обмене глюкозы участие в глюконеогенезе (почти 40% всего глюконеогенеза в состоянии голода), потребление
- 4. Метаболизм глюкозы в почках При повышении уровня гликемии продолжающаяся реабсорбция глюкозы из фильтрата способствует поддержанию гипергликемии.
- 5. Транспорт глюкозы (1): Процесс всасывания глюкозы в тонкой кишке, ее реабсорбция из клубочкового фильтрата в проксимальных
- 6. Транспорт глюкозы (2): Два основных вторичных активных транспортера глюкозы представлены в почках белками SGLT1 и SGLT2,
- 7. История вопроса: Идея воздействовать на почки для нормализации гликемии возникла при изучении патогенеза семейной почечной глюкозурии.
- 8. Патогенетическое обоснование использования sglt: обмен глюкозы в почках в норме Белок SGLT-2 встроен в виде туннеля
- 9. Патогенетическое обоснование использования sglt: обмен глюкозы в почках при патологии При развитии гипергликемии возрастает фильтрация глюкозы
- 10. Патогенетическое обоснование использования иSGLT: Фармацевтические компании начали поиски химического вещества, которое закрыло бы туннели SGLT-2, блокируя,
- 11. В настоящий момент в РФ зарегистрировано следующие представители класса иSGLT-2: Дапаглифлозин Эмпаглифлозин Канаглифлозин
- 12. ОБЩАЯ ХАРАКТЕРИСТИКА ГРУППЫ: достоинства снижение 0,8-0,9% низкий риск гипогликемии снижение массы тела инсулиннезависимый механизм действия умеренное
- 13. ОБЩАЯ ХАРАКТЕРИСТИКА ГРУППЫ: недостатки риск урогенитальных инфекций риск гиповолемии высокая цена
- 14. Противопоказания: Кетоацидоз Беременность и лактация Снижении СКФ:
- 15. С осторожностью применять: в пожилом возрасте при хронических урогенитальных инфекциях при приеме мочегонных средств
- 16. Режим дозирования: Дапаглифлозин (Форсига) (5мг, 10мг) Суточная доза 5 – 10мг Эмпаглифлозин (Джардинс) (10мг; 25мг) Суточная
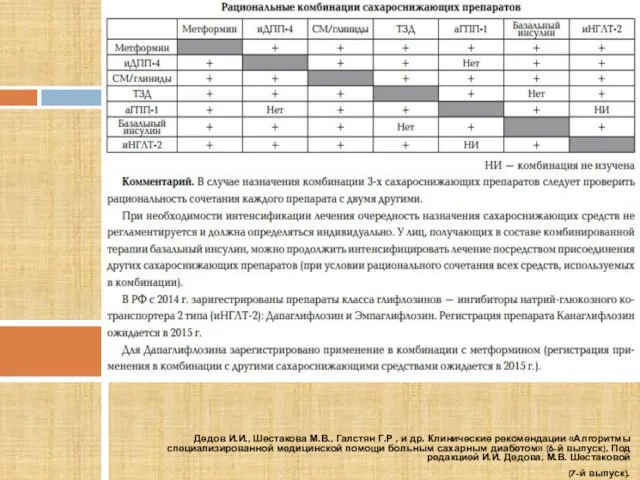
- 17. Место в алгоритмах
- 18. Место в алгоритмах Дедов И.И., Шестакова М.В., Галстян Г.Р , и др. Клинические рекомендации «Алгоритмы специализированной
- 19. Место в алгоритмах Дедов И.И., Шестакова М.В., Галстян Г.Р , и др. Клинические рекомендации «Алгоритмы специализированной
- 20. Дедов И.И., Шестакова М.В., Галстян Г.Р , и др. Клинические рекомендации «Алгоритмы специализированной медицинской помощи больным
- 21. Дедов И.И., Шестакова М.В., Галстян Г.Р , и др. Клинические рекомендации «Алгоритмы специализированной медицинской помощи больным
- 22. Результаты современных исследований применения иSGLT2
- 23. Достижение и поддержание снижения уровня HbA1c: Многоцентровое, рандомизированное, двойное слепое, плацебо контролируемое клиническое исследование 3 фазы
- 24. Плацебо-контролируемая редукция HbA1c: метанализ 22 исследования 6000 пациентов 7 исследований 1000 пациентов 3 исследования 500 пациентов
- 25. Достижение и поддержание снижения массы тела Вторая конечной точка: снижение массы тела. Снижение массы тела к
- 26. Двойная терапия: эффективность дапаглифлозина в сравнении с производными сульфонилмочевины (глипизид). Многоцентровое, рандомизационное, двойное слепое, 52-недельное исследование
- 27. Двойная терапия: безопасность дапаглифлозина в сравнении с производными сульфонилмочевины (глипизид). Частота эпизодов гипогликемии в группе приёма
- 28. Двойная терапия: дополнительное преимущество дапаглифлозина в сравнении с производными сульфонилмочевины (глипизид). Глипизид+ метформин: средняя масса тела
- 29. Монотерапия: эмпаглифлозин (25мг) в сравнении с иДПП4 (ситаглиптин -100мг) К 24 неделе исследования (n=899), на фоне
- 30. Двойная терапия: дапаглифлозин+метформин в сравнении с производными сульфонилмочевины (глипизид)+метформин. К 208 неделе исследования, на фоне комбинации
- 31. Двойная терапия: эмпаглифлозин+метформин в сравнении с производными сульфонилмочевины (глимепирид)+метформин. К 104 неделе исследования, на фоне комбинации
- 32. Двойная терапия: канаглифлозин (100 мг и 300мг) +иДПП4/аГПП1 в сравнении с плацебо+иДПП4/аГГП1 Многоцентровое, рандомизированное, двойное слепое,
- 33. К 18 неделе исследования на фоне канаглифлозина обнаружена большая редукция как HbA1c так и веса на
- 34. Тройная терапия: иSGLT-2 (канаглифлозин 300мг) в сравнении с другим препаратом. На фоне комбинации «канаглифлозин+метформин+сульфонилмочевина» против «ситаглиптин+метформин+сульфонилмочевина»,
- 35. Тройная терапия: иSGLT-2 Результат добавления эмпаглифлозина к комбинации «метформин+сульфонилмочевина»: Улучшение гликемического контроля (снижение HbA1c -0,6%) Снижении
- 36. Тройная терапия: иSGLT-2 Результат добавления канаглифлозина к комбинации «инкретиномиметик+другой препарат»: Снижение HbA1 при добавлении к иДПП4
- 37. Монотерапия: иSGLT2-стартовая терапия: Обзоры: 2 рандомизационых, двойных слепых, исследования 3 фазы для оценки эффективности и безопасности
- 38. Комбинированная терапия: иSGLT2, метформин и прочие препараты: Обзоры: 3 рандомизационых, двойных слепых, плацебоконтролируемых исследования 3 фазы
- 39. Двойная терапия: дапаглифлозин+метформин длительный период приёма Дапаглифлозин в комбинации с метформином доказал стойкий эффект в отношении
- 40. Канаглифлозин: микотические инфекции 2 рандомизационых клинических исследования: пациенты получали: 1 исследование: канаглифлозин 100/300мг или глимеперид 2
- 41. Дапаглифлозин: сердечная недостаточность Обзоры: 5 рандомизационых, клинических исследований, включавших пациентов (средний возраст 64 года, стаж диабета-
- 42. Канаглифлозин: пожилые пациенты Канаглифлозин, в дозе 100 и 300мг улучшал гликемический контроль и снижал массу тела
- 43. Дапаглифлозин: стоимость лечения Объединённое королевство (National Institute for Healf and Exellence, 2013): - дапаглифлозин признан как
- 44. Перспективы
- 45. Применение с инсулином при СД1: На фоне приема эмпаглифлозина (2,5мг, 10мг и 25мг) в комбинации с
- 46. Применение с инсулином при СД1: К 8неделе исследования (n=40), на фоне приёма эмпаглифлозина в комбинации с
- 47. Нефропротекция путем ингибирования SGLT2
- 48. Динамика уровня СКФ на фоне приёма эмпаглифорзина в течении 8 недель у лиц с СД1 при
- 49. Гемодинамические эффекты: Блокирование SGLT2 Блокирование РААС Блокирование SGLT2 и блокирование РААС Афферентная констрикция Эфферентная констрикция и
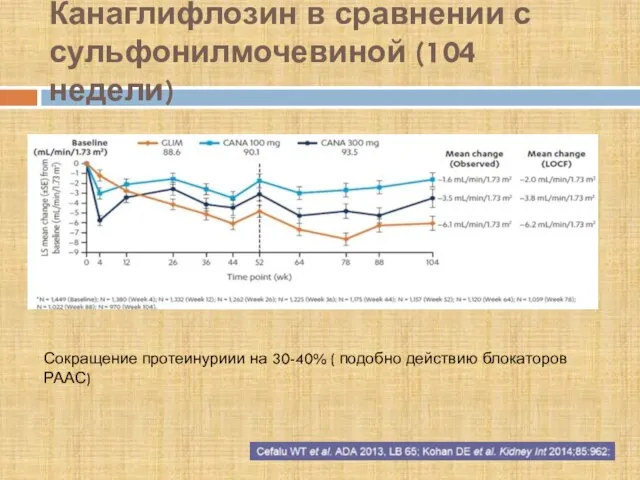
- 50. Канаглифлозин в сравнении с сульфонилмочевиной (104 недели) Сокращение протеинуриии на 30-40% ( подобно действию блокаторов РААС)
- 52. Скачать презентацию















































 Середня дорослість (Е. Еріксон)
Середня дорослість (Е. Еріксон) Профилактика и организация медицинской помощи при злокачественных новообразованиях
Профилактика и организация медицинской помощи при злокачественных новообразованиях Клиническая фармакология пожилых и беременных
Клиническая фармакология пожилых и беременных Патогенез лейкозов
Патогенез лейкозов Дерматомиозит
Дерматомиозит Вирусные гепатиты
Вирусные гепатиты Заболевания глаз
Заболевания глаз Первая помощь при кровотечении
Первая помощь при кровотечении Нейроэндокринные опухоли
Нейроэндокринные опухоли Аллергия (гиперчувствительность)
Аллергия (гиперчувствительность) Возрастная периодизация Д.Б. Эльконина
Возрастная периодизация Д.Б. Эльконина Robert Koch
Robert Koch Демографические показатели в оценке состояния общественного здоровья
Демографические показатели в оценке состояния общественного здоровья Общая характеристика зубных протезов
Общая характеристика зубных протезов Первичная профилактика патологического старения
Первичная профилактика патологического старения Средства, влияющие на функции органов дыхания
Средства, влияющие на функции органов дыхания Эритропоэздің нейро-гуморальдық реттелуі
Эритропоэздің нейро-гуморальдық реттелуі Прояви емоцій. Психічні стани, пов’язані з емоціями
Прояви емоцій. Психічні стани, пов’язані з емоціями Методы анализа белка в биологическом материале
Методы анализа белка в биологическом материале Как человек реагирует на явления в жизни и искусстве
Как человек реагирует на явления в жизни и искусстве Ультразвуковое исследование поджелудочной железы
Ультразвуковое исследование поджелудочной железы Потенция
Потенция Влияние ингибиторов гистондеацетилаз на формирование памяти
Влияние ингибиторов гистондеацетилаз на формирование памяти Анатомия наружного и среднего уха
Анатомия наружного и среднего уха Способы, с помощью которых возможно избежать последствия хронического недосыпания
Способы, с помощью которых возможно избежать последствия хронического недосыпания Здоровое питание и мой ребенок
Здоровое питание и мой ребенок Синдром анемии в обще-врачебной практике
Синдром анемии в обще-врачебной практике Способы и методика введения лекарственных средств детям
Способы и методика введения лекарственных средств детям