Содержание
- 2. План доклада Роль цитокинов в патогенезе воспалительных заболеваний Биологическое действие TNF-α и его растворимых рецепторов на
- 3. В последние несколько лет изучение роли цитокинов в патогенезе воспалительных заболеваний стало ключевым моментом для создания
- 4. Цитокины — низкомолекулярные гликопротеины, которые участвуют в передаче межклеточных молекулярных сигналов. К цитокинам относятся: Интерфероны (INF)
- 6. В зависимости от выполняемых функций: Провоспалительные Противовоспалительные Цитотоксические Стимулирующие антителообразование Участвующие в аллергических реакциях Регулирующие клеточную
- 7. Один и тот же цитокин может выполнять разные функции одновременно или в зависимости от конкретных условий,
- 8. При хроническом воспалении нарушается баланс провоспалительных и противовоспалительных цитокинов. К цитокинам с провоспалительным действием относят IL-1,
- 9. Механизмы действия цитокинов: Интракринный Аутокринный Паракринный Эндокринный
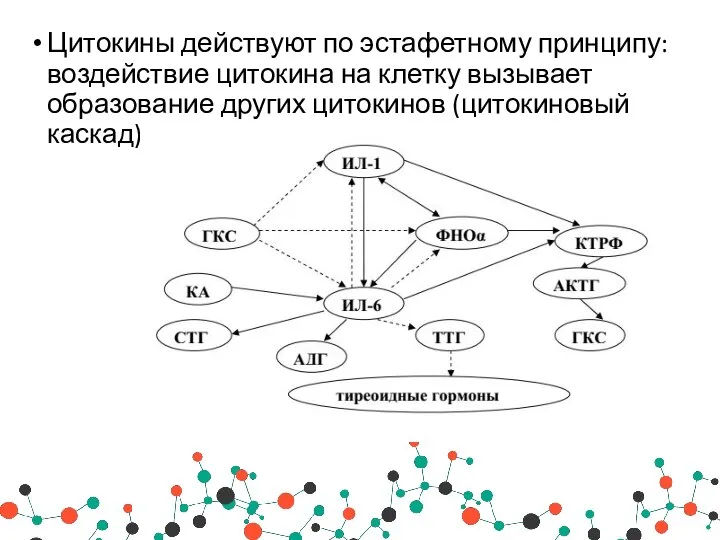
- 10. Цитокины действуют по эстафетному принципу: воздействие цитокина на клетку вызывает образование других цитокинов (цитокиновый каскад).
- 11. Фактор некроза опухолей альфа (TNF-α) действует как главный инициатор при запуске воспаления путем стимуляции синтеза других
- 12. По структуре TNF- α— гомотример, растворимая форма которого образуется из мембраноассоциированной, путем расщепления так называемым TNF-α
- 15. Выработка TNF, являющаяся ответом на антигенную стимуляцию стимулирует секрецию других провоспалительных интерлейкинов (IL-1, IL-6), хемокинов, простагландинов,
- 16. TNF-α регулирует не только воспалительные реакции, но также «подвижность» кератиноцитов. Во взаимодействие с кератиноцитами вовлекается множество
- 19. Псориаз-иммунопатологический гиперпролиферативный процесс
- 20. Обычно псориаз проявляется образованием красных, чрезмерно сухих, приподнятых над поверхностью кожи пятен — так называемых папул,
- 21. Псориаз является хроническим заболеванием, характеризующимся обычно волнообразным течением, с периодами спонтанных или вызванных теми или иными
- 22. Фазы воспалительных реакций I фаза — повреждение клеточных структур эпидермиса и дермы II фаза — включение
- 23. Активация CD4+ Т-лимфоцитов индуцирует ряд иммунных реакций, в том числе активацию макрофагов, синтезирующих широкий спектр провоспалительных
- 24. -У больных псориазом выработка TNF-α циркулирующими лимфоцитами и макрофагами повышена по сравнению со здоровыми людьми. -Уровень
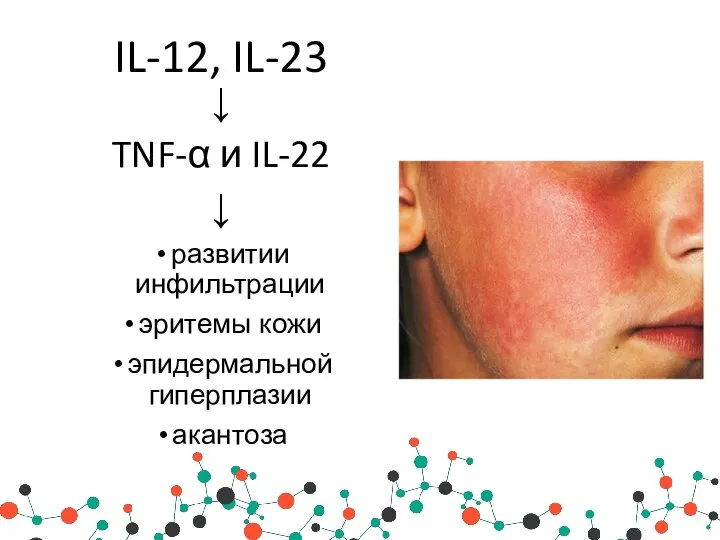
- 25. IL-12, IL-23 ↓ TNF-α и IL-22 ↓ развитии инфильтрации эритемы кожи эпидермальной гиперплазии акантоза
- 26. Исходя из патогенеза псориаза теоретически обоснованным методом лечения больных является терапия биологическими генно-инженерными препаратами. Стратегия биологической
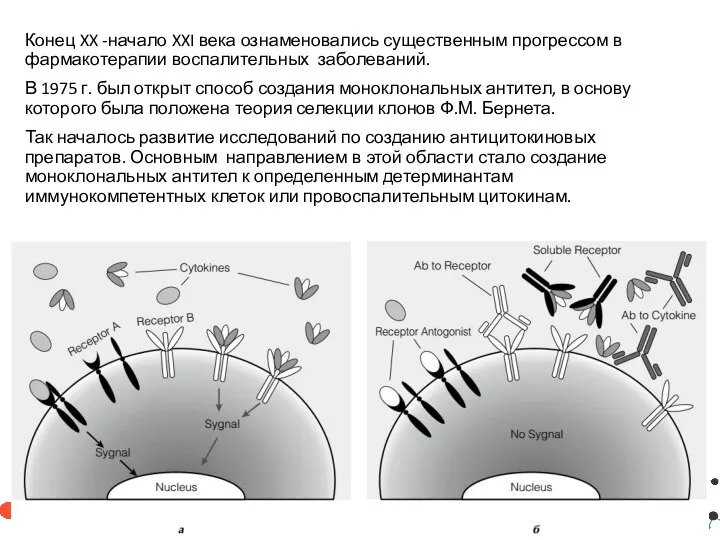
- 27. Конец XX -начало XXI века ознаменовались существенным прогрессом в фармакотерапии воспалительных заболеваний. В 1975 г. был
- 28. Препараты ингибиторов ФНО-альфа
- 29. Названия препаратов, созданных на основе моноклональных антител, отражают их структуру и основные свойства. Так, препараты с
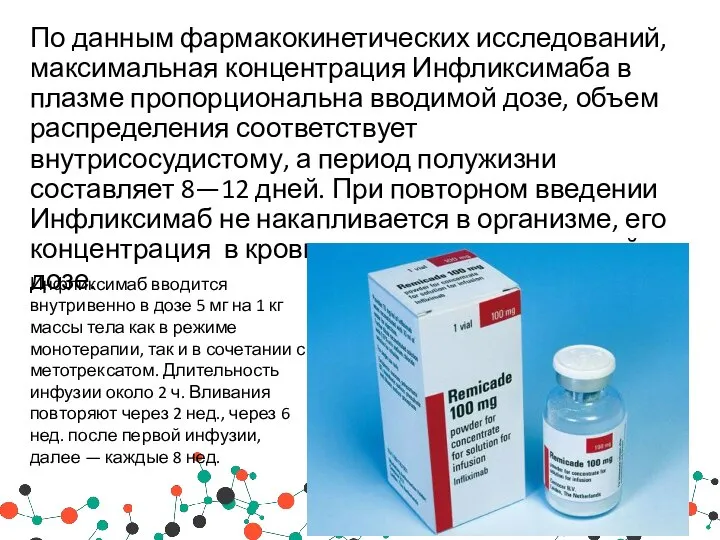
- 30. Инфликсимаб (Infliximab)(Ремикейд®) Инфликсимаб представляет собой химерные моноклональные антитела, состоящие из вариабельной (Fv) области высокоаффинных нейтрализующих мышиных
- 32. Механизм действия Инфликсимаб связывается с TNF-α с высокой специфичностью, аффинностью и авидностью, образует стабильные комплексы с
- 33. По данным фармакокинетических исследований, максимальная концентрация Инфликсимаба в плазме пропорциональна вводимой дозе, объем распределения соответствует внутрисосудистому,
- 34. Адалимумаб (Хумира(Humira®)) Первый и пока единственный препарат, представляющий собой полностью человеческие рекомбинантные моноклональные антитела к TNF-α.
- 35. Механизм действия Нейтрализует биологические функции TNF-α за счет блокады взаимодействия с поверхностными клеточными рецепторами р55 и
- 36. Этанерцепт (Etanercept)(Энбрел®) Гибридный димерный белок, имеющий домен сцепления с рецепторами человеческого TNF. Этанерцепт получен с помощью
- 37. Механизм действия Этанерцепт предупреждает клеточный ответ, опосредованный ФНО, способствуя биологической инактивации ФНО. Этанерцепт также может модулировать
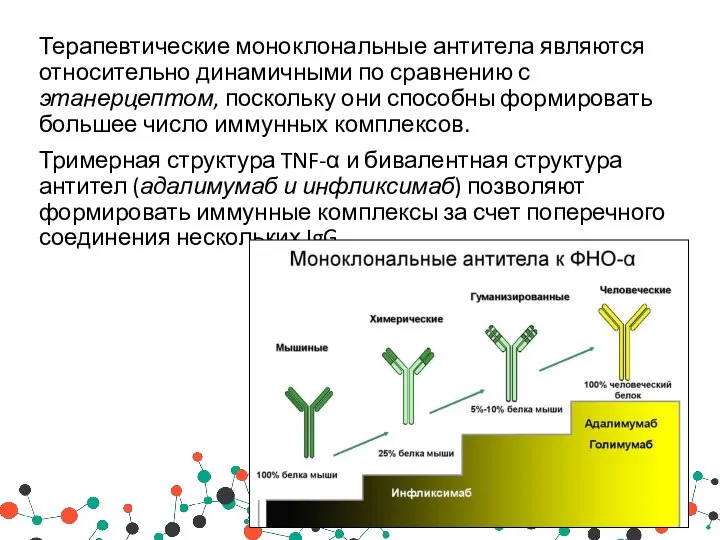
- 38. Терапевтические моноклональные антитела являются относительно динамичными по сравнению с этанерцептом, поскольку они способны формировать большее число
- 39. Биологические ингибиторы TNF-α являются чужеродными белками и поэтому обладают потенциальной иммуногенностью. Возможные клинические эффекты, являющиеся результатом
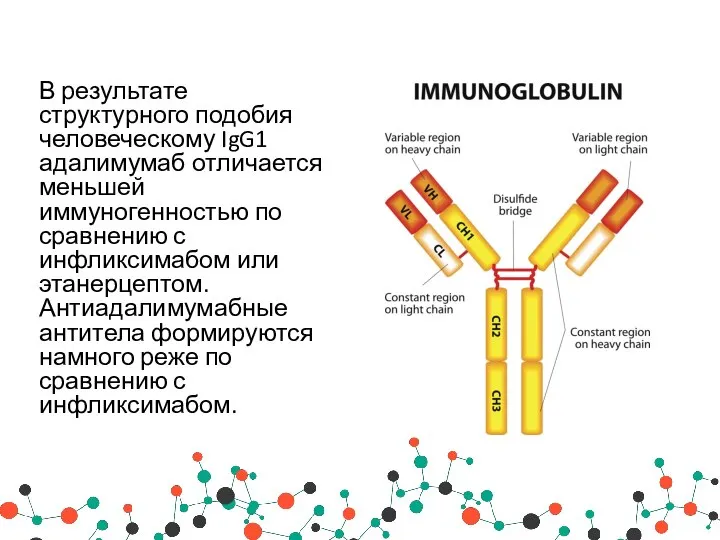
- 40. В результате структурного подобия человеческому IgG1 адалимумаб отличается меньшей иммуногенностью по сравнению с инфликсимабом или этанерцептом.
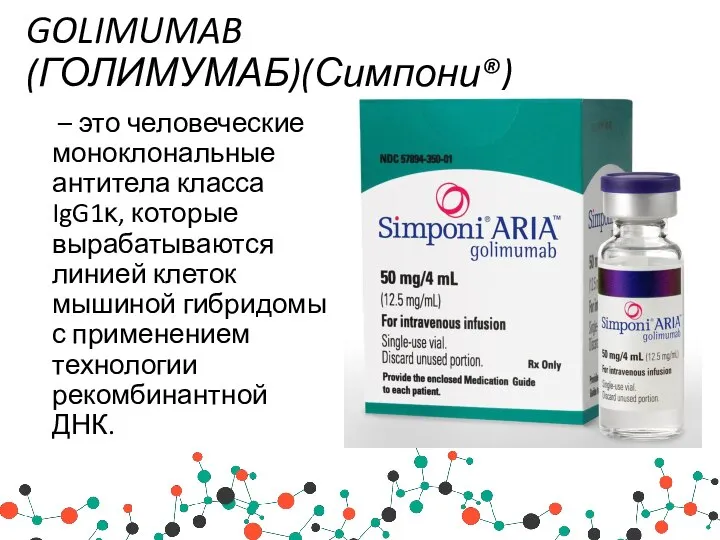
- 41. GOLIMUMAB (ГОЛИМУМАБ)(Симпони®) – это человеческие моноклональные антитела класса IgG1κ, которые вырабатываются линией клеток мышиной гибридомы с
- 42. Механизм действия Связывание ФНО-α человека голимумабом приводит к ингибированию (или подавлению) экспрессии молекул адгезии, в т.ч.
- 43. Цертолизумаба пэгол (Certolizumabi paegolum)(Симзия®) Это полиэтиленгликоль-конъюгированный ингибитор ФНО, который в отличие от других анти-ФНО моноклональных антител
- 44. Внедрение в клиническую практику биологических модификаторов иммунного ответа стало одним из наиболее крупных достижений медицины последних
- 46. Скачать презентацию



































 Опасность инфекционных заболеваний
Опасность инфекционных заболеваний Лекарственные средства, действующие на эфферентную иннервацию в области холинергических синапсов
Лекарственные средства, действующие на эфферентную иннервацию в области холинергических синапсов Medical faculty
Medical faculty Трихинеллез. Эпидемиология
Трихинеллез. Эпидемиология Системная красная волчанка
Системная красная волчанка Синдром внезапной детской смерти (СВДС)
Синдром внезапной детской смерти (СВДС) Седация в анестезиологии и интенсивной терапии
Седация в анестезиологии и интенсивной терапии Проблема Невынашивания: прегравидарная подготовка, ведение беременности
Проблема Невынашивания: прегравидарная подготовка, ведение беременности Острая ревматическая лихорадка у детей
Острая ревматическая лихорадка у детей Афазия
Афазия Болезнь Паркинсона
Болезнь Паркинсона Общая и экспериментальная психология. Деятельность
Общая и экспериментальная психология. Деятельность Стресс туралы Г. Сельенің ілімі. Эмоциялық стресс
Стресс туралы Г. Сельенің ілімі. Эмоциялық стресс Тромбофлебит поверхностных вен нижних конечностей
Тромбофлебит поверхностных вен нижних конечностей Наружное применение лекарственных средств
Наружное применение лекарственных средств Клиническая фармакогенетика
Клиническая фармакогенетика Профилактика вертикального пути передачи ВИЧ-инфекции. Особенности течения ВИЧ у детей
Профилактика вертикального пути передачи ВИЧ-инфекции. Особенности течения ВИЧ у детей Үй жұмысын тексеру. Есеп шығару
Үй жұмысын тексеру. Есеп шығару ЛФК кардиостимулятор
ЛФК кардиостимулятор Характерные симптомы, которые испытывают пациенты с опасными для жизни заболеванием (раны, жар, лимфедема)
Характерные симптомы, которые испытывают пациенты с опасными для жизни заболеванием (раны, жар, лимфедема) Мочевыделительная система
Мочевыделительная система Золотое правило этики
Золотое правило этики Заболевания желудочно-кишечного тракта
Заболевания желудочно-кишечного тракта Осложнения инфаркта миокарда
Осложнения инфаркта миокарда Восстановление подвижности тазобедренного сустава у лиц пожилого возраста после эндопротезирования
Восстановление подвижности тазобедренного сустава у лиц пожилого возраста после эндопротезирования Истмико-цервикальная недостаточность (ИЦН)
Истмико-цервикальная недостаточность (ИЦН) Расстройства памяти и интеллекта
Расстройства памяти и интеллекта CBL Аномалии рефракции
CBL Аномалии рефракции