Содержание
- 2. Условие задачи Министерством здравоохранения Республики Беларусь разработаны перечни лекарственных препаратов, которые должны содержаться в аптечках первой
- 3. Этапы работы 1. Классификация лекарственных средств 2. Фармакотерапевтическое действие веществ, указанных в задаче 3. Процессы окисления-восстановления
- 4. Классификация лекарственных средств Лекарство — вещество или смесь веществ природного или синтетического происхождения в виде лекарственной
- 5. Окисление-восстановление Единство двух процессов Окисление – процесс отдачи электронов Восстановитель отдаёт электроны, а сам окисляется Восстановление
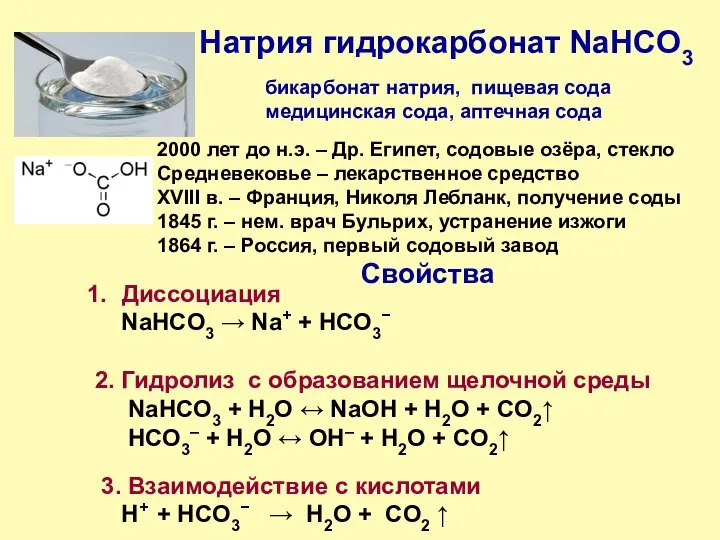
- 6. Натрия гидрокарбонат NaHCO3 Применение Нейтрализующее кислоту средство: H+ + HCO3− → H2О + CO2 ↑ при
- 7. Натрия гидрокарбонат NaHCO3 2000 лет до н.э. – Др. Египет, содовые озёра, стекло Средневековье – лекарственное
- 8. Натрия гидрокарбонат NaHCO3 Практическая часть 1. Образование слабощелочной среды в водном растворе. Индикатор – фенолфталеин 2.
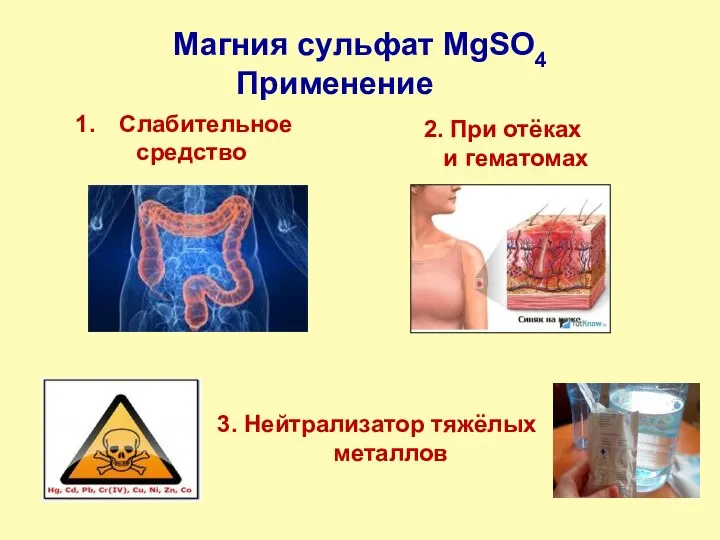
- 9. Магния сульфат MgSO4 Слабительное средство 3. Нейтрализатор тяжёлых металлов 2. При отёках и гематомах Применение
- 10. Магния сульфат MgSO4•7H2O гептагидрат сульфата магния, магнезия, магний сернокислый, горькая соль, английская соль, эпсомит, соль Эпсома
- 11. Магния сульфат MgSO4•7H2O Практическая часть Образование гидрата (на примере CuSO4 • 5H2O) 2. Опыт по осмотическому
- 12. Калия перманганат KMnO4 Применение 1. Антисептик - полоскание горла, промывание ран, обработка ожогов - промывание желудка
- 13. Калия перманганат KMnO4 1774 г. – шведский химик и минералог Йохан Готлиб Ган Свойства калий марганцовокислый,
- 14. Калия перманганат KMnO4 Практическая часть - в кислой среде до солей марганца в степени окисления +2:
- 15. Калия перманганат KMnO4 Практическая часть Взаимодействие перманганата калия с пероксидом водорода 2KMnO4 + 5H2O2 + 3H2SO4
- 16. Пероксид водорода Применение Кровоостанавлиающее средство при капиллярных кровотечениях Обеззараживание травмированных поверхностей Полоскание слизистых оболочек горла, носа
- 17. Пероксид водорода H2O2 перекись водорода, 30 %-й раствор – пергидроль 1818 г. – Луи Жак Тенар,
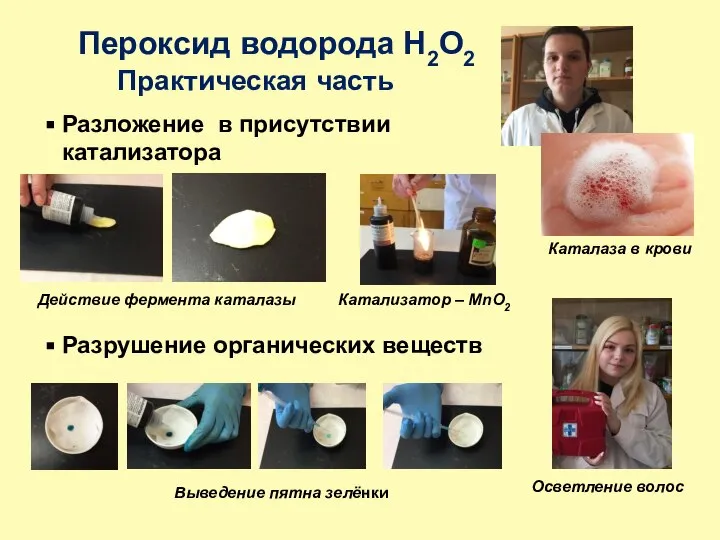
- 18. Пероксид водорода H2O2 Практическая часть Разложение в присутствии катализатора Катализатор – MnO2 Действие фермента каталазы Разрушение
- 19. Йод I2 Применение 1. Наружно: обработка ран, травм, при инфекционно-воспалительных поражениях кожи 2. Местно: тонзилит, ринит,
- 20. Йод I2 1811 г. – Бернар Куртуа, Франция Спиртовой раствор 5 %: I2 + KI +
- 21. Йод I2 Практическая часть Взаимодействие раствора йода с растительным маслом
- 22. Выводы На каких свойствах основано применение веществ из аптечки? Сода: реакция нейтрализации с более сильными кислотами,
- 24. Скачать презентацию


















 Внимание к безопасности и качеству лакокрасочных материалов
Внимание к безопасности и качеству лакокрасочных материалов Защита населения при радиационніх авариях
Защита населения при радиационніх авариях Санитарно-техническое оборудование пассажирского вагона
Санитарно-техническое оборудование пассажирского вагона Правила и порядок оказания первой помощи себе и пострадавшим при несчастных случаях, травмах, отравлениях и ЧС. (Тема 8)
Правила и порядок оказания первой помощи себе и пострадавшим при несчастных случаях, травмах, отравлениях и ЧС. (Тема 8) Мы за здоровый образ жизни
Мы за здоровый образ жизни Здоровье и безопасность. Викторина
Здоровье и безопасность. Викторина Принципы и правила здорового питания
Принципы и правила здорового питания УМП Тема 20 Организация пропаганды и информирования в области ГО и защиты от ЧС
УМП Тема 20 Организация пропаганды и информирования в области ГО и защиты от ЧС Авария на ЧАЭС
Авария на ЧАЭС Опасные погодные явления
Опасные погодные явления Информационная система специалиста по охране труда
Информационная система специалиста по охране труда Личная гигиена младших школьников
Личная гигиена младших школьников Управление охраной труда в организации. Лекция 11
Управление охраной труда в организации. Лекция 11 Табак. Влияние на организм подростка
Табак. Влияние на организм подростка Пожарная безопасность на производстве
Пожарная безопасность на производстве Система работы по ознакомлению детей дошкольного возраста с правилами дорожного движения
Система работы по ознакомлению детей дошкольного возраста с правилами дорожного движения Автономное выживание человека в природных условиях
Автономное выживание человека в природных условиях Организация рабочего места студента
Организация рабочего места студента Безопасность жизнедеятельности
Безопасность жизнедеятельности Презентация Средства и способы вооруженной борьбы ОБЖ «Основы обороны государства и воинская обязанность»
Презентация Средства и способы вооруженной борьбы ОБЖ «Основы обороны государства и воинская обязанность»  Памятка для родителей «Правила пожарной безопасности в Новогодние праздники»
Памятка для родителей «Правила пожарной безопасности в Новогодние праздники» Управление и взаимодействие в РСЧС. Постоянно действующие органы управления РСЧС. (Лекция 4)
Управление и взаимодействие в РСЧС. Постоянно действующие органы управления РСЧС. (Лекция 4) Методы и средства повышения безопасности технических систем и технологических процессов
Методы и средства повышения безопасности технических систем и технологических процессов День солидарности в борьбе с терроризмом. 3 сентября
День солидарности в борьбе с терроризмом. 3 сентября История возникновения дорожных знаков
История возникновения дорожных знаков Пожарная безопасность процессов сушки
Пожарная безопасность процессов сушки Терроризм
Терроризм Действия населения при угрозе террористического акта
Действия населения при угрозе террористического акта