Содержание
- 2. DRUG DISCOVERY BIOLOGY CHEMISTRY DEVELOPMENT Basic Research Indication Discovery Target ID Target Validation TARGET DISCOVERY Screening
- 3. Outline:
- 4. Drug Launch Costs Continue to Grow
- 5. * “Research-Based Pharmaceutical Companies” based on ethical pharmaceuticals sales and ethical pharmaceutical R&D only, tabulated by
- 6. Economic Value Of Health To Society Major Cardiovascular Diseases $5,142 Malignant Neoplasms 4,359 Infectious Diseases (including
- 7. The Delicate Biomedical “Ecosystem” Government Pharma Biotech Academia We are interlinked
- 8. Терминология, употребляемая в клинических исследованиях
- 9. Уполномоченные органы (Regulatory Authority): Органы, обладающие правом осуществлять регулирующие функции. Применительно к настоящему стандарту термин "уполномоченные
- 10. Стандартные операционные процедуры (Standard Operating Procedures/SOPs) Подробные письменные инструкции, предназначенные для достижения единообразия при осуществлении определенной
- 11. Рандомизация (Randomisation) Процесс распределения субъектов исследования по группам лечения или контроля случайным образом, позволяющий свести к
- 12. Препарат сравнения (Comparator Product) Исследуемый или зарегистрированный лекарственный продукт (т.е. активный контроль) либо плацебо, используемый(ое) как
- 13. Отчет о клиническом испытании/исследовании (Trial/Study Report) Отчет в письменной форме, представляющий собой описание клинического испытания/исследования какого-либо
- 14. FDA, Article 314.126. Adequate and well-controlled studies “a) Цель проведения клинических исследований лекарства – выявить и
- 15. Исследование должно решить основные поставленные цели (например, достаточная выборка). Минимизировать системные ошибки (статистические методы не могут
- 16. Планирование. Planning (9%) Дизайн, методы. Design (40%) Проведение и сбор данных. Execution/data collection (32%) Обработка данных.
- 17. использование адекватной контрольной группы (use of appropriate concurrent control) использование слепых методов/ослепления (use of blinding procedures)
- 18. Дополнительная терапия, которая не предусмотрена протоколом исследования и которую могут получать пациенты во время участия в
- 19. Контрольная группа предоставляет возможность проводить сравнение – в ней на тех же пациентах оцениваются другие возможные
- 20. Плацебо. Placebo Позволяет определить «чистый» эффект лечения исследуемым продуктом Может использоваться при не угрожающих жизни хронических
- 21. Стандартный подход в клинических исследованиях - везде где возможно применяется ослепление. Это означает, что ни пациент
- 22. Процедуры ослепления Использование плацебо (должно быть неотличимо от исследуемого продукта по вкусу, запаху, цвету и т.д.)
- 23. Рандомизация. Randomization Распределение пациентов случайным образом в группы с целью предотвращения ситуации, когда контрольная и опытная
- 24. Простая рандомизация. Simple Randomization Пациенты распределяются в группы абсолютно случайным образом. Однако простая рандомизация может оказаться
- 25. Блоковая Рандомизация. Block Randomization Гарантирует, что количество пациентов, распределенных в опытную и контрольную группы одинаковы после
- 26. Стратифицированная Рандомизация. Stratified Randomization Простая или блоковая рандомизация могут в некоторых случаях не работать, и, как
- 27. Выборка исследования. Study Sample Целевая популяция (Target population) – определяется критериями включения/исключения (inclusion / exclusion criteria)
- 28. Основные статистические методы Сравнение данных между пациентами (Between patient comparison) Параллельные группы (Parallel group design) Каждый
- 29. Основные статистические методы (2) Перекрестный дизайн (Cross-over design) Последовательное проведение двух или более видов терапии (в
- 30. Сравнительный обзор
- 31. Целевая популяция. Target Population Критерии включения/исключения определяют целевую популяцию, из которой формируется выборка пациентов для исследования.
- 32. Нулевая и альтернативные гипотезы. Null and Alternative Hypotheses Основные вопросы клинического исследования часто формулируются следующим образом:
- 33. Нулевая и альтернативные гипотезы. Null and Alternative Hypotheses(2) Предположим, что µ1 и µ2 представляют собой средние
- 34. Пи-величина. P-value Главный вопрос, на который мы хотим получить ответ: Говорят ли полученные данные, что достоверных
- 35. Пи-величина. P-value (2) Пример: Снижение АД: X1 (среднее) = 8.2 mmHg (активный препарат) X2 (среднее) =
- 36. Пи-величина. P-value (3) Два возможных сценария: P = 0.03 3% вероятность что различий нет P =
- 37. Определения Ho нулевая гипотеза (null hypothesis) H1 альтернативная гипотеза (alternative hypothesis) Тест: собранный массив данных для
- 38. Определения (2) Если p Если p > 0.05, то мы имеем статистически незначимые результаты (при 5%
- 39. Подходы, которыми мы пользуемся в статистике, также постулируют неизбежное наличие возможности ошибочных заключений. Важно отметить, что
- 40. Ошибка второго типа и мощность Type II Error and Power Мощность - это вероятность того, что
- 41. Ошибка второго типа и мощность Type II Error and Power (2) Мощность увеличивают за счет увеличения
- 42. Вычисление объема выборки На стадии планирования исследования мы хотим быть уверенными, что у нас будет достаточное
- 43. Вычисление объема выборки (2) Также для каждого статистического теста нам необходимы другие дополнительные сведения. Если мы
- 44. Вычисление объема выборки (3) ICH: Для расчета объема выборки у нас должны быть определены: Оцениваемый параметр
- 45. Вычисление объема выборки (4) Пример: Исследование с параллельными группами сравнивает влияние плацебо и активного препарат на
- 46. Проблемы при определении объема выборки Количество пациентов ограничено (например, орфанные заболевания). Что можно предпринять? Включить больше
- 47. Проблемы при определении объема выборки (2) 3. Стандартное отклонение имеет большую величину. Что делать, Стандартное отклонение
- 48. Стандартное отклонение. Standard Deviation Что нужно помнить: Важно иметь точные данные о величине σ Выбирать величину
- 49. Стандартное отклонение. Standard Deviation (2) Для лабораторных данных вариация может быть обусловлена: Вариация у одного пациента
- 50. Стандартное отклонение. Standard Deviation (3) Для лабораторных данных вариация может быть обусловлена: Вариация от пациента к
- 51. Стандартное отклонение. Standard Deviation (4) Величина σ2 может быть снижена за счет набора более однородной группы
- 52. Отчет исследования ICH E3 Данное руководство предназначено помочь спонсорам исследования подготовить отчет, который будет удовлетворять 4
- 53. Формат отчета Что было запланировано Протокол Статистический план Что представлено (результаты) Аномальные данные (нарушения и отклонения
- 54. Информация по пациентам Скринированные пациенты Не вошедшие в исследование (очень ценная информация) Вошедшие в исследование Рандомизированные
- 55. Конкурс на лучшую авиакомпанию по результатам опроса пассажиров Global Earth Airlines (GEA) 56% все было великолепно
- 56. Конкурс на лучшую авиакомпанию по результатам опроса пассажиров (2) Global Earth Airlines (GEA) 56% все было
- 57. Конкурс на лучшую авиакомпанию по результатам опроса пассажиров (3) Global Earth Airlines (GEA) 56% все было
- 58. Зачем мы проводим клинические исследования? Существуют две возможно главных цели клинических исследований. Первая цель – оценить
- 59. Зачем мы проводим клинические исследования (2)? Далее автор продолжает… Наверно будет правильно добавить, что первая цель
- 60. Мета анализ Позволяет комбинировать результаты различных клинических исследований Сильно зависит от гомогенности результатов Как правило такой
- 61. Number Needed to Treat (NNT) The Number needed to treat (NNT) – число больных, которое необходимо
- 62. Number Needed to Treat (2) В контрольной группе смертность 21/82 = 0.256 В опытной группе смертность
- 63. Оценка данных Отчеты о клинических исследованиях могут содержать следующие разделы: Цель Дизайн Участники Субъекты исследования Методы
- 64. Оценка данных (2) Список вопросов к авторам: О чем это исследование – ясно ли сформулированы его
- 65. Оценка данных (3) Как боролись с системными ошибками? Репрезентативна ли выборка? Достаточен ли объем выборки? Представлены
- 66. Оценка данных (4) Проводился ли анализ данных на предмет того, что различия между группами могли быть
- 67. Оценка данных (5) Были ли результаты, которые не были обсуждены? Если ответ да, то почему? Согласуются
- 68. Оценка данных (6) Три самых важных вопроса: Системные ошибки (Bias) – могли результаты быть искажены в
- 70. Скачать презентацию



































































 Определение свинца в золе пищевых продуктов
Определение свинца в золе пищевых продуктов Роль лимфатической системы головного мозга в поддержании гомеостаза центральной нервной системы
Роль лимфатической системы головного мозга в поддержании гомеостаза центральной нервной системы Дисфункциональные маточные кровотечения
Дисфункциональные маточные кровотечения Особенности лечения переломов при остеопорозе
Особенности лечения переломов при остеопорозе Тактика ведения многоплодной беременности при синдроме обратной артериальной перфузии
Тактика ведения многоплодной беременности при синдроме обратной артериальной перфузии Активное слушание
Активное слушание Имплантируемые кардиовертер-дефибрилляторы
Имплантируемые кардиовертер-дефибрилляторы Всасывание фармацевтических субстанций у детей после различных путей введения в организм
Всасывание фармацевтических субстанций у детей после различных путей введения в организм Эндокринология. Лечение сахарного диабета. (Лекция 3)
Эндокринология. Лечение сахарного диабета. (Лекция 3) Шизофрения
Шизофрения Значение онкомаркеров для диагностики колоректального рака
Значение онкомаркеров для диагностики колоректального рака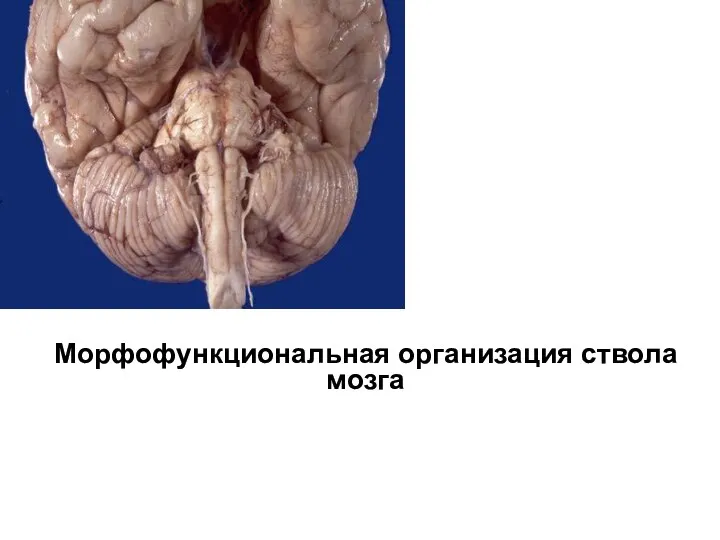 Морфофункциональная организация ствола мозга
Морфофункциональная организация ствола мозга Иммунитет. Назначение иммунитета
Иммунитет. Назначение иммунитета Мужской климакс
Мужской климакс Консервативные и оперативные методы лечения в гинекологии
Консервативные и оперативные методы лечения в гинекологии Шигеллы. Клиническая картина
Шигеллы. Клиническая картина Күйіктөр көзіндегі жедел жәрдем негідзері
Күйіктөр көзіндегі жедел жәрдем негідзері Больной в коме
Больной в коме Нравственное здоровье учащихся как фактор, влияющий на развитие личности
Нравственное здоровье учащихся как фактор, влияющий на развитие личности Лаборатория безопасности
Лаборатория безопасности Техника изготовления аппарата Катца и Шины Тигерштедта
Техника изготовления аппарата Катца и Шины Тигерштедта Болезни органов дыхания
Болезни органов дыхания Участие медицинской сестры педиатрического участка в мероприятиях по сохранению и укреплению здоровья недоношенных детей
Участие медицинской сестры педиатрического участка в мероприятиях по сохранению и укреплению здоровья недоношенных детей Ультразвуковая диагностика в гинекологии
Ультразвуковая диагностика в гинекологии Апаттар медицинасын ұйымдастыру принциптері
Апаттар медицинасын ұйымдастыру принциптері Деятельностный подход
Деятельностный подход Тест. Який ти друг !
Тест. Який ти друг ! Анализ полиморфизма гена IL6 у больных туберкулезом легких с разными клиническими формами
Анализ полиморфизма гена IL6 у больных туберкулезом легких с разными клиническими формами