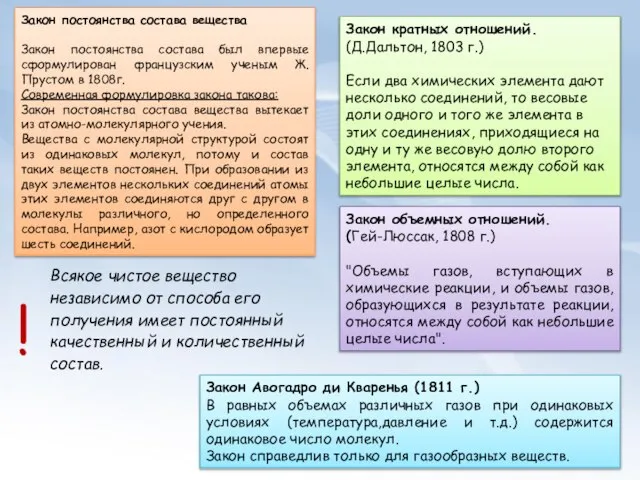
Закон постоянства состава вещества
Закон постоянства состава был впервые сформулирован французским ученым
Ж. Прустом в 1808г.
Современная формулировка закона такова:
Закон постоянства состава вещества вытекает из атомно-молекулярного учения.
Вещества с молекулярной структурой состоят из одинаковых молекул, потому и состав таких веществ постоянен. При образовании из двух элементов нескольких соединений атомы этих элементов соединяются друг с другом в молекулы различного, но определенного состава. Например, азот с кислородом образует шесть соединений.
!
Закон кратных отношений.
(Д.Дальтон, 1803 г.)
Если два химических элемента дают несколько соединений, то весовые доли одного и того же элемента в этих соединениях, приходящиеся на одну и ту же весовую долю второго элемента, относятся между собой как небольшие целые числа.
Закон объемных отношений.
(Гей-Люссак, 1808 г.)
"Объемы газов, вступающих в химические реакции, и объемы газов, образующихся в результате реакции, относятся между собой как небольшие целые числа".
Закон Авогадро ди Кваренья (1811 г.)
В равных объемах различных газов при одинаковых условиях (температура,давление и т.д.) содержится одинаковое число молекул.
Закон справедлив только для газообразных веществ.







 Древний Китай
Древний Китай История понятия государство. Теории возникновения государства. Основные признаки государства
История понятия государство. Теории возникновения государства. Основные признаки государства Презентація на тему Георг Сімон Ом
Презентація на тему Георг Сімон Ом Презентация Театр в 18 веке в Росиии
Презентация Театр в 18 веке в Росиии Внеклассное мероприятие в начальной школе - презентация для начальной школы
Внеклассное мероприятие в начальной школе - презентация для начальной школы Работа с базами данных
Работа с базами данных Министерство транспорта РФ
Министерство транспорта РФ «Банкир – это центральная фигура. Он держит на своих плечах весь мир.» Герберт Кэссон
«Банкир – это центральная фигура. Он держит на своих плечах весь мир.» Герберт Кэссон Разработка метеостанции на базе ATmega8 для измерения влажности, давления и CO2
Разработка метеостанции на базе ATmega8 для измерения влажности, давления и CO2 Подростковый возраст материалы для родительского собрания
Подростковый возраст материалы для родительского собрания Doping problem in sports. (Lecture 8)
Doping problem in sports. (Lecture 8) МБОУ «СОШ№12» г. Байкальск Внеклассное мероприятие По изобразительному искусству 8 класс Учитель : Грищенко Наталья Константино
МБОУ «СОШ№12» г. Байкальск Внеклассное мероприятие По изобразительному искусству 8 класс Учитель : Грищенко Наталья Константино Презентация Переход к Новой экономической политике
Презентация Переход к Новой экономической политике  Ландшафтный дизайн. Дренаж, декоративные покрытия дорожек
Ландшафтный дизайн. Дренаж, декоративные покрытия дорожек Грек-латын дублеттері
Грек-латын дублеттері Компьютер своими руками
Компьютер своими руками Износ основных фонов
Износ основных фонов Организация производства и продаж прибора для неинвазивного (чрезкожного) мониторинга содержания сахара в крови человека
Организация производства и продаж прибора для неинвазивного (чрезкожного) мониторинга содержания сахара в крови человека Индивидуализация и дифференциация обучения в современной школе. Методическая тема учителя русского языка и литературы МОУ СОШ
Индивидуализация и дифференциация обучения в современной школе. Методическая тема учителя русского языка и литературы МОУ СОШ  Числовые и символьные массивы
Числовые и символьные массивы Символическое значение животных и предметов в архитектурном декоре
Символическое значение животных и предметов в архитектурном декоре Әлем. XXI ғасыр
Әлем. XXI ғасыр Финансовая грамотность
Финансовая грамотность Построение проекций плоских фигур
Построение проекций плоских фигур Особенности деловых отношений в разных культурах
Особенности деловых отношений в разных культурах Организация занятий физической культурой с учащимися медицинских групп и детей с ОВЗ
Организация занятий физической культурой с учащимися медицинских групп и детей с ОВЗ Презентация "Эффективные способы рекламы" - скачать презентации по Экономике
Презентация "Эффективные способы рекламы" - скачать презентации по Экономике Йоганнес Кеплер
Йоганнес Кеплер