Сложные эфиры Сложные эфиры карбоновых кислот – это соединения, образующиеся при взаимодействии органических кислот со спиртами
Содержание
- 2. Номенклатура СН3СООС2Н5 – этилэтаноат; этилацетат; этиловый эфир уксусной кислоты; уксусноэтиловый эфир. С6Н5СООС2Н5 – этилбензоат; этиловый эфир
- 3. Физические свойства 1. Бесцветные летучие жидкости мало растворимые в воде; 2. Обладают приятным запахом; 3. Кипят
- 4. Нахождение в природе Аромат цветов Ягоды
- 5. Нахождение в природе Фрукты Мед, воск
- 6. ЖАСМИНОВЫЙ ЗАПАХ
- 7. ОРХИДЕЙНЫЙ ЗАПАХ
- 8. ХРИЗАНТЕМНЫЙ ЗАПАХ
- 9. Вишнёвый запах
- 10. Абрикосовый запах
- 11. Яблочный запах этил,3-метил-бутанат
- 12. Апельсиновый запах
- 13. ГРУШЕВЫЙ ЗАПАХ
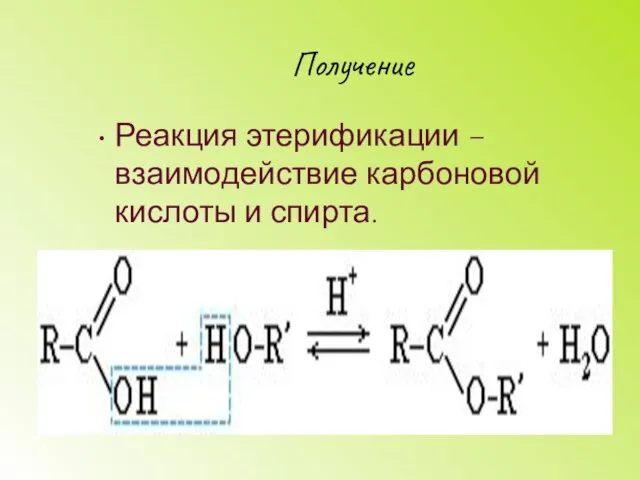
- 14. Получение Реакция этерификации – взаимодействие карбоновой кислоты и спирта.
- 15. Историческая справка Впервые сложный эфир был получен в 1759 году де Лаурагваисом при перегонке «крепкой уксусной
- 16. Химические свойства 1. Кислотный гидролиз Н+ СН3СООС2Н5 + НОН ↔ СН3СООН + С2Н5ОН 2. Щелочной гидролиз
- 17. Применение Растворители Парфюмерия
- 18. Применение Газированные напитки Лекарственные препараты
- 19. Вместо заключения Эти сложные эфиры Управляют целым миром. В барбариске и ириске, В мармеладке, в шоколадке,
- 20. Вопросы по теме «Сложные эфиры» 1. Какой класс органических соединений имеет такую же общую формулу как
- 21. Вопросы по теме «Сложные эфиры» 5. Имеются ли среди сложных эфиров газообразные соединения? 6. С чем
- 22. Занимательные вопросы 4. Как повествует Библия, пророк Моисей пас овец и видел, «что терновый куст горит
- 24. Скачать презентацию




















 Легенды и мифы звездного неба
Легенды и мифы звездного неба Созвездия и звёзды
Созвездия и звёзды Воева Наталья Михайловна, учитель начальных классов МАОУНОШ д. Дубовицы Старорусского района Новгородской области
Воева Наталья Михайловна, учитель начальных классов МАОУНОШ д. Дубовицы Старорусского района Новгородской области  Склад атмосфери та значення атмосферного тиску на планетах Сонячної системи
Склад атмосфери та значення атмосферного тиску на планетах Сонячної системи Межзвездное поглощение света
Межзвездное поглощение света ИЗУЧЕНИЕ ДИНАМИКИ СОЛНЕЧНОЙ СИСТЕМЫ НА ОСНОВЕ НАБЛЮДЕНИЙ Н. В. Емельянов
ИЗУЧЕНИЕ ДИНАМИКИ СОЛНЕЧНОЙ СИСТЕМЫ НА ОСНОВЕ НАБЛЮДЕНИЙ Н. В. Емельянов  Закони і формули в астрономії
Закони і формули в астрономії Астрономическая ботаника
Астрономическая ботаника Спутник-1. Первый искусственный спутник Земли, советский космический аппарат, запущенный на орбиту
Спутник-1. Первый искусственный спутник Земли, советский космический аппарат, запущенный на орбиту Астероидная опасность
Астероидная опасность Презентация по астрономии Законы Кеплера – законы движения небесных тел
Презентация по астрономии Законы Кеплера – законы движения небесных тел  Происхождение нашей Галактики
Происхождение нашей Галактики Проблема измерения времени в современной астрономии Исследовательская работа Выполнили: ученицы 11 "А" класса Голова Е.,
Проблема измерения времени в современной астрономии Исследовательская работа Выполнили: ученицы 11 "А" класса Голова Е., Планети земної групи. Планети земної групи — Меркурій, Венера, Земля і Марс
Планети земної групи. Планети земної групи — Меркурій, Венера, Земля і Марс  Вселенная. Как родилась вселенная
Вселенная. Как родилась вселенная Законы Кеплера - презентация по Астрономии скачать _
Законы Кеплера - презентация по Астрономии скачать _ Венера – вторая по удаленности от Солнца планета Солнечной системы
Венера – вторая по удаленности от Солнца планета Солнечной системы Планета Меркурий
Планета Меркурий Кастор
Кастор Строение Солнечной системы
Строение Солнечной системы Кометы - презентация по Астрономии скачать
Кометы - презентация по Астрономии скачать  Jules Henri Poincaré
Jules Henri Poincaré Венера
Венера Предмет и история космологии. Большой взрыв. Антропный принцип
Предмет и история космологии. Большой взрыв. Антропный принцип Сонце
Сонце Фридрих Бессель и звезда Лебедь, измерение
Фридрих Бессель и звезда Лебедь, измерение Детям о Космосе
Детям о Космосе Космос и его загадки - презентация по Астрономии скачать
Космос и его загадки - презентация по Астрономии скачать