Содержание
- 2. БИОЛОГИЧЕСКОЕ ОКИСЛЕНИЕ - это совокупность окислительных процессов в живом организме, протекающих с обязательным участием кислорода. Окисление
- 3. МИТОХОНДРИАЛЬНОЕ ОКИСЛЕНИЕ Мультиферментная система митохондриального окисления - система, постепенно транспортирующая протоны и электроны на кислород с
- 4. Только первый переносчик протонов и электронов – никотинамид (НАД+)-зависимая дегидрогеназа расположена в матриксе митохондрий. Этот фермент
- 5. Существует строгая последовательность работы каждого звена в цепочке переносчиков. Эта последовательность определяется величиной редокс-потенциала (окислительно-восстановительного потенциала)
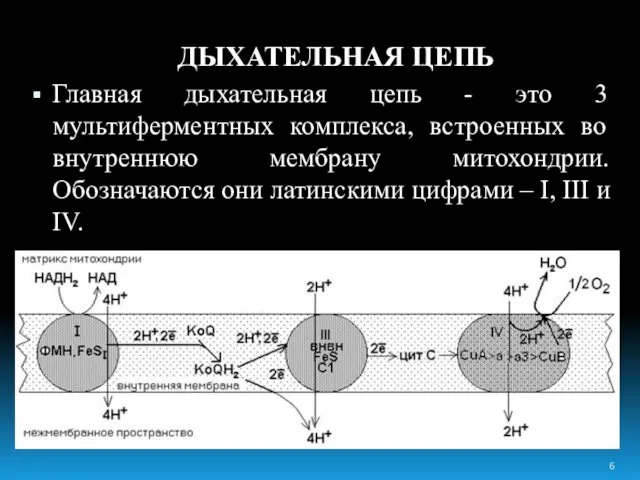
- 6. ДЫХАТЕЛЬНАЯ ЦЕПЬ Главная дыхательная цепь - это 3 мультиферментных комплекса, встроенных во внутреннюю мембрану митохондрии. Обозначаются
- 7. Комплекс I – НАДН-KoQ-редуктаза, комплекс III – KoQH2-редуктаза, комплекс IV – цитохромоксидаза. Есть ещё комплекс II
- 8. Эти комплексы транспортируют водород от никотинамидных дегидрогеназ на кислород воздуха, в результате чего создается электрохимический градиент
- 9. ЭНЕРГИЯ ΔμΗ+ ИСПОЛЬЗУЕТСЯ ДЛЯ СЛЕДУЮЩИХ ПРОЦЕССОВ: Синтез АТФ. Получение тепла (особенно важно для бурого жира и
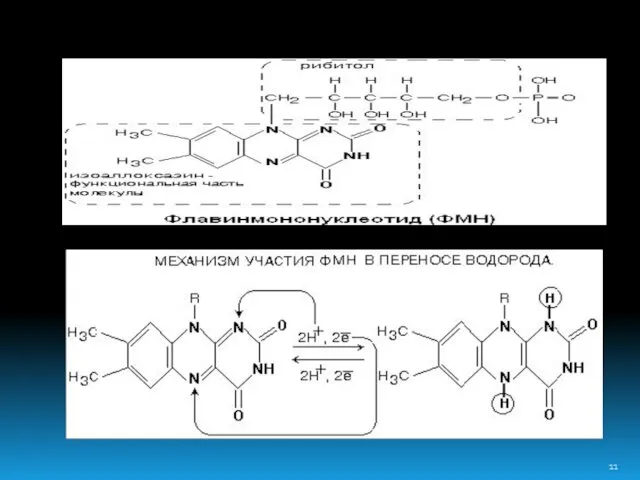
- 10. КОМПЛЕКС I В составе комплекса находится 26 полипептидных цепей общей массой 800 кДа. Комплекс содержит следующие
- 12. Одновременно с протонами по дыхательной цепи транспортируются и электроны. Наибольшие перепады редокс-потенциала наблюдаются между железо-серными белками,
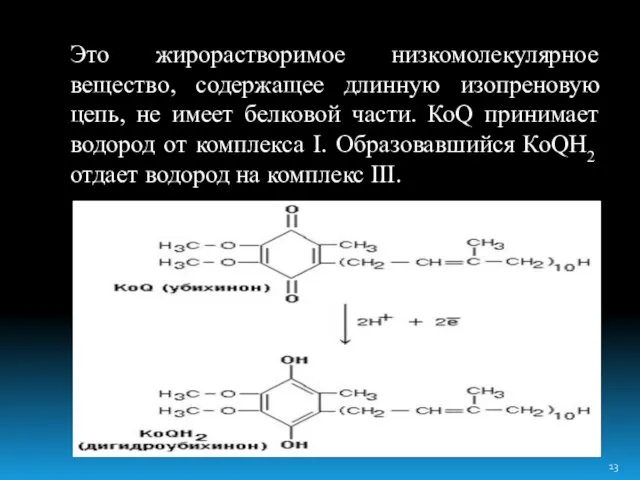
- 13. Это жирорастворимое низкомолекулярное вещество, содержащее длинную изопреновую цепь, не имеет белковой части. КоQ принимает водород от
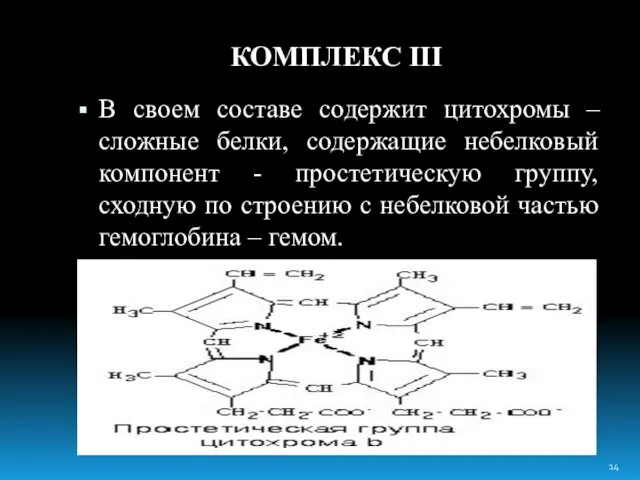
- 14. КОМПЛЕКС III В своем составе содержит цитохромы – сложные белки, содержащие небелковый компонент - простетическую группу,
- 15. Цитохромы b, имеющие в своем составе два типа простетических групп тетрапиррольной структуры - «гем». Известно два
- 16. КОМПЛЕКС IV От двух атомов водорода, которые переносятся от KoQ на комплекс III, дальше по цепи
- 17. Комплекс IV называется цитохромоксидазой. Он способен захватывать из матрикса 4 протона. Два из них он отправляет
- 18. Но на нескольких стадиях ее достаточно, чтобы синтезировать макроэргические связи в молекуле АТФ. Такими стадиями являются:
- 20. Скачать презентацию













 Тигры. Научное описание
Тигры. Научное описание Накопление загрязняющих веществ в пищевых цепях
Накопление загрязняющих веществ в пищевых цепях  Презентация на тему "Невероятные факты о животных" - скачать бесплатно презентации по Биологии
Презентация на тему "Невероятные факты о животных" - скачать бесплатно презентации по Биологии Иммунитет Виды иммунитета
Иммунитет Виды иммунитета  Будова вуха, слухового та стато-кінетичного аналізаторів
Будова вуха, слухового та стато-кінетичного аналізаторів Презентация по биологии Органы чувств. Анализаторы
Презентация по биологии Органы чувств. Анализаторы Птицы рядом с нами и вокруг нас
Птицы рядом с нами и вокруг нас НЕКЛЕТОЧНЫЕ ФОРМЫ ЖИЗНИ
НЕКЛЕТОЧНЫЕ ФОРМЫ ЖИЗНИ Биологиялық ырғақтар
Биологиялық ырғақтар Мастер-класс по теме: Метапредметные связи на уроках биологии
Мастер-класс по теме: Метапредметные связи на уроках биологии Возникновение и развитие жизни на Земле
Возникновение и развитие жизни на Земле Дополнительный_материал_09.06_24.01.2022_ef804d7e
Дополнительный_материал_09.06_24.01.2022_ef804d7e Тема урока: «Космическая роль зеленых растений. Решение задач с экологическим содержанием.»
Тема урока: «Космическая роль зеленых растений. Решение задач с экологическим содержанием.» Спланхнология
Спланхнология Презентация на тему Животные истребленные человеком
Презентация на тему Животные истребленные человеком  Биологиялық ырғақтар
Биологиялық ырғақтар Презентация на тему Строение и функции кожи
Презентация на тему Строение и функции кожи  Презентация на тему "Селекція" - скачать бесплатно презентации по Биологии
Презентация на тему "Селекція" - скачать бесплатно презентации по Биологии Биология – это комплекс наук, изучающих закономерности развития и жизнедеятельности живых систем, причины их многообразия и прис
Биология – это комплекс наук, изучающих закономерности развития и жизнедеятельности живых систем, причины их многообразия и прис Вомбати
Вомбати Спостереження за поведiнкою тварин
Спостереження за поведiнкою тварин Секреты здорового питания
Секреты здорового питания  Сравнительная морфология живых организмов
Сравнительная морфология живых организмов Семейства двудольных и однодольных
Семейства двудольных и однодольных Питание бактерий, грибов и животных
Питание бактерий, грибов и животных АНАТОМИЯ ОРГАНА ЗРЕНИЯ
АНАТОМИЯ ОРГАНА ЗРЕНИЯ  Сердце – главный орган кровеносной системы
Сердце – главный орган кровеносной системы Цветоведение
Цветоведение