Содержание
- 2. План лекции Ферменты – биологические катализаторы. Отличительные признаки ферментативного и химического катализа. Специфичность Природа катализа, теории
- 3. Использование ферментов человеком Сыроварение Дубление кожи Хлебопечение Молочнокислые продукты В Древнем Египте при строительстве пирамиды Хеопса
- 4. Значение брожения для приготовления и сохранения пищи Обогащение пищи разнообразием вкусов, ароматов и текстуры Сохранение пищи
- 5. ХVII век Жан Баптист ван Гельмонт (Jan Baptista van Helmont, 12 января 1580-30 декабря 1644)) голландский
- 6. XIX век. «Организованными ферментами» (от латинского fermentum — закваска)» Луи Пастер называл живые микроорганизмы. «Неорганизованными ферментами»
- 7. Эдуард Бухнер (20 мая 1860- 13 августа 1917 Через два года после смерти Л. Пастера в
- 8. ХХ век Впервые высокоочищенный кристаллический фермент (уреазу) выделил в 1926 году Джеймс Бетчеллер Самнер (James Batcheller
- 9. Рибозимы Каталитическую активность РНК в 1980-х годах впервые обнаружил Томас Роберт Чек (Thomas Robert Cech; 8
- 10. Определение Катализаторы – это вещества, которые влияют на скорость химической реакции, но сами при этом не
- 11. Общие свойства ферментов и небиологических катализаторов: 1) не входят в состав конечных продуктов реакции и не
- 12. Отличительные признаки ферментативного катализа: Скорость ферментативного катализа выше, чем небиологического. Ферменты обладают узкой избирательностью – специфичностью,
- 13. Специфичность действия Под субстратной специфичностью понимают способность фермента взаимодействовать с одним или несколькими определенными субстратами Различают:
- 14. Процесс катализа можно представить следующим уравнением: E + S ⇆ [ES] → [EР] → E +
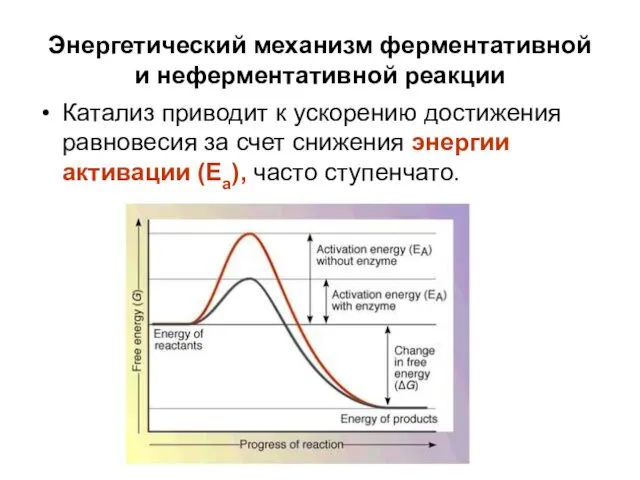
- 15. Энергетический механизм ферментативной и неферментативной реакции Катализ приводит к ускорению достижения равновесия за счет снижения энергии
- 16. Природа катализа В реакцию вступают молекулы, преодолевшие энергетический барьер и обладающие энергией активации Еа В переходном
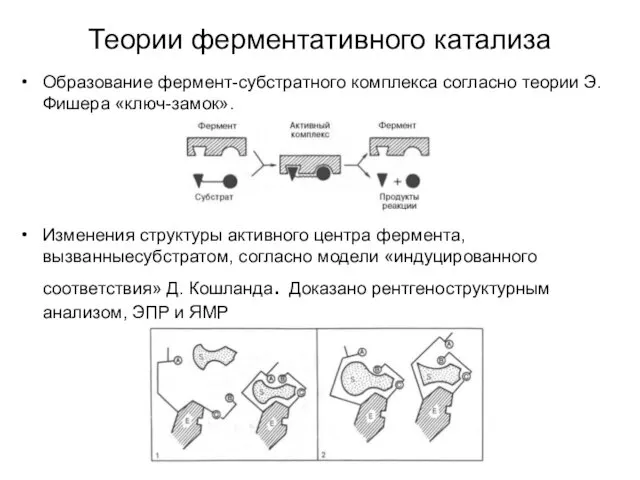
- 17. Теории ферментативного катализа Образование фермент-субстратного комплекса согласно теории Э. Фишера «ключ-замок». Изменения структуры активного центра фермента,
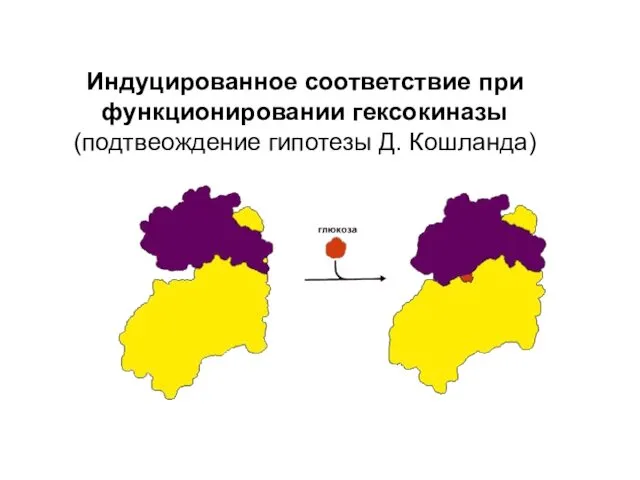
- 18. Индуцированное соответствие при функционировании гексокиназы (подтвеождение гипотезы Д. Кошланда)
- 19. Номенклатура и классификация ферментов была принята в 1961 г. после 6-летней работы Комиссии по ферментам Оксидоредуктазы
- 20. Название ферментов В соответствии с классификацией ферментов каждый фермент получил систематической название: название субстратов (через двоеточие),
- 21. Оксидоредуктазы катализируют реакции окисления-восстановления: Лактатдегидрогеназа (LDH, EC 1.1.1.27) катализирует превращение молочной кислоты (лактат) в пировиноградную (пируват)
- 22. Трансферазы Катализируют реакции переноса групп с одной молекулы на другую Холинацетилтрансфераза, ЕС 2.3.1.6, (систематическое название ацетил-КоА:
- 23. Гидролазы (фосфатазы, эстеразы, фосфолипазы) Катализируют реакции разрыва связей с присоединением воды Дипептидаза расщепляет дипептид на две
- 24. ЛИАЗЫ (альдолазы, гидратазы-дегидратазы, синтазы, декарбоксилазы) Катализируют реакции разрыва связей в субстрате без присоединения воды или окисления):
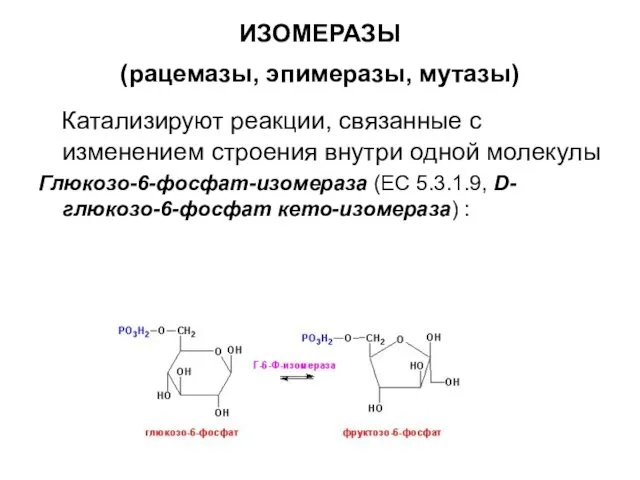
- 25. ИЗОМЕРАЗЫ (рацемазы, эпимеразы, мутазы) Катализируют реакции, связанные с изменением строения внутри одной молекулы Глюкозо-6-фосфат-изомераза (ЕС 5.3.1.9,
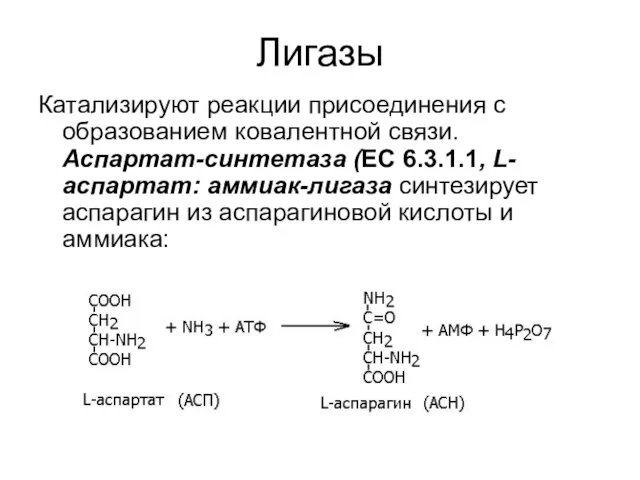
- 26. Лигазы Катализируют реакции присоединения с образованием ковалентной связи. Аспартат-синтетаза (ЕС 6.3.1.1, L-аспартат: аммиак-лигаза синтезирует аспарагин из
- 27. Номенклатура ферментов По классификации ферментов (КФ- русскоязычная, ЕС-англоязычная) каждый фермент (энзим) имеет свой определенный код, состоящий
- 28. Подклассы ферментов Внутри каждого класса происходит разделение на подклассы: EC 1.1 Действующие на CH-OH группы донора
- 29. Подподклассы ферментов Внутри каждого подкласса происходит разделение на подподклассы: EC 1.1.1 Акцептор NAD или NADP EC
- 30. Четвертая цифра – номер фермента Последнее число – номер конкретного фермента: EC 1.1.1.1 alcohol dehydrogenase EC
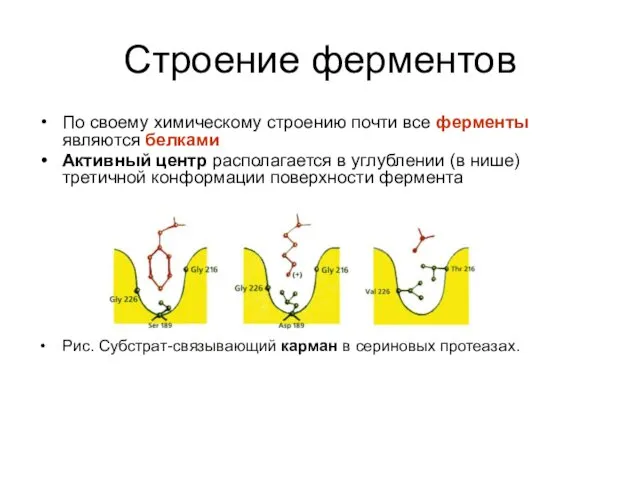
- 31. Строение ферментов По своему химическому строению почти все ферменты являются белками Активный центр располагается в углублении
- 32. Активный центр Активный центр фермента – это уникальная комбинация аминокислот, благодаря которой осуществляется его каталитическое действие.
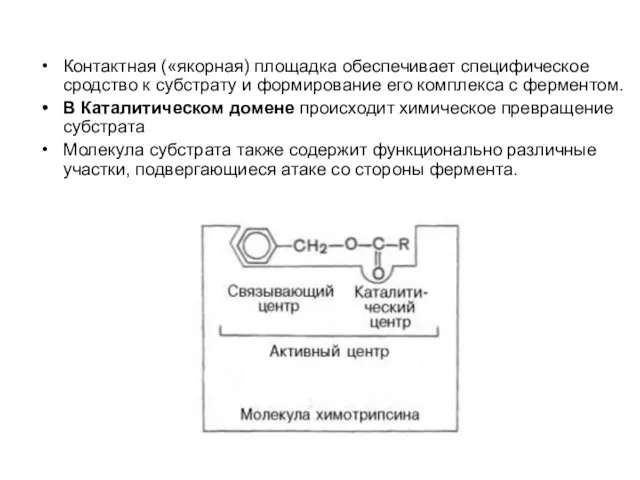
- 33. Контактная («якорная) площадка обеспечивает специфическое сродство к субстрату и формирование его комплекса с ферментом. В Каталитическом
- 34. В образовании фермент-субстратных комплексов участвуют водородные, электростатические (ионные) и гидрофобные взаимодействия, а также координационные связи Информация
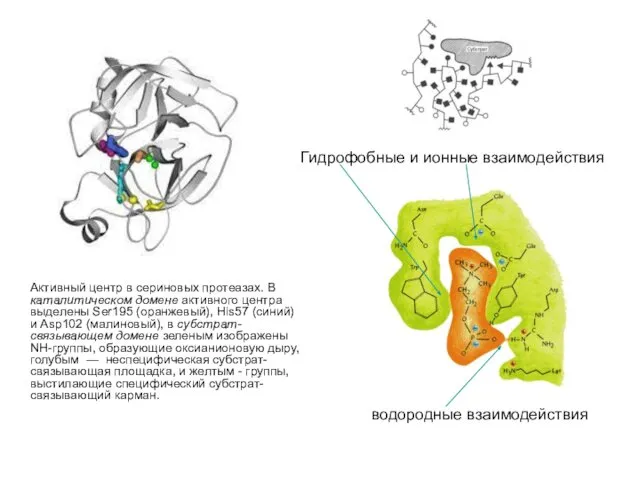
- 35. Активный центр в сериновых протеазах. В каталитическом домене активного центра выделены Ser195 (оранжевый), His57 (синий) и
- 36. Аллостерический центр («Аллос» – другой, «Steros» - пространственный), расположенный вдали от активного центра, специальный регуляторный центр
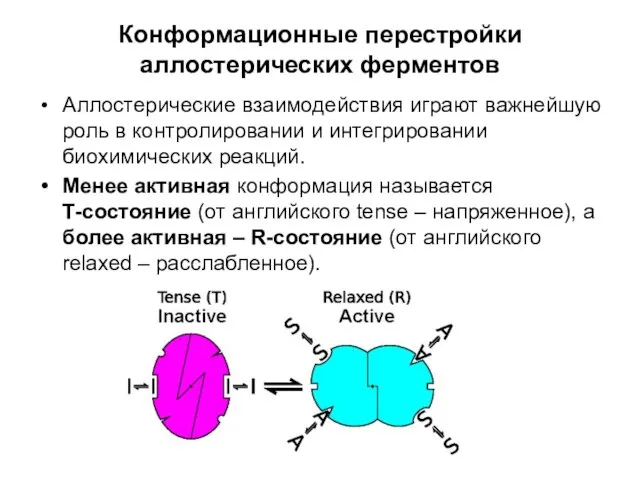
- 37. Конформационные перестройки аллостерических ферментов Аллостерические взаимодействия играют важнейшую роль в контролировании и интегрировании биохимических реакций. Менее
- 38. Строение сложных белков-ферментов Белковая часть фермента, называется апоферментом Небелковая часть сложного фермента, называется КОФЕРМЕНТОМ или кофактором
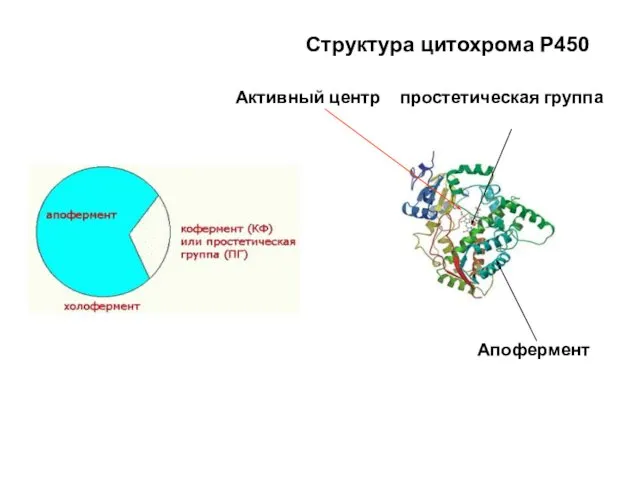
- 39. Структура цитохрома Р450 Активный центр простетическая группа Апофермент
- 40. Кофермент – термостабильное низкомолекулярное соединение, небелковая часть сложных белков-ферментов, без которых фермент не активен Кофакторы -
- 41. Функции коферментов Участие в акте катализа Осуществление связи между ферментом и субстратом Стабилизация апофермента Апофермент усиливает
- 42. Химическая природа коферментов К коферментам относят следующие соединения: Производные витаминов (пиридоксальфосфат) Гемы, являющиеся простетической группой цитохромов,
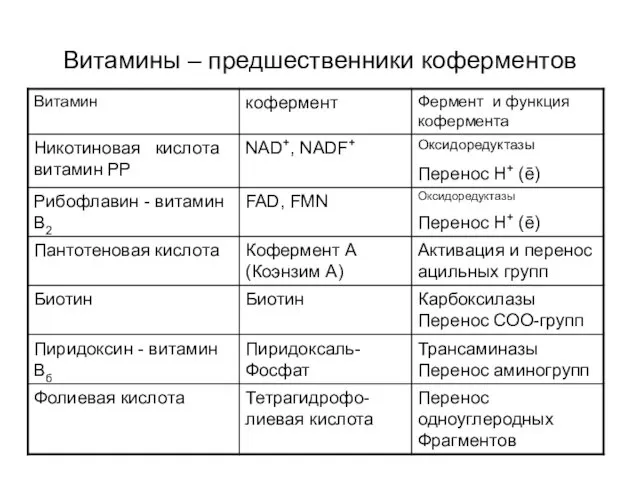
- 43. Витамины – предшественники коферментов
- 44. Изоферменты Изоферменты(изоэнзимы, изозимы) разные структурные формы ферментов, обладающие каталитической активностью одного типа; встречаются у организмов одного
- 45. Основы кинетики ферментативных реакций Кинетика ферментативных реакций – раздел энзимологии, который изучает зависимость скорости реакции от
- 46. Единицы каталитической активности фермента Каталитическая активность ферментов выражается в каталах и международных единицах (МЕ): 1 кат
- 47. Полный математический анализ ферментативной реакции приводит к сложным уравнениям, не пригодным для практического применения. Наиболее удобной
- 48. Ферментативный процесс можно выразить следующим уравнением: где k1 – константа скорости образования [ES] k-1 – константа
- 49. Зависимость скорости ферментативной реакции от концентрации субстрата выражается следующим уравнением (математическое выведение этой формулы можно найти
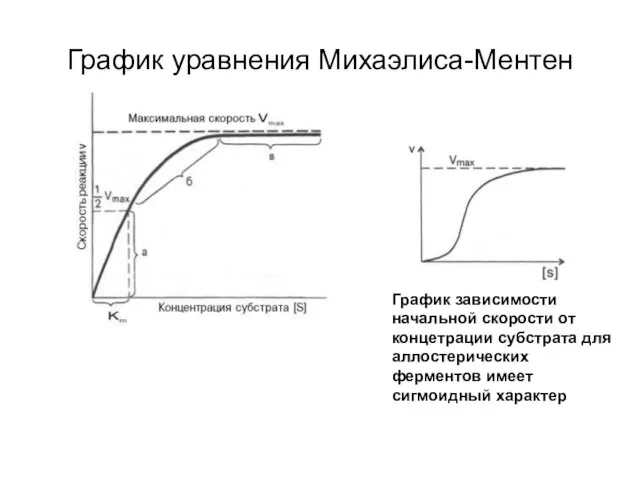
- 50. График уравнения Михаэлиса-Ментен График зависимости начальной скорости от концетрации субстрата для аллостерических ферментов имеет сигмоидный характер
- 51. Определение Vmax и Km При [S] V = Vmax•[S]/km = k •[S], т.е. при очень низких
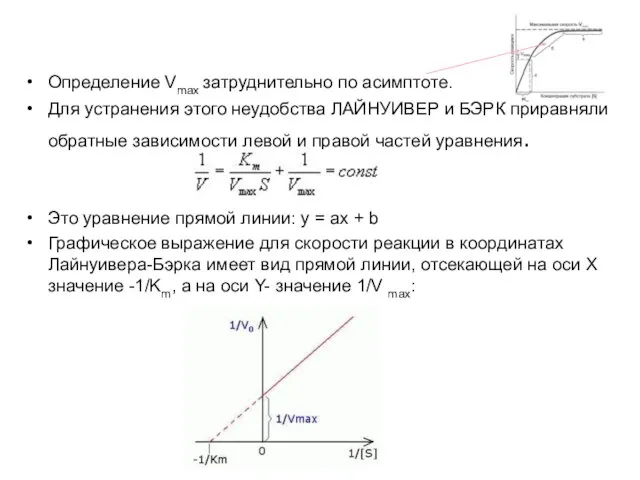
- 52. Определение Vmax затруднительно по асимптоте. Для устранения этого неудобства ЛАЙНУИВЕР и БЭРК приравняли обратные зависимости левой
- 53. Термолабильность ферментов Температурный коэффициент Q10 показывает во сколько раз ускоряется скорость реакции при повышении температуры на
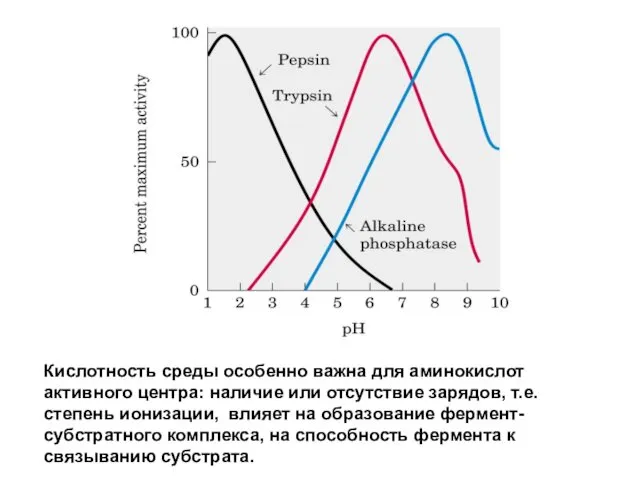
- 54. Кислотность среды особенно важна для аминокислот активного центра: наличие или отсутствие зарядов, т.е. степень ионизации, влияет
- 55. Зависимость активности ферментов от рН среды рН-оптимум действия ферментов лежит в пределах физиологических значений. Исключение составляет
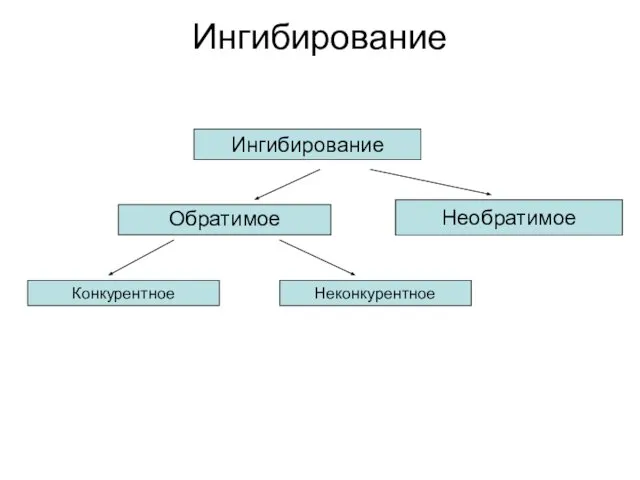
- 56. Ингибирование Ингибирование Обратимое Необратимое Конкурентное Неконкурентное
- 57. Необратимое ингибирование Ферменты являются белками, поэтому любые агенты, вызывающие денатурацию белка (кислоты, щелочи, соли тяжелыхи металлов,
- 58. Обратимое ингибирование Специфические ингибиторы вызывают обратимое ингибирование и поддаются количественному изучению на основе уравнения Михаэлиса-Ментен. Обратимое
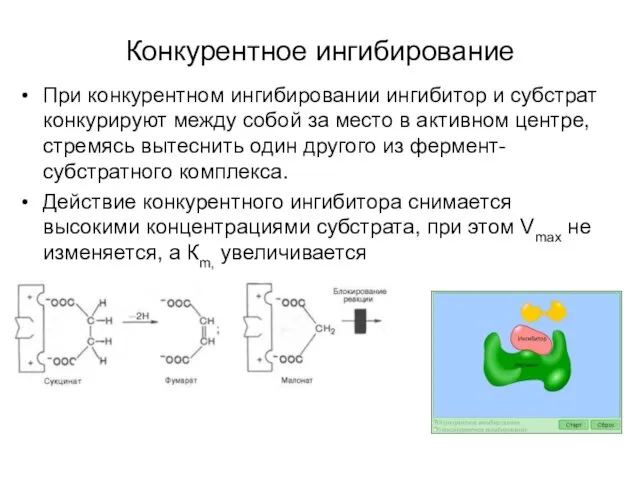
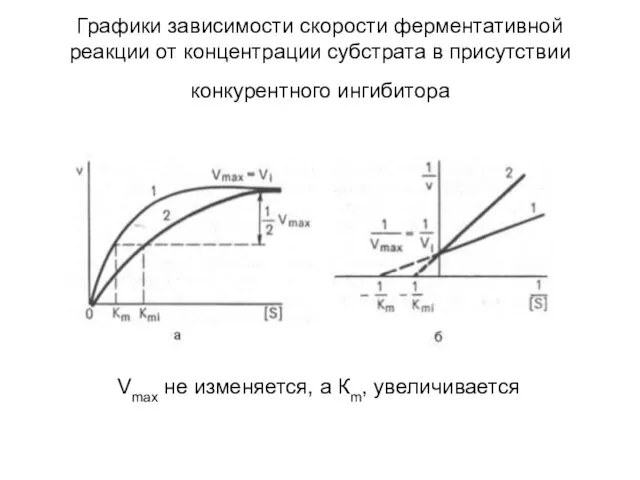
- 59. Конкурентное ингибирование При конкурентном ингибировании ингибитор и субстрат конкурируют между собой за место в активном центре,
- 60. Графики зависимости скорости ферментативной реакции от концентрации субстрата в присутствии конкурентного ингибитора Vmax не изменяется, а
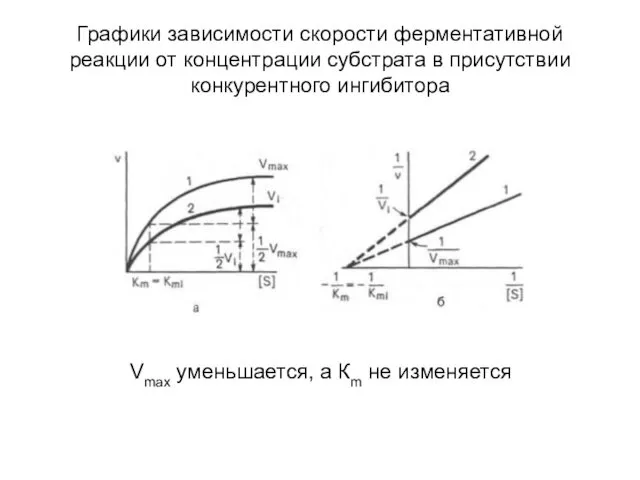
- 61. Неконкурентное ингибирование Неконкурентное ингибирование вызывается веществами, не имеющими структурного сходства с субстратами и часто связывающимися не
- 62. Графики зависимости скорости ферментативной реакции от концентрации субстрата в присутствии конкурентного ингибитора Vmax уменьшается, а Кm
- 63. Лекарственные препараты как ингибиторы Прозерин и эндрофоний – ингибиторы холинэстеразы используют при лечении мышечной дистрофии (нейромедиатор
- 64. Регуляция активности ферментов Ковалентная модификация – частичный протеолиз: зимогены - пепсиноген Нековалентная модификация: фосфорилирование-дефосфорилирование – гликогенфосфорилаза
- 65. Принципы энзимодиагностики Концентрация внутриклеточных (тканевых) ферментов в крови увеличивается при поврежден клеток: АСТ, АЛТ – гепатит;
- 66. Применение ферментных препаратов в медицине При заболеваниях ЖКТ: мезим-форте, фестал, энзистал, панкреатин При иммунодефицитах: вобэнзим Протеолитические
- 68. Скачать презентацию












![Процесс катализа можно представить следующим уравнением: E + S ⇆ [ES]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/496290/slide-13.jpg)
























![Определение Vmax и Km При [S] V = Vmax•[S]/km = k](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/496290/slide-50.jpg)









 Рыбный промысел и охота в Самарском крае в XVII-XVIII веке
Рыбный промысел и охота в Самарском крае в XVII-XVIII веке Презентация на тему "Генетические опыты Менделя" - скачать бесплатно презентации по Биологии
Презентация на тему "Генетические опыты Менделя" - скачать бесплатно презентации по Биологии Таблица генетического кода иРНК
Таблица генетического кода иРНК Половое и бесполое размножение Обобщение
Половое и бесполое размножение Обобщение Экологические законы природопользования Выполнила ученица 10 класса «а» Средней школы пгт Ярославский Дубовая Виктория
Экологические законы природопользования Выполнила ученица 10 класса «а» Средней школы пгт Ярославский Дубовая Виктория Паразитология
Паразитология Функции живого вещества
Функции живого вещества Күйісті мал қоректенуіндегі месқарын метаболизмі
Күйісті мал қоректенуіндегі месқарын метаболизмі Экологические факторы, действующие в почве: гуминовые вещества с точки зрения биологии
Экологические факторы, действующие в почве: гуминовые вещества с точки зрения биологии Майстерність маскування
Майстерність маскування Meiosis. (Chapter 7.1)
Meiosis. (Chapter 7.1) Презентация по биологии Биогеоценоз
Презентация по биологии Биогеоценоз  Презентация на тему Классификация животных основные систематические группы
Презентация на тему Классификация животных основные систематические группы  Лекция 6.
Лекция 6. Лекарственные растения
Лекарственные растения Автор: учитель биологии высшей категории МОУ «Засосенская СОШ имени Героя Советского Союза Н.Л.Яценко» Ковшов Анатолий Влад
Автор: учитель биологии высшей категории МОУ «Засосенская СОШ имени Героя Советского Союза Н.Л.Яценко» Ковшов Анатолий Влад Дыхательная система человека
Дыхательная система человека Pet the coo
Pet the coo Домашние и дикие животные
Домашние и дикие животные Презентация Химические загрязнения среды промышленностью
Презентация Химические загрязнения среды промышленностью  РІДКІСНІ ТА ЗНИКАЮЧІ ВИДИ РОСЛИН І ТВАРИН Підготувала учениця 11-ВГ класу Чугунова Ірина
РІДКІСНІ ТА ЗНИКАЮЧІ ВИДИ РОСЛИН І ТВАРИН Підготувала учениця 11-ВГ класу Чугунова Ірина  Грибы-паразиты. Тест
Грибы-паразиты. Тест Решение задач по теме Генетический код
Решение задач по теме Генетический код Презентацию составила Е.В. Потапенко, воспитатель ГПД 2011г. – 2012г.
Презентацию составила Е.В. Потапенко, воспитатель ГПД 2011г. – 2012г.  Хочу всё знать. КВН по окружающему миру для 4 класса
Хочу всё знать. КВН по окружающему миру для 4 класса День кошек ( средняя группа)
День кошек ( средняя группа) Насекомые
Насекомые Моллюски. Удивительные существа
Моллюски. Удивительные существа