Содержание
- 2. Лекция № 6 Энтропия и вероятность. 1. Статистический вес макросостояния. 2. Формула Больцмана для энтропии равновесного
- 3. Статистический смысл энтропии Посмотрим на энтропию с другой стороны. Более глубокий смысл энтропии вскрывается в статистической
- 4. Термодинамическая вероятность состояния системы - это число способов, которыми может быть реализовано данное состояние макроскопической системы,
- 5. Макросостояние – это состояние вещества, характеризуемое его термодинамическими парамет-рами (объемом, давлением, температурой и т. д.) .
- 6. Так как молекулы движутся хаотически, то имеется много микросостояний, соот-ветствующих одному макросостоянию. Обозначим Ω − число
- 7. Термодинамической вероятностью или статистическим весом Ω макросостояния − называется число перестановок одноименных элементов, при которых сохраняется
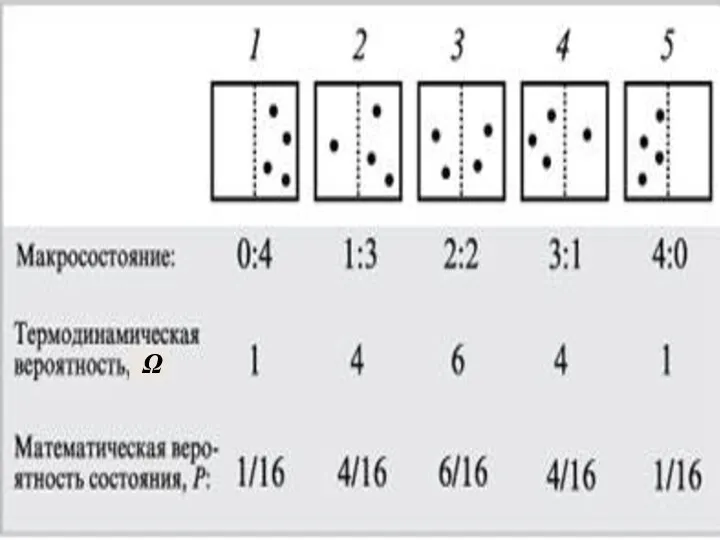
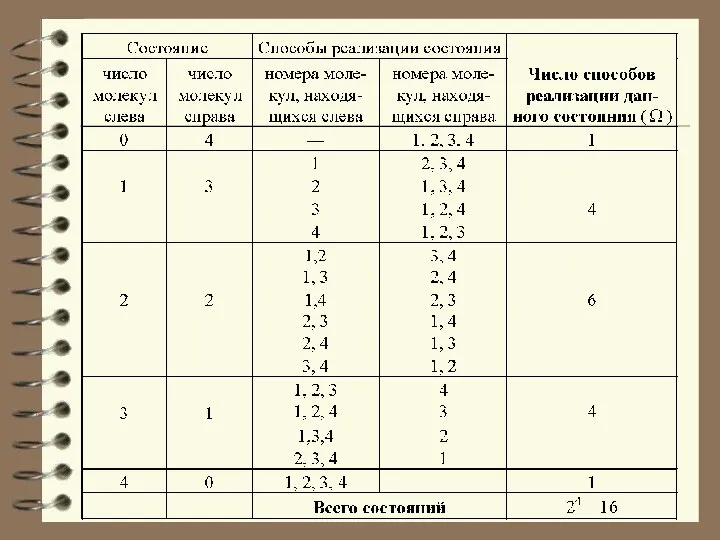
- 8. Чтобы пояснить понятие статистичес-кого веса (термодинамической вероят-ности), рассмотрим способы, которыми молекулы газа могут распределиться между двумя
- 10. Ω
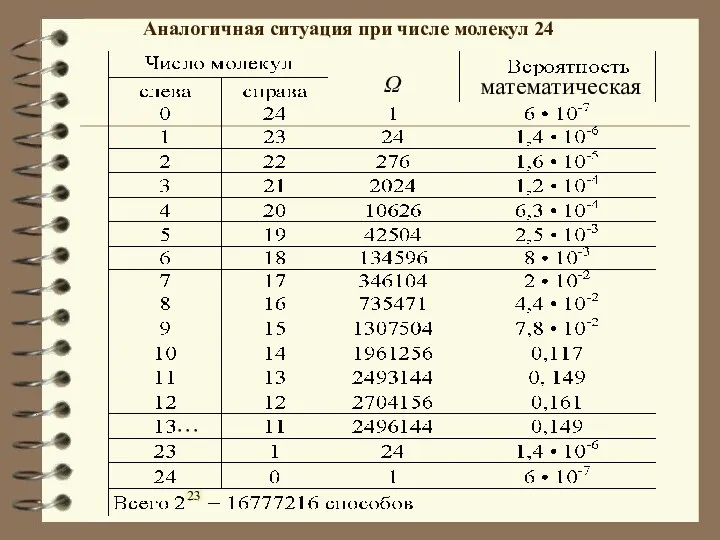
- 12. Аналогичная ситуация при числе молекул 24 математическая 23 … Ω
- 13. Обратный процесс, в результате которого газ самопроизвольно собрался бы в одной из половин сосуда, невозможен. Это
- 14. Из сказанного следует, что для того чтобы определить, какие процессы могут протекать в изолированной термодинамической системе,
- 15. Изолированная система будет самопроизвольно переходить из менее вероятных в более вероятные состояния либо преимущественно находиться в
- 16. 1
- 17. Статистический вес Ω обычно выражается огромными числами. Так, например, для одного моля кислорода при атмосферном давлении
- 18. В основе статистической физики лежит предположение о том, что все микросостояния данной термодина-мической системы равновероятны. Отсюда
- 19. Эргодическая гипотеза заключается в утверждении, что все микросостояния данной термодинамической системы равновероятны. Следовательно, веро-ятность макросостояния пропорцио-нальна
- 20. Предположим, что эти подсистемы находятся в состояниях с весами и Каждое из микросостояний первой подсистемы может
- 21. Но оказывается свойством аддитивности обладает логарифм статистического веса. А иметь дело с аддитивными величинами много проще
- 22. В связи с этим в качестве характеристики вероятности состояния системы принимается величина: называемая энтропией системы. Определенная
- 23. В экспериментальной физике от величины переходят к величине , которая также называется энтропией: Для одного моля
- 24. Согласно Больцману, энтропия системы и термодинамическая вероятность связаны между собой следующим образом (формула Больцмана): где k
- 25. В состоянии равновесия в термодинамике и вероятность максимальна и энтропия максимальна. Из этого можно сделать вывод,
- 26. Связь между S и Ω позволяет несколько иначе сформулировать второе начало термодинамики: всякий процесс в природе
- 27. Второе начало надо понимать так, что если система находится в каком-то состоянии с данной энтропией, то
- 28. Второе начало термодина-мики есть статистический закон, согласно которому отступления от термодинами-ческого равновесия – флуктуации – не
- 29. Энтропия – вероятностная статисти-ческая величина. Утверждение о возрастании энтропии потеряло свою категоричность. Её увеличение вероятно, но
- 30. Энтропия выступает, как мера беспорядочности, хаотичности состояния. Например, в ящике сиреневые и белые шары. Они порознь,
- 31. Клаузиус в 1867 г. выдвинул гипотезу о тепловой смерти Вселенной. Л. Больцман один из первых опроверг
- 32. Российские физики Я.Б. Зельдович и И.Д. Новиков, так же опровергли эту теорию, и показали, что Р.
- 33. При стремлении температуры к абсолют-ному нулю ( Т= 0 К ) уменьшается хаотич-ность системы. В пределе
- 34. Принцип Нернста был развит Планком, предположившим, что при абсолютном нуле температуры энергия системы минимальна (но не
- 36. Основные свойства энтропии: 1. Энтропия является функцией состояния. Для вычисления энтропии системы в дан-ном состоянии относительно
- 37. 5. Максимальное значение энтропии соот-ствует равновесное состояние. 6. Энтропия непосредственно связана с вероятностью: . Возрастание энтропии
- 38. Уве Бремер «Возрастающая энтропия»
- 39. Виктор Бурмин «Энтропия в пространстве не ограниченная во времени»
- 40. Далеко не всегда система находится в сос-тоянии термодинамического равновесия. Если температура системы в разных точка неодинакова,
- 41. Явления переноса в газах Молекулы в газе движутся со скоростью звука, с такой же скоростью движется
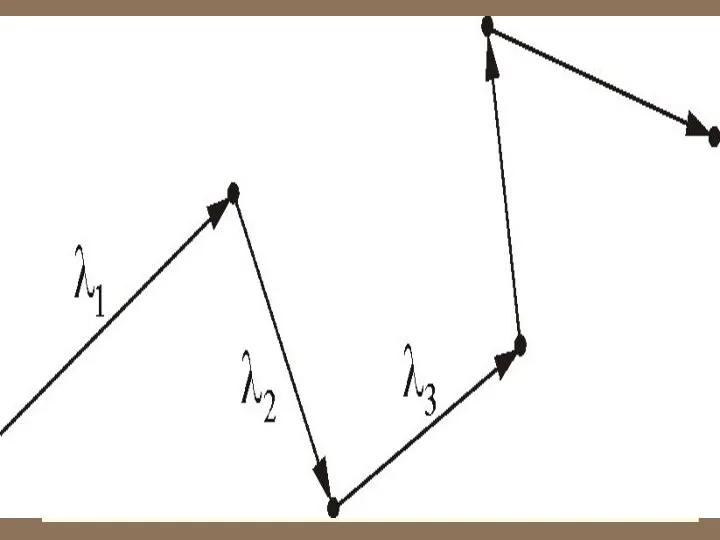
- 43. Число столкновений и средняя длина свободного пробега молекул в газах Обозначим – длина свободного пробега молекулы.
- 44. Расстояние, проходимое молекулой в среднем без столкнове-ний, называется средней длиной свободного пробега: – средняя скорость теплового
- 45. Модель идеального газа – твёрдые шарики одного диаметра, взаимодействующие между собой только при столкновении. Обозначим σ
- 46. – эффективное сечение молекулы – площадь в которую не может проникнуть центр любой другой молекулы. d
- 47. За одну секунду молекула проходит путь, равный средней арифметической скорости. За ту же секунду молекула претерпевает
- 48. Подсчитаем число столкновений ν. Вероятность столкновения трех и более молекул бесконечно мала. Предположим, что все молекулы
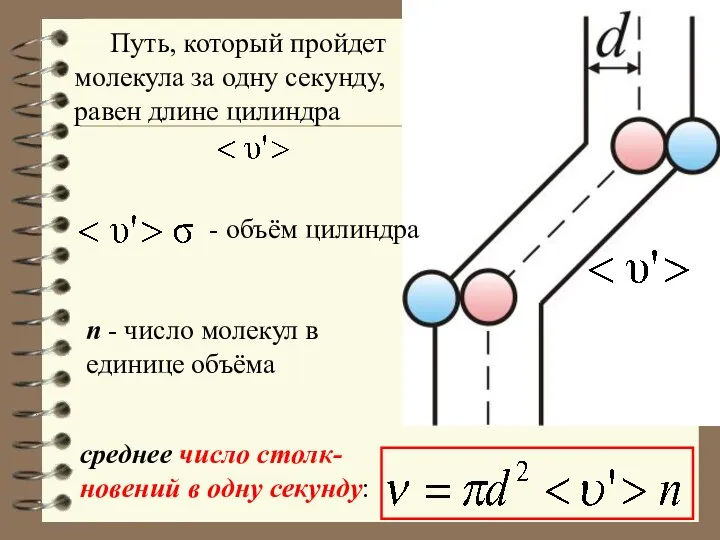
- 49. Путь, который пройдет молекула за одну секунду, равен длине цилиндра - объём цилиндра n - число
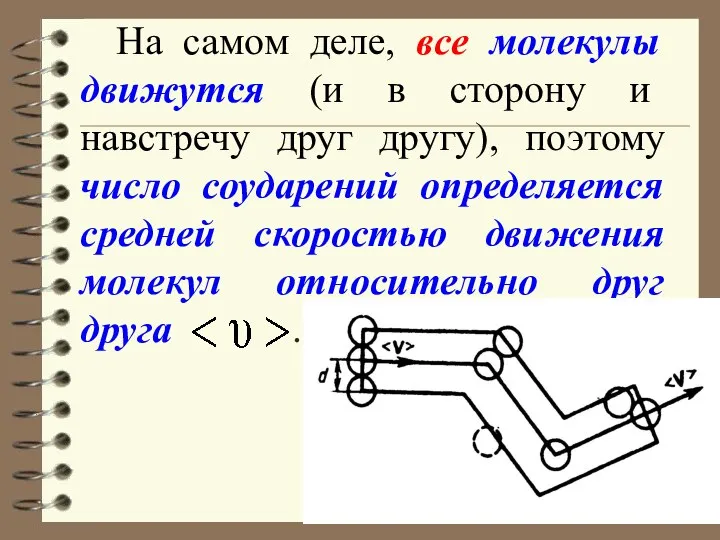
- 50. На самом деле, все молекулы движутся (и в сторону и навстречу друг другу), поэтому число соударений
- 51. По закону сложения случайных величин: Так как - средняя длина свободного пробега Тогда:
- 52. Из уравнения состояния идеального газа выразим n через давление P и температуру Т Так как ,
- 53. Таким образом, при заданной температуре, средняя длина свободного пробега обратно пропорциональна давлению Р: Например: d =
- 56. Скачать презентацию















































 Изотопная геология (введение)
Изотопная геология (введение) Диэлектрические потери
Диэлектрические потери Импульс, энергия, законы сохранения. Решение задач
Импульс, энергия, законы сохранения. Решение задач Классификация методов синтеза наноматериалов
Классификация методов синтеза наноматериалов Презентація з фізичного практикуму на тему:”Фізика й науково-технічний прогрес” підготувала: учениця 11-А класу Харківської ЗОШ І-ІІІ ст №102 Антіпова Марія
Презентація з фізичного практикуму на тему:”Фізика й науково-технічний прогрес” підготувала: учениця 11-А класу Харківської ЗОШ І-ІІІ ст №102 Антіпова Марія  Презентация по физике "Напряжение" - скачать
Презентация по физике "Напряжение" - скачать  Зубчатые передачи
Зубчатые передачи Нагревание проводников электрическим током. Закон Джоуля-Ленца
Нагревание проводников электрическим током. Закон Джоуля-Ленца Штормгласс - предсказатель бурь
Штормгласс - предсказатель бурь Передача и использование электроэнергии
Передача и использование электроэнергии Электрическое поле. (лекция 1а)
Электрическое поле. (лекция 1а) Механическое движение и его виды
Механическое движение и его виды Действие магнитного поля на проводник с током. Электрический двигатель
Действие магнитного поля на проводник с током. Электрический двигатель Физические основы термодинамики
Физические основы термодинамики Теплопроводность при наличии внутренних источников теплоты
Теплопроводность при наличии внутренних источников теплоты Ультразвук и инфразвук в природе
Ультразвук и инфразвук в природе Вес воздуха. Атмосферное давление. Выполнил: студент 4 курса Специальность физика Д.Е. Таргоний
Вес воздуха. Атмосферное давление. Выполнил: студент 4 курса Специальность физика Д.Е. Таргоний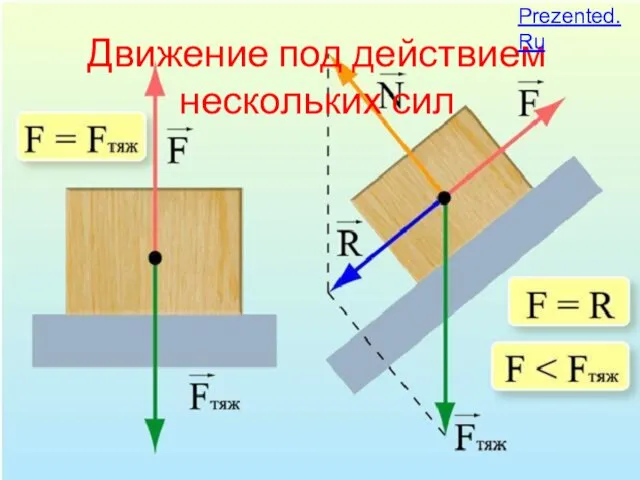 Движение под действием нескольких сил
Движение под действием нескольких сил Современные проблемы технической физики. Самые дорогие научные проекты
Современные проблемы технической физики. Самые дорогие научные проекты Макс Карл Эрнст Людвиг Планк (23.05.1858-04.10.1947)
Макс Карл Эрнст Людвиг Планк (23.05.1858-04.10.1947) Лабораторные работы по физике 8 класс
Лабораторные работы по физике 8 класс Принципы радиосвязи. (8 класс)
Принципы радиосвязи. (8 класс) Индикаторлық галоидты жанарғы
Индикаторлық галоидты жанарғы Электрическое поле
Электрическое поле ПРОЕКТ «Определение средней скорости моего движения.» Выполнил ученик 7Б класса
ПРОЕКТ «Определение средней скорости моего движения.» Выполнил ученик 7Б класса  Светодиодные лампы
Светодиодные лампы Внутренняя энергия. Термодинамика
Внутренняя энергия. Термодинамика Термодинамика поверхностных явлений. (Часть 2)
Термодинамика поверхностных явлений. (Часть 2)