Содержание
- 2. Состояние газа определяют Температура (T) Давление (P) Объём (V) Количество вещества равно 1 моль
- 3. ИЗОТЕРМИЧЕСКИЙ ПРОЦЕСС. «терма» - баня, промывочная (греч.)
- 4. Ро́берт Бойль — англо-ирландский натурфилософ, физик, химик и богослов. Седьмой сын Ричарда Бойля, 1-го графа Коркского,
- 5. Для газа данной массы произведение давления газа на его объем постоянно, если температура газа не меняется.
- 6. Закон Бойля-Мариотта
- 7. ИЗОБАРНЫЙ ПРОЦЕСС. «барос» - тяжесть, вес (греч.)
- 8. Жозе́ф Луи́ Гей-Люсса́к (6 декабря 1778, Сен-Леонар-де-Нобла — 9 мая 1850, Париж) — французский химик и
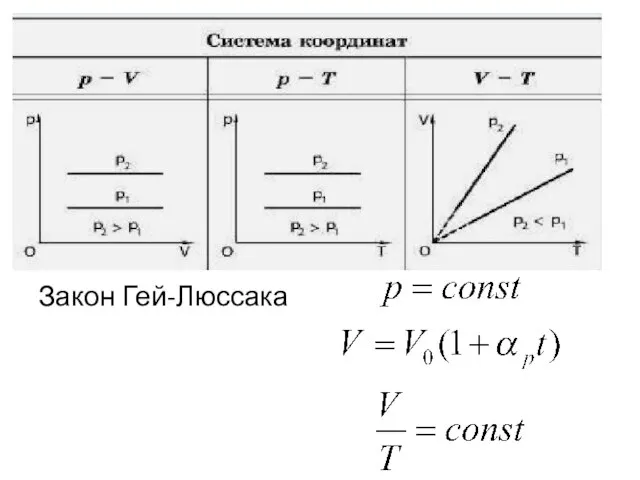
- 9. Для газа данной массы отношение объема к температуре постоянно, если давление газа не меняется.
- 10. Закон Гей-Люссака
- 11. ИЗОХОРНЫЙ ПРОЦЕСС. «хорема» - вместимость (греч.)
- 12. Жак Алекса́ндр Сеза́р Шарль (12 ноября 1746, Божанси, Луаре — 7 апреля 1823, Париж) — французский
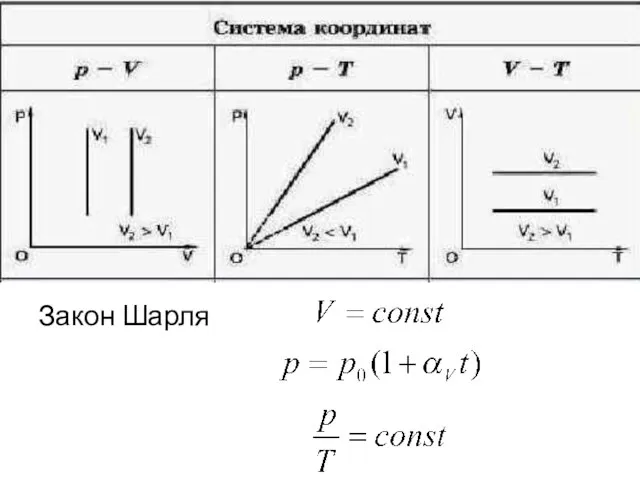
- 13. Для газа данной массы отношение давления к температуре постоянно, если объем газа не меняется.
- 14. Закон Шарля
- 15. Бенуа́ Поль Эми́ль Клапейро́н (26 февраля1799, Париж - 28 января 1864, Париж) –французский физик и инженер.
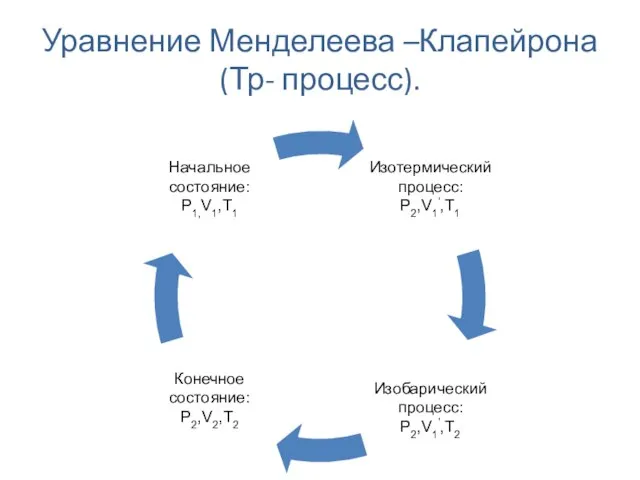
- 16. Уравнение Менделеева –Клапейрона (Тр- процесс).
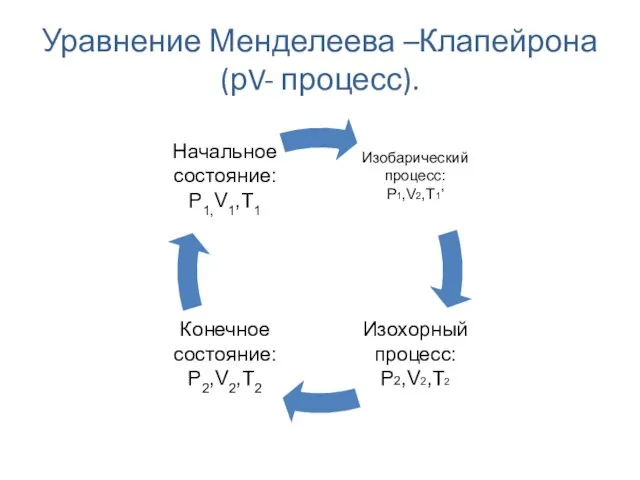
- 19. Уравнение Менделеева –Клапейрона (рV- процесс).
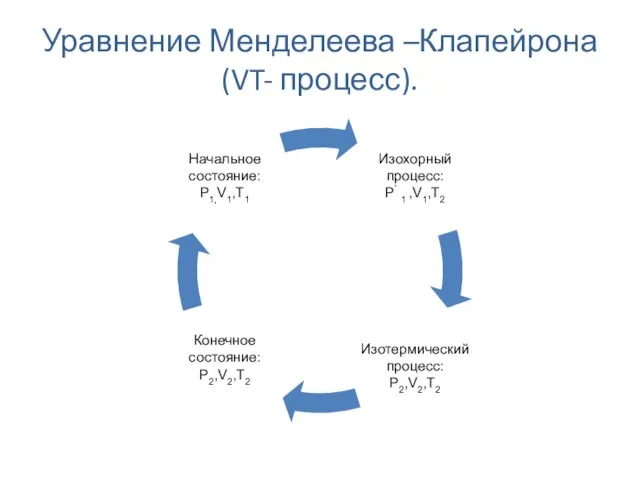
- 22. Уравнение Менделеева –Клапейрона (VT- процесс).
- 25. Уравнение Клайперона. Для любых переходов из состояния p1,V1, T1 в состояние p2 ,V2 ,T2 имеем
- 26. Дмитрий Иванович Менделеев (27 января 1834 - 20 января 1907) -русский ученый, энциклопедист, химик, метролог, экономист,
- 27. Постоянная Менделеева. Универсальная газовая постоянная, численно равная работе одного моля идеального газа при изобарическом нагревании на
- 28. Уравнение Менделеева -Клайперона.
- 29. Уравнение состояния газа.
- 31. Скачать презентацию












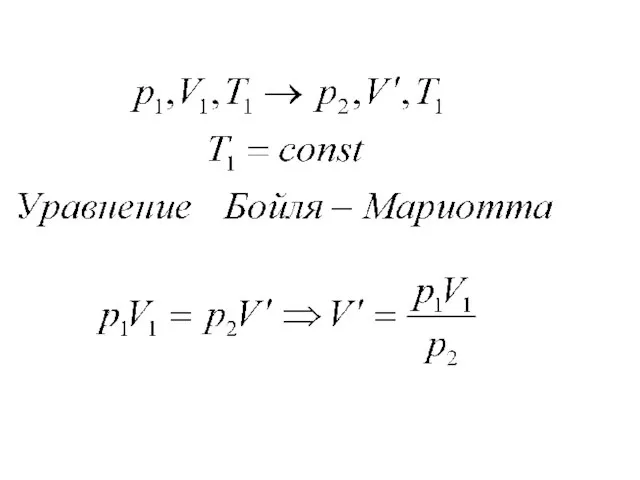
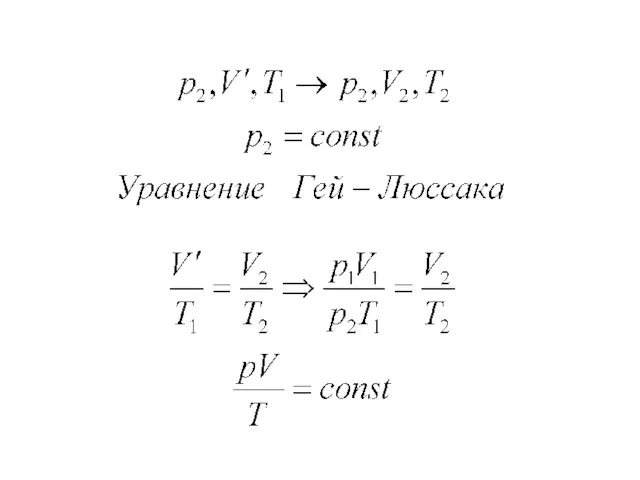
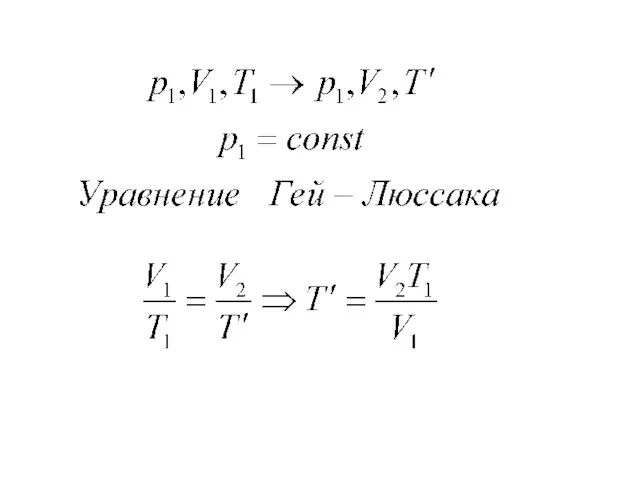
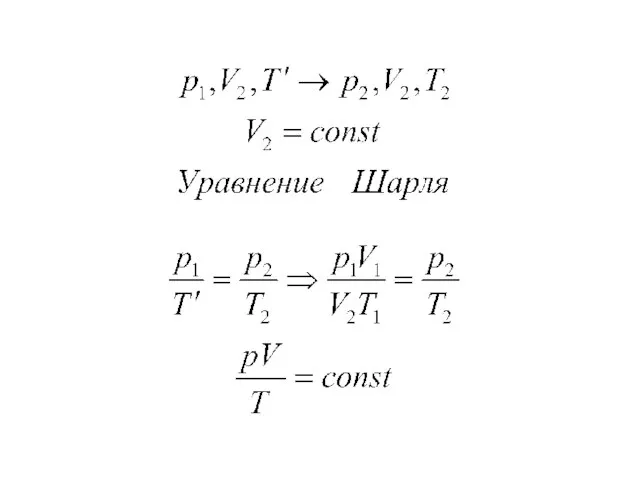
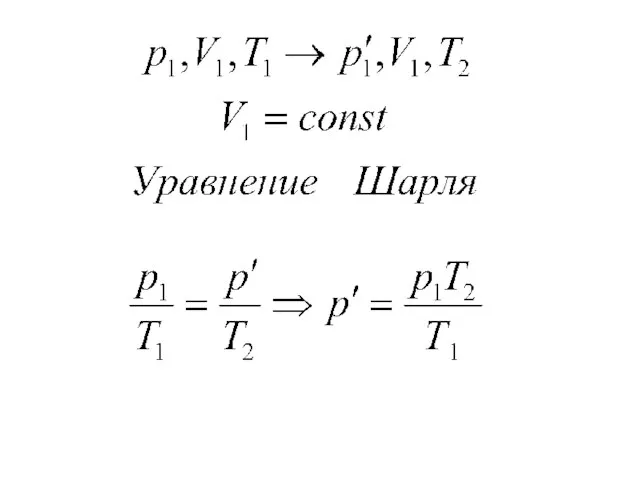
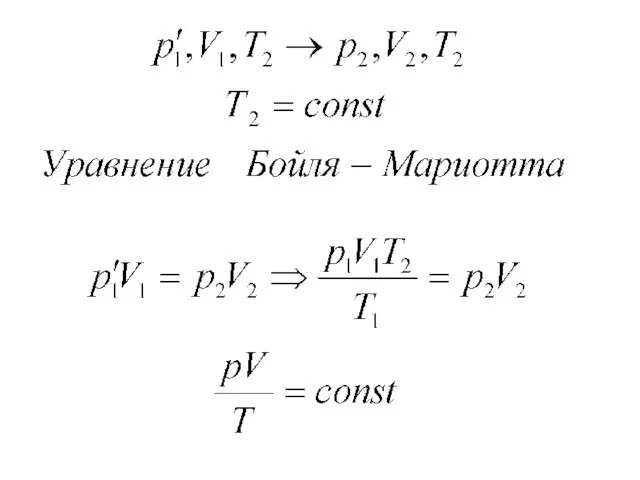





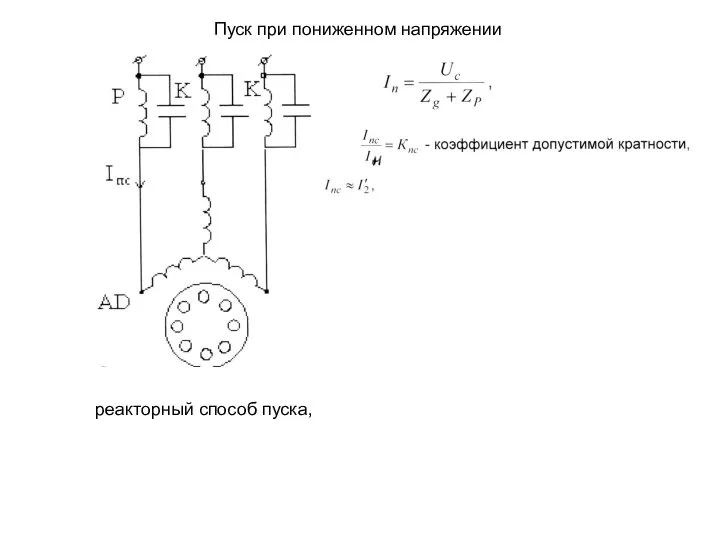 Пуск при пониженном напряжении. Реакторный способ пуска. (Лекция 9)
Пуск при пониженном напряжении. Реакторный способ пуска. (Лекция 9) Приборы для измерения давления
Приборы для измерения давления Влияние шума на организм человека
Влияние шума на организм человека Исключение выпадения конденсата на внутренней поверхности ОК
Исключение выпадения конденсата на внутренней поверхности ОК Рівноприскорений рух. Прискорення. Рівняння рівноприскореного руху
Рівноприскорений рух. Прискорення. Рівняння рівноприскореного руху Наблюдение за горящей свечой. Практическая работа
Наблюдение за горящей свечой. Практическая работа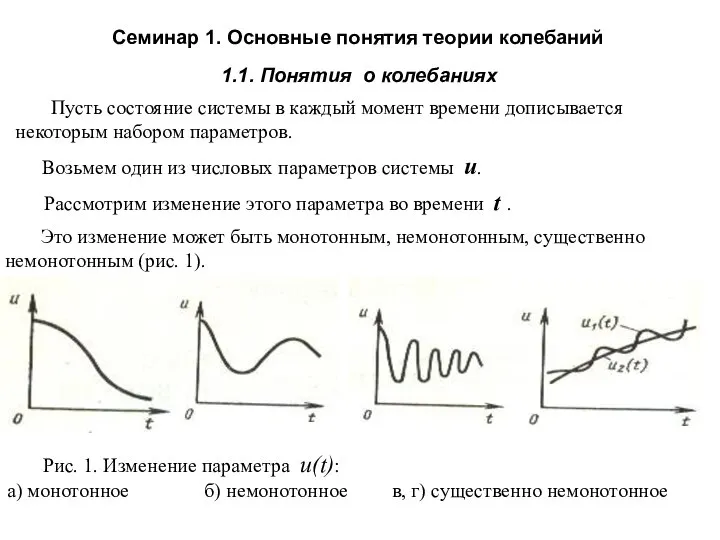 Основные понятия теории колебаний
Основные понятия теории колебаний Тема. Водородная связь
Тема. Водородная связь Работа. Мехническая энергия. Кинетическая и потенциальная энергия. Закон сохранения механической энергии
Работа. Мехническая энергия. Кинетическая и потенциальная энергия. Закон сохранения механической энергии Традиционные источники энергии. Достоинства и недостатки Работу выполнил: ученица 10 класса Елагина М.В. 2012 год. Проверила: Ва
Традиционные источники энергии. Достоинства и недостатки Работу выполнил: ученица 10 класса Елагина М.В. 2012 год. Проверила: Ва Оптические явления в природе
Оптические явления в природе Гидростатиканың негізгі теңдеуі
Гидростатиканың негізгі теңдеуі Электропроводность. Плотность полного электрического тока
Электропроводность. Плотность полного электрического тока Проект по физике на тему: «Экология, энергетика, человек» Выполнил: Анцупов Егор, 10 «А», Гимназия № 201, г. Москва. Руководител
Проект по физике на тему: «Экология, энергетика, человек» Выполнил: Анцупов Егор, 10 «А», Гимназия № 201, г. Москва. Руководител Нейтронная терапия как метод лечения онкологических заболеваний
Нейтронная терапия как метод лечения онкологических заболеваний Физические основы воздействия на атмосферные процессы. Реагенты
Физические основы воздействия на атмосферные процессы. Реагенты Спектрофотометрия видимой области спектра
Спектрофотометрия видимой области спектра Двигатель автомобиля
Двигатель автомобиля Аморфні та склоподібні матеріали. (Лекція 2)
Аморфні та склоподібні матеріали. (Лекція 2) Трансформаторы тока
Трансформаторы тока Термодинамика и теплопередача. Влажный воздух
Термодинамика и теплопередача. Влажный воздух Динамика вращения твердого тела. Кинетическая энергия вращательного движения твердого тела. Лекция 7
Динамика вращения твердого тела. Кинетическая энергия вращательного движения твердого тела. Лекция 7 Равновесие при наличии трения
Равновесие при наличии трения Цепные передачи. Общие сведения. Геометрия и кинематика передачи. Устройство цепи и звездочек. Лекция 2
Цепные передачи. Общие сведения. Геометрия и кинематика передачи. Устройство цепи и звездочек. Лекция 2 Плотность тела
Плотность тела Биоэнергетика, биологиялық энергетика
Биоэнергетика, биологиялық энергетика Өлшеу сигналдары. Өлшеу сигналдарын кванттау мен дискреттеу Өлшеу сигналдарының жіктелуі
Өлшеу сигналдары. Өлшеу сигналдарын кванттау мен дискреттеу Өлшеу сигналдарының жіктелуі Великий сын России. 19 ноября 2011 года Россия отмечала 300 лет со дня рождения выдающегося ученого, титана человеческой мысли, насто
Великий сын России. 19 ноября 2011 года Россия отмечала 300 лет со дня рождения выдающегося ученого, титана человеческой мысли, насто