Содержание
- 2. Раздел 2. ОСНОВНЫЕ ПОЛОЖЕНИЯ ТЕРМОДИНАМИКИ И ТЕПЛОТЕХНИКИ Учебные вопросы 2.1. Термодинамические системы. Уравнения состояния парогазовых систем
- 3. Учебный вопрос №2.1 ТЕРМОДИНАМИЧЕСКИЕ СИСТЕМЫ. УРАВНЕНИЯ СОСТОЯНИЯ ПАРОГАЗОВЫХ СИСТЕМ
- 4. Проблемы, связанные с осуществлением тепловых процессов, рассматриваются термодинамикой и теплотехникой. Термодинамика изучает процессы в системах путем
- 5. Основным понятием термодинамики является понятие термодинамической системы - совокупности материальных тел, являющихся объектами изучения, которые могут
- 6. В термодинамике вводится другое и более простое понятие состояния системы. Во-первых, невозможно множество точечных масс (атомов
- 7. В такой системе измеряются температура t, объем V и давление P. Следует заметить, что термодинамические свойства
- 8. Для данного количества вещества, содержащегося в системе, температура, объем и давление не являются независимыми величинами; они
- 9. Перед тем, как начать обсуждение, какие конкретно соотношения характеризуют связь между параметрами уравнения состояния, напомним, как
- 10. В термодинамической шкале температур началом отсчета служит температура "абсолютного нуля" 0 град. К = - 273,15
- 11. Считается, что при абсолютной температуре, равной нулю, прекращается тепловое движение молекул. В то же время предполагается,
- 12. где m - масса молекулы; v - средняя скорость поступательного движения молекул; k - постоянная Больцмана,
- 13. Изменение импульса каждой молекулы найдем как разность импульсов после и до удара: (-mv)-mv=-2mv. Согласно третьему закону
- 14. С учетом сказанного можно считать, что давление p зависит от числа молекул в единице объема и
- 15. Закон, устанавливающий зависимость давления определенной массы газа от температуры при постоянном объеме, открыт Шарлем (закон Шарля):
- 16. При охлаждении газа ниже 0°C, температура t° будет иметь отрицательные значения. При низких температурах, когда газ
- 17. Другими словами, закон Шарля может быть сформулирован в другой форме: давление данной массы газа при постоянном
- 18. Формула, выражающая данный закон, имеет вид, аналогичный формуле закона Шарля, V=V0°C(1+ βt°), где - коэффициент объемного
- 19. Закон Гей-Люссака также применим как к температурам выше 0°С, так и ниже, но им нельзя пользоваться,
- 20. Если ρ1 и ρ2 - плотности газа при температурах T1 и T2, то имеет место соотношение
- 21. Другими словами, для данной массы газа произведение объема газа на его давление при постоянной температуре остается
- 22. Так, при соблюдении постоянства температуры процесс носит название изотермического, а соответствующие кривые носят название "изотермы". Если
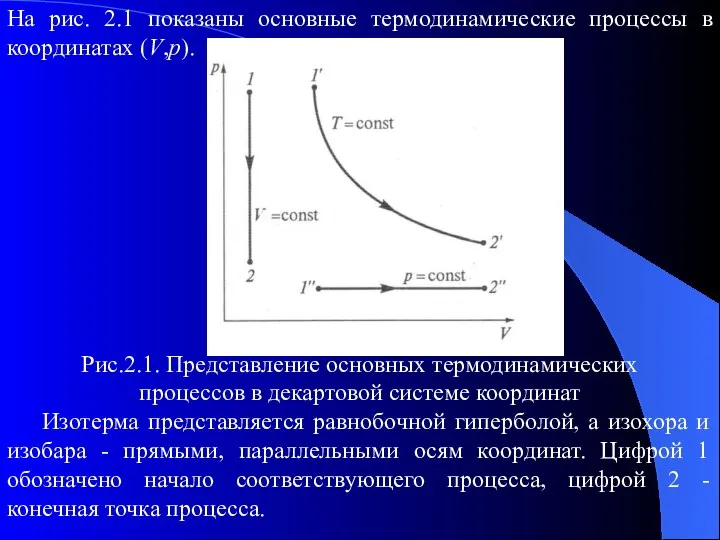
- 23. На рис. 2.1 показаны основные термодинамические процессы в координатах (V,p). Рис.2.1. Представление основных термодинамических процессов в
- 24. Объединение законов Шарля, Гей-Люссака и Бойля-Мариотта дает уравнение состояния идеального газа, которое для системы, содержащей n;
- 25. Моль (русское обозначение: моль; международное: mol; устаревшее название грамм-молекула (по отношению к количеству молекул); от лат.
- 26. Из определения моля непосредственно следует, что молярная масса углерода-12 равна 12 г/моль. Количество специфицированных структурных элементов
- 28. Таким образом, масса одного моля вещества (молярная масса) равна массе одной частицы вещества, атома или молекулы,
- 29. В ряде случаев полезной оказывается формула, связывающая плотность газа ρ с его температурой и давлением: Реальные
- 30. Наиболее простым и качественно верно отображающим изменение состояние реального газа является уравнение Ван-дер-Ваальса, которое для единицы
- 31. Термодинамическая система называется изолированной, если она не допускает обмена с окружающей средой как теплотой, так и
- 32. Равновесным называется такое состояние системы, при котором во всех точках ее объема все термодинамические параметры состояния
- 33. Если в термодинамическом процессе не происходит теплообмена с окружающей средой, то такой процесс носит название адиабатного.
- 34. Гра́дус Фаренге́йта (обозначение: °F) — единица измерения температуры. Назван в честь немецкого учёного Габриеля Фаренгейта, предложившего
- 35. По изначальному предложению ноль по шкале Фаренгейта определялся по самоподдерживающейся температуре смеси воды, льда и хлорида
- 36. Шкала Фаренгейта использовалась в англоязычных странах до 1960-х годов. Затем большинство тех стран перешло на метрическую
- 39. Шкала Ранкина (измеряется в градусах Ранкина — °Ra) — абсолютная температурная шкала, названа по имени шотландского
- 40. Градус Рёмера (°Rø) — неиспользуемая ныне единица температуры. Температурная шкала Рёмера была создана в 1701 году
- 41. Градус Ньютона (°N) — не используемая ныне единица температуры. Температурная шкала Ньютона была разработана Исааком Ньютоном
- 42. Гра́дус Дели́ля (обозначение: °Д или °D)— ныне неупотребляемая единица измерения температуры. Была изобретена французским астрономом Жозефом
- 43. «Перевернутость» этой шкалы (как и изначального варианта шкалы Цельсия) по сравнению с принятыми в настоящее время
- 44. Гра́дус Реомю́ра (°R) — единица измерения температуры, в которой температуры замерзания и кипения воды приняты за
- 45. Однако из-за того, что в качестве жидкости в те времена использовался не только спирт, но и
- 46. Учебный вопрос №2.2 РАБОТА В ТЕРМОДИНАМИЧЕСКОМ ПРОЦЕССЕ
- 47. Во время термодинамического процесса система может совершать положительную или отрицательную внешнюю работу, т.е система может выполнять
- 48. Но Sdh равно изменению объема dV системы. Следовательно, можно записать: dL=pdV. Для конечного процесса работу по
- 49. В соответствии с последним выражением работа, совершаемая в течение этого процесса, выражается интегралом где пределы интегрирования
- 50. Этот интеграл, а следовательно, и проделанная работа геометрически могут быть представлены заштрихованной на рис.2.2 а площадью.
- 51. Следует подчеркнуть, что проделанная работа является положительной, так как цикл протекал в направлении по часовой стрелке.
- 52. Учебный вопрос №2.3 КРИТИЧЕСКОЕ СОСТОЯНИЕ ВЕЩЕСТВА
- 53. В термодинамике существует понятие критического состояния вещества, впервые введенное Д.И.Менделеевым в 1861 г. Критической температурой Tк
- 54. Типичная изотерма для газа, находящегося при температуре ниже критической (t Рис. 2.3. Изотермы в окрестности критической
- 55. Представим себе жидкость, заключенную в цилиндр с поршнем. Пространство между поверхностью жидкости и поверхностью поршня будет
- 56. Если теперь сжимать систему, сохраняя по-прежнему температуру постоянной, то давление повышается до тех пор, пока не
- 57. С повышением температуры величина горизонтального участка уменьшается, и при t≥TК горизонтальный участок изотермы исчезает. При дальнейшем
- 58. Учебный вопрос №2.4 ПЕРВОЕ НАЧАЛО (ПЕРВЫЙ ЗАКОН) ТЕРМОДИНАМИКИ
- 59. Первое начало (первый закон) термодинамики представляет собой формулировку принципа сохранения энергии для термодинамических систем. Чтобы уточнить
- 60. Когда на систему действуют внешние силы, то равенство не соблюдается. Если (-L) представляет работу, совершаемую внешними
- 61. При взаимодействии тел в термодинамическом процессе тела обмениваются энергией. При этом возможны два пути передачи энергии.
- 62. Второй путь. Повышаем температуру воды посредством трения лопастей, погруженных в воду и вращаемых с помощью некоторого
- 63. Величина, обратная термическому эквиваленту работы, называется механическим эквивалентом теплоты, который, очевидно, равен 0,2388 кал/Дж. Если система
- 64. Для термически неизолированной системы левая часть последнего уравнения будет отличаться от нуля, т.к. обмен энергией может
- 65. Известны следующие формулировки данного закона: 1. Энергия не исчезает, а переходит из одной формы в другую.
- 66. Учебный вопрос №2.5 ТЕПЛОЕМКОСТЬ
- 67. При подводе или отводе теплоты температура любого тела повышается или понижается. Способность поглощать теплоту зависит от
- 68. Для соблюдения единообразия обозначений в формулах условимся в дальнейшем обозначать соответствующие величины (количество теплоты, внутреннюю энергию
- 69. Определим, как связаны между собой удельные теплоемкости cp и cV для идеального газа. Запишем уравнение (2.3)
- 70. Величина du в точности соответствует увеличению внутренней энергии газа. А поскольку собственно внутренняя энергия газа определяется
- 71. Поскольку для процесса при постоянном давлении dp=0, то из последнего уравнения следует связь между теплоемкостями cp
- 72. Учебный вопрос №2.6 ВТОРОЕ НАЧАЛО (ВТОРОЙ ЗАКОН) ТЕРМОДИНАМИКИ
- 73. Первое начало термодинамики, констатируя непреложность принципа сохранения количества энергии при ее превращениях, не дает ответа на
- 74. Второе начало (второй закон) термодинамики исключает возможность построения такой машины. Этот закон устанавливает, что самопроизвольные процессы
- 75. Понятие компенсации и другие формулировки второго закона термодинамики будут даны ниже, а сейчас отметим следующее. С
- 76. Теплота, связанная с движением молекул и атомов, является микрофизической формой передачи энергии, а работа, связанная с
- 78. Скачать презентацию










































































 Методы и средства регистрации ионизирующих излучений. Газонаполненные детекторы
Методы и средства регистрации ионизирующих излучений. Газонаполненные детекторы Резьбовые соединения
Резьбовые соединения Открытие магнитного поля. Параметры, характеризующие магнитное поле. Магнитная проницаемость среды
Открытие магнитного поля. Параметры, характеризующие магнитное поле. Магнитная проницаемость среды МОУ «Основная общеобразовательная школа №9» Электромагнитное излучение Рентгеновские излучения Выполнил : ученик 8 класса Ники
МОУ «Основная общеобразовательная школа №9» Электромагнитное излучение Рентгеновские излучения Выполнил : ученик 8 класса Ники Сила. Единицы силы
Сила. Единицы силы Физика в живой природе
Физика в живой природе Презентация по физике на тему «Производство электроэнергии. Передача электроэнергии на расстоянии.» Ученицы 9 класса «В» Зениной
Презентация по физике на тему «Производство электроэнергии. Передача электроэнергии на расстоянии.» Ученицы 9 класса «В» Зениной ВВЕДЕНИЕ В ФИЗИКУ И МОДЕЛИРОВАНИЕ ФОТОННЫХ КРИСТАЛЛОВ Лекция 3 2013
ВВЕДЕНИЕ В ФИЗИКУ И МОДЕЛИРОВАНИЕ ФОТОННЫХ КРИСТАЛЛОВ Лекция 3 2013 Колокол дремавший… (колокол как источник звуковых волн)
Колокол дремавший… (колокол как источник звуковых волн) Рейка с подогревом
Рейка с подогревом Свойства жидкостей. Поверхностное натяжение
Свойства жидкостей. Поверхностное натяжение  Інфразвук. Джерела інфразвуку
Інфразвук. Джерела інфразвуку Розвиток літакобудування та ракетної техніки
Розвиток літакобудування та ракетної техніки Сила упругости
Сила упругости «Работы М.В.Ломоносова в области физики: размышления о причине теплоты и холода»
«Работы М.В.Ломоносова в области физики: размышления о причине теплоты и холода»  Высочайшие здания мира с точки зрения физики
Высочайшие здания мира с точки зрения физики 8 класс 2009
8 класс 2009 Абрам Федорович Иоффе — создатель отечественной физической школы Презентация
Абрам Федорович Иоффе — создатель отечественной физической школы Презентация Теорія електричних та магнітних кіл (лекція 1)
Теорія електричних та магнітних кіл (лекція 1) Презентация по физике "Электризация тел. Взаимодействие заряженных тел. Два рода зарядов" - скачать
Презентация по физике "Электризация тел. Взаимодействие заряженных тел. Два рода зарядов" - скачать  Работа и мощность. Решение задач
Работа и мощность. Решение задач Кремний - как полупроводник
Кремний - как полупроводник Презентація на тему: “Надпровідникові прилади та їх застосування”
Презентація на тему: “Надпровідникові прилади та їх застосування”  Элементы квантовой статистики. (Лекция 8)
Элементы квантовой статистики. (Лекция 8) Двигатели внутреннего сгорания
Двигатели внутреннего сгорания Презентация по физике "Влажность воздуха" - скачать бесплатно
Презентация по физике "Влажность воздуха" - скачать бесплатно Сила упругости. Закон Гука
Сила упругости. Закон Гука Подготовила: Котрецкая Т.А. учитель физики СОШ №20 г.Донецк Ростовской области
Подготовила: Котрецкая Т.А. учитель физики СОШ №20 г.Донецк Ростовской области